Structuur en functies
Hemoglobine is een metalloproteïne dat zich in rode bloedcellen bevindt en verantwoordelijk is voor het transport van zuurstof in de bloedbaan.Zuurstof is in feite slechts matig oplosbaar in water; daarom zijn de in het bloed opgeloste hoeveelheden (minder dan 2% van het totaal) niet voldoende om aan de metabolische eisen van de weefsels te voldoen. De behoefte aan een specifieke vervoerder is dan ook evident.
In de bloedbaan kan zuurstof niet direct en omkeerbaar aan eiwitten binden, zoals in plaats daarvan gebeurt voor metalen zoals koper en ijzer.Het is niet verrassend dat we in het midden van elke eiwitsubeenheid van hemoglobine, verpakt in een eiwitomhulsel, de zogenaamde prothetische groep EME, met een metallisch hart vertegenwoordigd door een ijzeratoom in de Fe2 + oxidatietoestand (gereduceerde toestand), die zuurstof op een omkeerbare manier bindt.
Bloedanalyse
- Normale hemoglobinewaarden in het bloed: 13-17 g/100 ml
Bij vrouwen zijn de waarden gemiddeld 5-10% lager dan bij mannen.
Mogelijke oorzaken van hoge hemoglobine
- Polycytemie
- Verlengd verblijf op de hoge grond
- Chronische longziekten
- Hartziekte
- Bloeddoping (gebruik van erytropoëtine en derivaten of stoffen die hun werking nabootsen)
Mogelijke oorzaken van lage hemoglobine
- Bloedarmoede
- IJzertekort (ijzertekort)
- Overvloedig bloeden
- carcinomen
- Zwangerschap
- thalassemieën
- brandwonden
Het zuurstofgehalte in het bloed wordt dus bepaald door de optelling van de kleine hoeveelheid opgelost in het plasma met de fractie gebonden aan hemoglobine-ijzer.
Meer dan 98% van de zuurstof in het bloed is gebonden aan hemoglobine, dat op zijn beurt circuleert in de bloedbaan die is toegewezen aan de rode bloedcellen.Zonder hemoglobine zouden de erytrocyten daarom hun taak als zuurstoftransporteur in het bloed niet kunnen vervullen.
Gezien de centrale rol van dit metaal, vereist de synthese van hemoglobine een adequate inname van ijzer in de voeding. Ongeveer 70% van het ijzer dat in het lichaam aanwezig is, zit namelijk in de heemgroepen van hemoglobine.
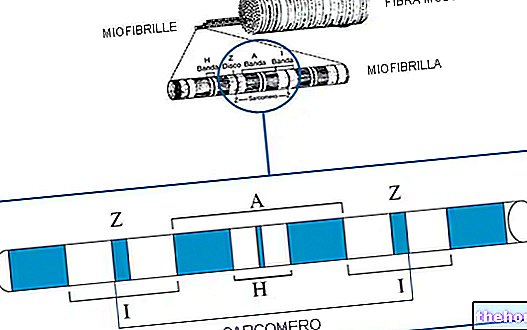
Hemoglobine bestaat uit 4 subeenheden die qua structuur sterk lijken op myoglobine*.
* Terwijl hemoglobine zuurstof van de longen naar de weefsels transporteert, transporteert myoglobine de zuurstof die door hemoglobine wordt afgegeven naar de verschillende cellulaire organellen die het gebruiken (bijv. mitochondriën).

Hemoglobine is een groot en complex metalloproteïne, gekenmerkt door vier bolvormige eiwitketens die respectievelijk zijn gewikkeld rond een heemgroep die Fe2+ bevat.
Voor elk hemoglobinemolecuul vinden we daarom vier heemgroepen verpakt in de relatieve bolvormige eiwitketen. Omdat er vier ijzeratomen in elk hemoglobinemolecuul zitten, kan elk hemoglobinemolecuul vier zuurstofatomen aan zichzelf binden, volgens de omkeerbare reactie:
Hb + 4O2 ← → Hb (O2) 4
Zoals de meesten bekend is, is de taak van hemoglobine om zuurstof in de longen op te nemen, het af te geven aan de cellen die het nodig hebben, koolstofdioxide uit hen te nemen en het af te geven in de longen waar de chilo opnieuw begint.
Tijdens de doorgang van bloed in de haarvaten van de longblaasjes, bindt hemoglobine zuurstof aan zichzelf, die vervolgens wordt afgegeven aan de weefsels in de perifere circulatie. Deze uitwisseling vindt plaats omdat de bindingen van zuurstof met het ijzer van de EME-groep labiel en gevoelig zijn voor vele factoren, waarvan de belangrijkste de spanning of partiële zuurstofdruk is.
Binding van zuurstof aan hemoglobine en het Bohr-effect
In de longen neemt de zuurstofspanning in het plasma toe door de diffusie van gas van de longblaasjes naar het bloed (↑ PO2); deze toename zorgt ervoor dat hemoglobine zich gretig bindt aan zuurstof; het tegenovergestelde doet zich voor in de perifere weefsels, waar de concentratie van opgeloste zuurstof in het bloed afneemt (↓ PO2) en de partiële druk van kooldioxide toeneemt (↑ CO2); dit zorgt ervoor dat hemoglobine zuurstof afgeeft en geladen wordt met CO 2. Het concept zoveel mogelijk vereenvoudigen, hoe meer koolstofdioxide in het bloed aanwezig is, hoe minder zuurstof er aan hemoglobine gebonden blijft.
Hoewel de hoeveelheid fysiek in het bloed opgeloste zuurstof erg laag is, speelt het daarom een fundamentele rol. In feite heeft deze hoeveelheid een grote invloed op de bindingssterkte tussen zuurstof en hemoglobine (en vertegenwoordigt het ook een "belangrijke referentiewaarde bij het reguleren van de longventilatie).
Alles samenvattend met een grafiek, groeit de hoeveelheid zuurstof gekoppeld aan hemoglobine in verhouding tot de pO2 volgens een sigmoïde curve:

Het feit dat het plateaugebied zo groot is, plaatst een belangrijke veiligheidsmarge bij de maximale verzadiging van hemoglobine tijdens de passage in de longen Hoewel de pO2 op het alveolaire niveau normaal gesproken gelijk is aan 100 mm Hg, zien we bij het bekijken van de figuur in feite hoe zelfs een partiële zuurstofdruk gelijk aan 70 mmHg (typisch voorkomen van sommige ziekten of van verblijf op grote hoogte), blijven de percentages verzadigde hemoglobine dicht bij 100%.
In het gebied van maximale helling, wanneer de partiële zuurstofspanning onder 40 mmHg daalt, neemt het vermogen van hemoglobine om zuurstof te binden plotseling af.
In rusttoestand is de PO2 in intracellulaire vloeistoffen ongeveer 40 mmHg; op deze plaats diffundeert de in het plasma opgeloste zuurstof naar de armere weefsels van O2, door het capillaire membraan, door de wetten van gassen, waardoor de plasmaspanning van O2 verder daalt en dit bevordert de afgifte van zuurstof uit de hemoglobine. . Bij zware lichamelijke inspanning daarentegen daalt de zuurstofspanning in de weefsels tot 15 mmHg of minder, waardoor het bloed sterk zuurstofarm wordt.
Zoals gezegd, in rust verlaat een belangrijke hoeveelheid zuurstofrijk hemoglobine de weefsels en blijft beschikbaar in geval van nood (bijvoorbeeld om het hoofd te bieden aan een plotselinge toename van het metabolisme in sommige cellen).
De ononderbroken lijn die in de afbeelding hierboven wordt getoond, wordt de hemoglobine-dissociatiecurve genoemd; het wordt typisch in vitro bepaald bij pH 7,4 en bij een temperatuur van 37 ° C.
Het Bohr-effect heeft zowel gevolgen voor de opname van O2 op longniveau als voor de afgifte ervan op weefselniveau.
Waar meer koolstofdioxide is opgelost in de vorm van bicarbonaat, geeft hemoglobine gemakkelijker zuurstof af en wordt het geladen met koolstofdioxide (in de vorm van bicarbonaat).

Hetzelfde effect wordt bereikt door het bloed aan te zuren: hoe meer de pH van het bloed daalt en hoe minder zuurstof aan de hemoglobine gebonden blijft; het is niet verrassend dat in het bloed kooldioxide voornamelijk wordt opgelost in de vorm van koolzuur, dat dissocieert.



Ter ere van zijn ontdekker staat het effect van pH of kooldioxide op zuurstofdissociatie bekend als het Bohr-effect.
Zoals verwacht geeft hemoglobine in een zure omgeving gemakkelijker zuurstof af, terwijl in een basische omgeving de binding met zuurstof sterker is.

Andere factoren die de affiniteit van hemoglobine voor zuurstof kunnen wijzigen, zijn onder meer de temperatuur. Met name de affiniteit van hemoglobine voor zuurstof neemt af met toenemende lichaamstemperatuur. Dit is vooral voordelig tijdens de winter- en lentemaanden, aangezien de temperatuur van het longbloed (in contact met de lucht van de externe omgeving) lager is dan die in de weefsels wordt bereikt, waar de afgifte van zuurstof daardoor wordt vergemakkelijkt.

2.3 difosfoglyceraat is een tussenproduct in glycolyse dat de affiniteit van hemoglobine voor zuurstof beïnvloedt. Als de concentraties in de rode bloedcellen toenemen, neemt de affiniteit van hemoglobine voor zuurstof af, waardoor de afgifte van zuurstof aan de weefsels wordt vergemakkelijkt. Het is niet verrassend dat de erytrocytenconcentraties verhoging van 2,3 difosfoglyceraat, bijvoorbeeld bij bloedarmoede, hart- en longinsufficiëntie en tijdens het verblijf op grote hoogte.
Over het algemeen is het effect van 2,3-bisfosfoglyceraat relatief langzaam, vooral in vergelijking met de snelle reactie op veranderingen in pH, temperatuur en partiële druk van kooldioxide.

Het Bohr-effect is erg belangrijk tijdens intensief spierwerk; in dergelijke omstandigheden is er in feite in de weefsels die het meest worden blootgesteld aan stress, een lokale toename van de temperatuur en druk van kooldioxide, en dus van de zuurgraad van het bloed. Zoals hierboven uitgelegd, bevordert dit alles de afgifte van zuurstof aan de weefsels, waardoor de hemoglobinedissociatiecurve naar rechts verschuift.