Actieve ingrediënten: Mycofenolzuur (natriummycofenolaat)
Myfortic 360 mg maagsapresistente tabletten
Myfortic-bijsluiters zijn beschikbaar voor verpakkingsgrootten:- Myfortic 180 mg maagsapresistente tabletten
- Myfortic 360 mg maagsapresistente tabletten
Indicaties Waarom wordt Myfortic gebruikt? Waar is het voor?
Myfortic bevat een stof genaamd mycofenolzuur. Het behoort tot een groep geneesmiddelen die immunosuppressiva worden genoemd.
Myfortic wordt gebruikt om te voorkomen dat het immuunsysteem een getransplanteerde nier afstoot. Het wordt gebruikt in combinatie met andere geneesmiddelen die ciclosporine en corticosteroïden bevatten.
Contra-indicaties Wanneer Myfortic niet mag worden gebruikt
Mycofenolaat veroorzaakt geboorteafwijkingen en miskramen. Als u een vrouw bent die zwanger kan worden, moet u een negatieve zwangerschapstest afleggen voordat u met de behandeling begint en moet u het anticonceptieadvies van uw arts opvolgen.
Uw arts zal met u praten en u schriftelijke informatie geven, vooral over de effecten van mycofenolaat op het ongeboren kind. Lees de informatie aandachtig en volg de instructies.
Als u de instructies niet helemaal begrijpt, vraag dan uw arts om ze nogmaals uit te leggen voordat u mycofenolaat inneemt.Meer informatie vindt u in deze rubriek onder "Waarschuwingen en voorzorgsmaatregelen" en "Zwangerschap en borstvoeding".
Gebruik Myfortic niet:
- als u allergisch (overgevoelig) bent voor mycofenolzuur, mycofenolaatnatrium, mycofenolaatmofetil of voor één van de andere bestanddelen van dit geneesmiddel
- als u een vrouw bent in de vruchtbare leeftijd (die zwanger kan worden) en vóór het eerste recept geen negatieve zwangerschapstest heeft afgegeven, aangezien mycofenolaat geboorteafwijkingen en miskramen veroorzaakt
- als u zwanger bent of van plan bent zwanger te worden of denkt dat u zwanger zou kunnen zijn
- als u geen effectieve anticonceptie gebruikt (zie Anticonceptie voor vrouwen en mannen)
- als u borstvoeding geeft (zie ook "Zwangerschap en borstvoeding").
Als dit op u van toepassing is, vertel het dan uw arts zonder Myfortic in te nemen.
Voorzorgen bij gebruik Wat u moet weten voordat u Myfortic inneemt
Neem contact op met uw arts of apotheker voordat u Myfortic inneemt:
- als u ernstige spijsverteringsstoornissen heeft of ooit heeft gehad, zoals een maagzweer.
- als u een zeldzame erfelijke deficiëntie van het enzym hypoxanthine-guanine-fosforibosyltransferase (HGPRT) heeft, zoals het Lesch-Nyhan-syndroom en het Kelley-Seegmille-syndroom.
Hij moet ook worden geïnformeerd dat:
- Myfortic vermindert het beschermingsniveau van de opperhuid tegen de zon. Dit verhoogt het risico op huidkanker. Het moet blootstelling aan de zon en ultraviolette stralen (UV) beperken door de blootgestelde delen zoveel mogelijk te beschermen en door regelmatig een hoogbeschermende zon aan te brengen crèmes. Vraag uw arts om advies over hoe u uzelf tegen de zon kunt beschermen.
- Als u al hepatitis B of C heeft gehad, kan Myfortic het risico op deze ziekten verhogen door ervoor te zorgen dat ze terugkomen. Uw arts kan bloedonderzoeken uitvoeren en de symptomen van deze ziekten controleren. Als u symptomen heeft (gele ogen en huid, misselijkheid, verlies van eetlust, donkere urine) moet u uw arts onmiddellijk informeren.
- Als u aanhoudend hoest of kortademig bent, vooral als u andere immunosuppressiva gebruikt, moet u dit onmiddellijk aan uw arts vertellen.
- Uw arts kan u vragen om de hoeveelheid antistoffen in uw bloed te controleren tijdens de behandeling met Myfortc, vooral wanneer infecties terugkeren, vooral als u ook met andere immunosuppressiva wordt behandeld, en hij zal u informeren of u de behandeling met Myfortic kunt voortzetten.
- Als u tekenen van infectie heeft (zoals koorts of keelpijn) of als u onverwachte blauwe plekken of bloedingen krijgt, moet u dit onmiddellijk aan uw arts vertellen.
- Uw arts kan u vragen om uw witte bloedcelwaarden te controleren tijdens de behandeling met Myfortic en zal u informeren of u de behandeling met Myfortic kunt voortzetten.
- De werkzame stof, mycofenolzuur, is anders dan die van andere geneesmiddelen met een vergelijkbare naam, zoals mycofenolaatmofetil. U mag niet tussen geneesmiddelen wisselen, tenzij uw arts u dat zegt.
- Het gebruik van Myfortic tijdens de zwangerschap kan schadelijk zijn voor een ongeboren baby (zie ook "Zwangerschap en borstvoeding") en kan het risico op zwangerschapsverlies (miskraam) vergroten.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Myfortic . veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken, ook als u geneesmiddelen gebruikt die u zonder voorschrift kunt krijgen. In het bijzonder moet u uw arts informeren als u een van de volgende geneesmiddelen gebruikt:
- andere immunosuppressiva zoals azathioprine of tacrolimus.
- geneesmiddelen die worden gebruikt om een hoog cholesterolgehalte in het bloed te behandelen, zoals colestyramine.
- actieve kool gebruikt voor de behandeling van spijsverteringsstoornissen zoals diarree, maagklachten en een opgeblazen gevoel.
- antacida die magnesium en aluminium bevatten.
- geneesmiddelen die worden gebruikt om virale infecties te behandelen, zoals aciclovir of ganciclovir.
Vertel het ook aan uw arts als u van plan bent zich te laten vaccineren.
U mag geen bloed doneren tijdens de behandeling met Myfortic en gedurende ten minste 6 weken na het stoppen van de behandeling Mannen mogen geen sperma doneren tijdens de behandeling met Myfortic en gedurende ten minste 90 dagen na het stoppen van de behandeling.
Myfortic kan met of zonder voedsel worden ingenomen. U moet kiezen of u de tabletten met of zonder voedsel wilt innemen en ze vervolgens elke dag op dezelfde manier blijven innemen. Op deze manier is het veilig om elke dag dezelfde hoeveelheid geneesmiddel op te nemen.
Waarschuwingen Het is belangrijk om te weten dat:
Bejaarden
Oudere mensen (van 65 jaar en ouder) kunnen Myfortic gebruiken zonder de gebruikelijke aanbevolen dosis aan te passen.
Pediatrische en adolescente populatie
Vanwege het gebrek aan gegevens wordt het gebruik van Myfortic bij kinderen en adolescenten niet aanbevolen.
Zwangerschap en borstvoeding
Als u zwanger bent of borstvoeding geeft, denkt zwanger te zijn of zwanger wilt worden, vraag dan uw arts of apotheker om advies voordat u dit geneesmiddel inneemt. Uw arts zal met u praten over de risico's om zwanger te worden en over alternatieve therapieën die u kunt nemen om afstoting van het getransplanteerde orgaan te voorkomen als:
- een zwangerschap plannen.
- als u een menstruatie heeft gemist of denkt te hebben overgeslagen of een ongewone menstruatiebloeding opmerkt of vermoedt dat u zwanger bent.
- seks hebben zonder een effectieve anticonceptiemethode te gebruiken.
Als u zwanger wordt terwijl u mycofenolaat gebruikt, dient u onmiddellijk uw arts te informeren. Blijf mycofenolaat echter innemen totdat u uw arts heeft gezien.
Zwangerschap
Mycofenolaat veroorzaakt een zeer hoge frequentie van spontane abortussen (50%) en ernstige geboorteafwijkingen (23 - 27%) bij het ongeboren kind. Geboorteafwijkingen die zijn gemeld, zijn onder meer afwijkingen van de oren, ogen, gezicht (lip/gehemelte), ontwikkeling van de vingers, het hart, de slokdarm (het kanaal dat de keel met de maag verbindt), de nieren en het zenuwstelsel (voor bijvoorbeeld spina bifida (waarbij de botten van de wervelkolom niet goed zijn ontwikkeld) Een of meer hiervan kunnen invloed hebben op uw baby.
Als u een vrouw bent die zwanger kan worden, moet u een negatieve zwangerschapstest afleggen voordat u met de behandeling begint en moet u het anticonceptieadvies van uw arts opvolgen. Uw arts kan om meer dan één test vragen om er zeker van te zijn dat u niet zwanger bent voordat u met de behandeling begint.
Voedertijd
Gebruik Myfortic niet als u borstvoeding geeft. Dit komt omdat kleine hoeveelheden van het geneesmiddel in de moedermelk terecht kunnen komen.
Anticonceptie bij vrouwen die Myfortic® gebruiken
Als u een vrouw bent in de vruchtbare leeftijd, moet u altijd twee effectieve anticonceptiemethoden gebruiken met Myfortic. Dit bevat:
- Voordat u begint met de behandeling met Myfortic
- Gedurende de gehele behandelingsperiode met Myfortic
- Gedurende 6 weken na het stoppen van de behandeling met Myfortic.
Praat met uw arts over de meest geschikte anticonceptiemethode voor u. Dit is afhankelijk van uw persoonlijke situatie. Neem zo snel mogelijk contact op met uw arts als u denkt dat de anticonceptiemethode niet werkt en als u bent vergeten de anticonceptiepil in te nemen.
Als een van de volgende situaties op u van toepassing is, kunt u uzelf als een onvruchtbare vrouw beschouwen:
- Ze is postmenopauzaal, dwz ze is minstens 50 jaar oud en haar laatste menstruatie vond meer dan een jaar geleden plaats (als haar menstruatie was gestopt omdat ze een kankerbehandeling kreeg, bestaat de mogelijkheid dat ze zwanger blijft)
- Haar eileiders en beide eierstokken zijn operatief verwijderd (bilaterale salpingovariectomie)
- Haar baarmoeder werd operatief verwijderd (hysterectomie)
- Uw eierstokken werken niet meer (vroeg ovariumfalen bevestigd door een gynaecoloog-specialist)
- Ze werd geboren met een van de volgende zeldzame aandoeningen die zwangerschap onmogelijk maken: het XY-genotype, het syndroom van Turner of uteriene agenesie.
- Het is een "meisje of een" tiener die haar eerste menstruatie nog niet heeft gehad.
Anticonceptie bij mannen die Myfortic® gebruiken
U moet altijd een condoom gebruiken tijdens de behandeling en gedurende ten minste 90 dagen na het stoppen met Myfortic
Als u van plan bent om te bevallen, zal uw arts u informeren over de risico's en alternatieve behandelingen die u kunt nemen om afstoting van het getransplanteerde orgaan te voorkomen.
Rijvaardigheid en het gebruik van machines
Myfortic lijkt geen invloed te hebben op de rijvaardigheid of het vermogen om machines te bedienen.
Myfortic bevat lactose
Als uw arts u heeft verteld dat u bepaalde suikers (waaronder lactose, galactose of glucose) niet verdraagt, neem dan contact op met uw arts voordat u Myfortic inneemt.
Dosis, wijze en tijdstip van toediening Hoe Myfortic te gebruiken: Dosering
Gebruik Myfortic altijd precies zoals uw arts u dat heeft verteld. Myfortic wordt alleen aan u voorgeschreven door artsen die ervaring hebben met de behandeling van transplantatiepatiënten. Raadpleeg bij twijfel uw arts of apotheker.
Welke dosis te nemen?
De aanbevolen dagelijkse dosis Myfortic is 1440 mg (8 tabletten Myfortic 180 mg). Ze worden ingenomen in 2 afzonderlijke doses van elk 720 mg (4 Myfortic-tabletten van 180 mg). Neem de tabletten 's morgens en' s avonds in.
De eerste dosis van 720 mg zal u binnen 72 uur na de transplantatie worden toegediend.
Als u ernstige nierproblemen heeft
De dagelijkse dosis mag niet hoger zijn dan 1440 mg (8 tabletten Myfortic 180 mg).
Myfortic nemen
Slik de tabletten heel door met een glas water.
De tabletten mogen niet worden gebroken of fijngemaakt.
Neem geen gebroken of gespleten tabletten in
De behandeling zal worden voortgezet zolang immunosuppressie nodig is om afstoting van het getransplanteerde orgaan te voorkomen.
Bent u vergeten Myfortic in te nemen?
Als u bent vergeten Myfortic in te nemen, neem het dan in zodra u het zich herinnert, tenzij het bijna tijd is voor uw volgende dosis. Neem vervolgens uw volgende dosis wanneer u deze naar verwachting zult innemen. Vraag uw arts om advies. Neem geen dubbele dosis om een vergeten dosis in te halen.
Als u stopt met het innemen van Myfortic
Stop niet met het innemen van Myfortic tenzij uw arts u dat zegt.Het stoppen van de behandeling met Myfortic kan het risico op afstoting van een getransplanteerde nier verhogen.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Overdosering Wat moet u doen als u een overdosis Myfortic heeft ingenomen?
Als u meer Myfortic heeft ingenomen dan u is voorgeschreven of als iemand anders uw tabletten heeft ingenomen, neem dan onmiddellijk contact op met uw arts en ga naar een ziekenhuis. Medische behandeling kan nodig zijn. Neem de tabletten mee en laat ze aan uw arts of ziekenhuispersoneel zien. Als u geen tabletten meer heeft, neem dan de lege verpakking mee.
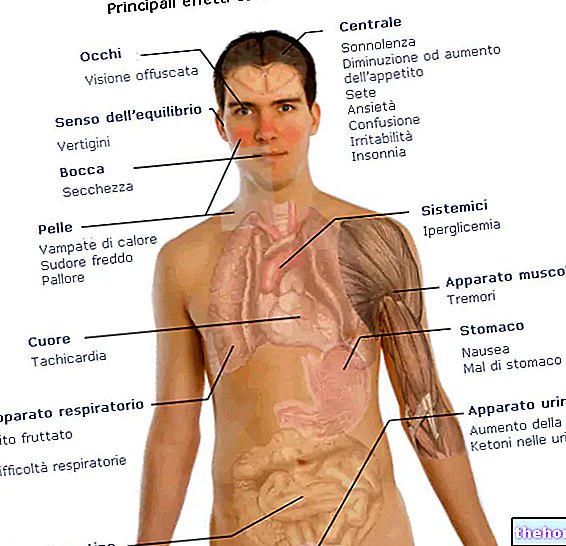
Bijwerkingen Wat zijn de bijwerkingen van Myfortic
Zoals alle geneesmiddelen kan Myfortic bijwerkingen hebben, al krijgt niet iedereen daarmee te maken. Oudere patiënten kunnen meer bijwerkingen krijgen als gevolg van een verminderde immuunafweer.
Immunosuppressiva, waaronder Myfortic, verminderen de afweermechanismen van uw lichaam om te voorkomen dat u uw getransplanteerde orgaan afstoot. Als gevolg hiervan zal uw lichaam zich niet kunnen verdedigen tegen infecties zoals onder normale omstandigheden. Daarom kunt u, als u Myfortic gebruikt, meer infecties krijgen dan normaal, zoals infecties van de hersenen, huid, mond, maag en darmen, longen en urinewegen.
Uw arts zal regelmatig bloedonderzoeken ondergaan om te controleren op veranderingen in het aantal bloedcellen of de hoeveelheid stoffen die in het bloed worden vervoerd, zoals suiker, vet en cholesterol.
Sommige bijwerkingen kunnen ernstig zijn:
- tekenen van infectie, waaronder koorts, koude rillingen, zweten, zich moe, slaperig of gebrek aan energie voelen. Als u Myfortic gebruikt, kunt u vaker dan normaal virale, bacteriële en schimmelinfecties krijgen. Deze infecties kunnen verschillende delen van het lichaam aantasten, maar meestal de nieren, blaas, bovenste en/of onderste luchtwegen.
- bloedend braken, donkere of bloederige ontlasting, maag- of darmzweer.
- zwelling van de klieren, proliferatie van nieuwe huidformaties, toename van het volume van bestaande formaties of veranderingen van een reeds bestaande formatie. Zoals kan gebeuren bij patiënten die worden behandeld met immunosuppressiva, heeft een zeer klein aantal patiënten die Myfortic gebruiken kanker van de huid of lymfeklieren ontwikkeld.
Als u een van de bovenstaande bijwerkingen heeft ervaren na het innemen van Myfortic, neem dan onmiddellijk contact op met uw arts.
Andere bijwerkingen kunnen zijn:
Zeer vaak (komen voor bij meer dan 1 op de 10 patiënten)
- lage niveaus van witte bloedcellen.
- laag calciumgehalte in het bloed (hypocalciëmie)
- lage kaliumspiegels in het bloed (hypokaliëmie)
- hoge niveaus van urinezuur in het bloed (hyperurikemie)
- hoge bloeddruk (hypertensie)
- ongerustheid
- diarree
- gewrichtspijn (artralgie)
Vaak (komen voor bij minder dan 1 op de 10 patiënten)
- laag aantal rode bloedcellen dat vermoeidheid, kortademigheid en bleekheid kan veroorzaken (bloedarmoede)
- laag aantal bloedplaatjes in het bloed, wat onverwachte bloedingen en blauwe plekken kan veroorzaken (trombocytopenie)
- hoge kaliumspiegels in het bloed (hyperkaliëmie)
- laag magnesiumgehalte in het bloed (hypomagnesiëmie)
- duizeligheid
- hoofdpijn
- hoest
- lage bloeddruk (hypotensie)
- kortademigheid (dyspneu)
- pijn in de buik of maag, ontsteking van de maagwand, opgeblazen gevoel, constipatie, dyspepsie, winderigheid, dunne ontlasting, misselijkheid, braken
- vermoeidheid, koorts
- abnormale resultaten van lever- en nierfunctietesten
- luchtweginfecties
- acne
- zwakte (asthenie)
- spierpijn (myalgie)
- zwelling van de handen, enkels of voeten (perifeer oedeem)
- jeuk
Soms (treedt op bij minder dan 1 op de 100 patiënten)
- snelle (tachycardie) of onregelmatige hartslag (ventriculaire extrasystolen), vocht in de longen (longoedeem)
- vloeistofbevattende cyste-achtige huidvorming (lymfocele)
- tremor, moeite met slapen
- roodheid en zwelling van de ogen (conjunctivitis), wazig zien
- piepende ademhaling
- oprispingen, moeite met ademhalen, darmblokkade (ileus), ulceratie van de lippen, brandend maagzuur, verkleuring van de tong, droge mond, ontsteking van het tandvlees, ontsteking van de alvleesklier die hevige pijn in de bovenbuik (pancreatitis) veroorzaakt, verstopping van de speekselklieren, ontsteking van de binnenwand van de buik (peritonitis)
- infectie van de botten, het bloed en de huid
- bloed in de urine, nierbeschadiging, pijn en moeite met plassen
- haaruitval, blauwe plekken
- gewrichtsontsteking (artritis), rugpijn, spierkrampen
- verlies van eetlust, verhoogde lipidenspiegels (hyperlipidemie), suiker (diabetes), cholesterol (hypercholesterolemie) of verlaagde fosfaatspiegels in het bloed (hypofosfatemie)
- griepverschijnselen (zoals vermoeidheid, koude rillingen, keelpijn, gewrichts- of spierpijn), zwelling van enkels en voeten, pijn, stijfheid, dorst of zwakte
- abnormale dromen, gevoel van teleurstelling
- onvermogen om een erectie te krijgen of te behouden
- hoesten, ademhalingsmoeilijkheden, pijnlijke ademhaling (mogelijke symptomen van interstitiële longziekte).
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald)
- uitslag
- koorts, keelpijn, frequente infecties (mogelijke symptomen van een tekort aan witte bloedcellen) (agranulocytose)
Andere bijwerkingen gemeld bij geneesmiddelen vergelijkbaar met Myfortic
Bijkomende bijwerkingen zijn gemeld met de groep geneesmiddelen waartoe Myfortic behoort: ontsteking van de dikke darm (dikke darm), ontsteking van de maagwand veroorzaakt door cytomegalovirus, vorming van een laesie in de darmwand die hevige pijn in de buik veroorzaakt met de mogelijkheid van bloeding, maag- of darmzweren, laag aantal witte bloedcellen, specifiek of van alle bloedcellen, ernstige infecties zoals ontsteking van het hart en hartkleppen en vliezen die de hersenen en het ruggenmerg bekleden, kortademigheid, hoest die veroorzaakt door bronchiëctasie (een aandoening waarbij de luchtwegen in de longen abnormaal verwijd zijn) en andere, minder vaak voorkomende bacteriële infecties die gewoonlijk ernstige longproblemen veroorzaken (tuberculose en atypische mycobacteriële infecties).Neem contact op met uw arts als u aanhoudende hoest of kortademigheid heeft .
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op www.agenziafarmaco.it/it/responsabili Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik Myfortic niet meer na de vervaldatum die staat vermeld op de doos. De vervaldatum verwijst naar de laatste dag van de maand.
Niet bewaren boven 30°C.
Bewaar Myfortic in de originele verpakking ter bescherming tegen vocht.Gebruik Myfortic niet als u merkt dat de verpakking beschadigd is of tekenen van manipulatie vertoont.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Andere informatie
Wat bevat Myfortic
- Het werkzame bestanddeel is mycofenolzuur (als natriummycofenolaat).Elke Myfortic-tablet bevat 180 mg mycofenolzuur.
- De hulpstoffen zijn:
- Kerntablet: maïszetmeel, povidon, crospovidon, watervrije lactose, watervrij colloïdaal siliciumdioxide, magnesiumstearaat.
- Tabletomhulling: hypromelloseftalaat, titaandioxide (E 171), geel ijzeroxide (E 172), indigokarmijn (E 132).
Hoe ziet Myfortic eruit en hoeveel zit er in een verpakking?
Myfortic 180 mg maagsapresistente tabletten zijn geelgroen, filmomhuld, rond van vorm en aan één kant bedrukt met "C". Myfortic 180 mg maagsapresistente tabletten zijn verkrijgbaar in blisterverpakkingen met 20, 50, 100, 120 of 250 tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
MYFORTIC 360 MG GASTRORESISTENTE TABLETTEN
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke maagsapresistente tablet bevat 360 mg mycofenolzuur (als natriummycofenolaat).
Hulpstoffen:
Watervrije lactose: 90 mg per tablet.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
03.0 FARMACEUTISCHE VORM
Maagsapresistente tablet.
Lichtoranjerode, ovale, filmomhulde tabletten met aan één kant de inscriptie "CT".
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Myfortic is geïndiceerd in combinatie met ciclosporine en corticosteroïden voor de profylaxe van acute afstoting bij volwassen patiënten die een allogene niertransplantatie ondergaan.
04.2 Dosering en wijze van toediening
Behandeling met Myfortic dient te worden gestart en voortgezet door naar behoren gekwalificeerde transplantatieartsen.
De aanbevolen dosis is 720 mg tweemaal daags (1440 mg dagelijkse dosis). In termen van mycofenolzuur (MPA)-gehalte komt deze natriummycofenolaatdosis overeen met 1 g mycofenolaatmofetil tweemaal daags ingenomen (dagelijkse dosis van 2 g).
Voor meer informatie over het matchen van therapeutische doses mycofenolaatnatrium en mycofenolaatmofetil, zie rubrieken 4.4 en 5.2.
Bij transplantatiepatiënten de-novo De toediening van Myfortic moet binnen 72 uur na de transplantatie worden gestart.
Myfortic kan bij of tussen de maaltijden worden ingenomen. Patiënten kunnen een van de twee toedieningswijzen kiezen, maar zullen deze gedurende de gehele periode van inname van het geneesmiddel moeten bewaren (zie rubriek 5.2).
Myfortic-tabletten mogen niet worden fijngemaakt om de enterische coating intact te houden. In gevallen waar het fijnmaken van Myfortic tabletten nodig is, vermijd inademing van het poeder of direct contact van het poeder met de huid of slijmvliezen.Als contact optreedt, was dan grondig met water en zeep; spoel de ogen alleen met natuurlijk water Dit vanwege de teratogene werking effecten van mycofenolaat.
Pediatrische en adolescente populatie
Er zijn onvoldoende gegevens om de werkzaamheid en veiligheid van Myfortic bij kinderen en adolescenten te documenteren.Er zijn beperkte farmacokinetische gegevens beschikbaar bij pediatrische niertransplantatiepatiënten (zie rubriek 5.2).
Bejaarden
De aanbevolen dosis bij oudere patiënten is tweemaal daags 720 mg.
Patiënten met nierinsufficiëntie
Er is geen dosisaanpassing nodig bij patiënten met een vertraagde nierfunctie na transplantatie (zie rubriek 5.2).
Patiënten met een ernstige nierfunctiestoornis (glomerulaire filtratiesnelheid
Patiënten met leverinsufficiëntie
Er zijn geen dosisaanpassingen nodig bij patiënten met niertransplantatie en ernstige leverinsufficiëntie.
Behandeling tijdens afleveringen van afstoting
Er werden geen veranderingen in de farmacokinetiek van mycofenolzuur (MPA) waargenomen tijdens episodes van afstoting na niertransplantatie; daarom is een dosisaanpassing of stopzetting van de behandeling met Myfortic niet nodig.
04.3 Contra-indicaties
Myfortic mag niet worden gebruikt bij patiënten met overgevoeligheid voor natriummycofenolaat, mycofenolzuur, mycofenolaatmofetil of voor één van de hulpstoffen (zie rubriek 6.1).
Myfortic mag niet worden gebruikt bij vrouwen die borstvoeding geven en bij vrouwen in de vruchtbare leeftijd die geen zeer effectieve anticonceptiemethoden gebruiken en mag niet worden gestart zonder een zwangerschapstest om onbedoeld gebruik van het geneesmiddel tijdens de zwangerschap uit te sluiten (zie rubriek 4.6). ).
Myfortic mag niet tijdens de zwangerschap worden gebruikt, tenzij er een geschikte alternatieve behandeling is om orgaanafstoting te voorkomen (zie rubriek 4.6).
Myfortic mag niet worden toegediend aan vrouwen die borstvoeding geven (zie rubriek 4.6).
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Patiënten die een immunosuppressieve therapie krijgen op basis van een combinatie van geneesmiddelen, waaronder Myfortic, hebben een verhoogd risico op het ontwikkelen van lymfomen of andere maligniteiten, vooral van de huid (zie rubriek 4.8). Het risico lijkt verband te houden met de intensiteit en duur van de immunosuppressieve behandeling en niet met het gebruik van een specifiek product. Als algemene waarschuwing: om het risico op huidkanker te verkleinen, is het noodzakelijk om de blootstelling aan zonlicht en UV-stralen te beperken door het gebruik van beschermende kleding en zonnecrèmes met een hoge beschermingsfactor.
Patiënten die met Myfortic worden behandeld, moeten worden geïnstrueerd over de noodzaak om tekenen van infectie of de aanwezigheid van onverwachte blauwe plekken, bloedingen of andere manifestaties van beenmergdepressie onmiddellijk te melden.
Patiënten die worden behandeld met immunosuppressiva, waaronder Myfortic, hebben een verhoogd risico op opportunistische infecties (bacteriële, schimmel-, virale en protozoaire), fatale infecties en sepsis (zie rubriek 4.8). Opportunistische infecties omvatten BK-virus-geassocieerde nefropathie en JC-virus-geassocieerde progressieve multifocale leuko-encefalopathie (PML). Deze infecties zijn vaak het gevolg van een hoge totale immunosuppressieve belasting en kunnen leiden tot ernstige of fatale aandoeningen waarmee artsen rekening moeten houden bij het stellen van een differentiële diagnose bij immunosuppressieve patiënten met een verslechterende nierfunctie of neurologische symptomen.
Er zijn meldingen geweest van hypogammaglobulinemie in verband met terugkerende infecties bij patiënten die Myfortic kregen in combinatie met andere immunosuppressiva. In sommige van deze gevallen resulteerde het overschakelen van MPA-derivaten op een alternatief immunosuppressivum in serum-IgG-spiegels die weer normaal werden. Bij met Myfortic behandelde patiënten die terugkerende infecties ontwikkelen, moeten serumimmunoglobulinen worden gemeten. In gevallen van aanhoudende klinisch relevante hypogammaglobulinemie moet geschikte klinische interventie worden overwogen, rekening houdend met de krachtige cytostatische effecten van mycofenolzuur op T- en B-lymfocyten.
Er zijn meldingen geweest van bronchiëctasie bij patiënten die werden behandeld met Myfortic in combinatie met andere immunosuppressiva. In sommige van deze gevallen leidde het overschakelen van MPA-derivaten naar een ander immunosuppressivum tot verbetering van de ademhalingssymptomen. Het risico op bronchiëctasie kan verband houden met hypogammaglobulinemie of een direct effect op de longen Er zijn ook geïsoleerde meldingen van interstitiële longziekte (zie rubriek 4.8) Het wordt aanbevolen dat patiënten die aanhoudende ademhalingssymptomen ontwikkelen, zoals hoesten en dyspneu, worden onderzocht op enig bewijs van onderliggende interstitiële longziekte.
Reactivering van hepatitis B (HBV) of hepatitis C (HCV) is gemeld bij patiënten die werden behandeld met immunosuppressiva, waaronder derivaten van myfortic mycofenolzuur (MPA) en mycofenolaatmofetil (MMF). Het wordt aanbevolen om geïnfecteerde patiënten te controleren op klinische en laboratoriumsymptomen van actieve HBV- of HCV-infectie.
Er zijn gevallen van pure rode-cel-aplasie (PRCA) gemeld bij patiënten die werden behandeld met mycofenolzuurderivaten (waaronder mycofenolaatmofetil en natriummycofenolaat) in combinatie met andere immunosuppressiva.mycofenol-geïnduceerde PRCA is niet bekend. PRCA kan verdwijnen door dosisverlaging of stopzetting van de behandeling Wijzigingen in de behandeling met Myfortic bij transplantatiepatiënten mogen alleen worden aangebracht onder passend klinisch toezicht om het risico op afstoting tot een minimum te beperken (zie rubriek 4.8).
Patiënten die met Myfortic worden behandeld, moeten worden gecontroleerd op bloedaandoeningen (bijv. neutropenie of anemie - zie rubriek 4.8), die verband kunnen houden met mycofenolzuur zelf, gelijktijdige medicatie, virale infecties of combinaties van deze oorzaken. Patiënten die met Myfortic worden behandeld, moeten daarom elke week een volledig bloedbeeld krijgen tijdens de eerste maand van de behandeling, tweemaal per maand tijdens de tweede en derde maand en daarna maandelijks tot het einde van het eerste jaar van de behandeling. In het geval van bloedaandoeningen (bijv. neutropenie met absoluut aantal neutrofielen 3/mcl of anemie) kan het aangewezen zijn om de behandeling met Myfortic te staken of stop te zetten.
Patiënten moeten erop worden gewezen dat vaccinaties mogelijk minder effectief zijn tijdens de behandeling met mycofenolzuur, terwijl vaccinaties met levende verzwakte vaccins moeten worden vermeden (zie rubriek 4.5). Influenzavaccinatie kan echter nuttig zijn; artsen dienen de nationale richtlijnen voor griepvaccinatie te raadplegen.
Aangezien mycofenolzuurderivaten in verband zijn gebracht met een verhoogde incidentie van bijwerkingen die het spijsverteringsstelsel beïnvloeden, waaronder zeldzame gevallen van gastro-intestinale ulcera, bloedingen en perforaties, moet Myfortic met voorzichtigheid worden toegediend aan patiënten met een ernstige ziekte in de actieve fase van het spijsverteringsstelsel. .
Het wordt aanbevolen Myfortic niet gelijktijdig met azathioprine toe te dienen, aangezien gelijktijdige toediening van deze geneesmiddelen niet is onderzocht.
Vanwege het verschillende farmacokinetische profiel mogen mycofenolzuur (als natriumzout) en mycofenolaatmofetil niet willekeurig worden uitgewisseld of vervangen Myfortic werd toegediend in combinatie met ciclosporine en corticosteroïden. beperkt. De werkzaamheid en veiligheid van Myfortic in combinatie met andere immunosuppressiva (bijv. tacrolimus) zijn niet onderzocht.
Myfortic bevat lactose. Patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, Lapp-lactasedeficiëntie of glucose-galactosemalabsorptie dienen dit geneesmiddel niet te gebruiken.
Toediening van Myfortic samen met geneesmiddelen die interfereren met de enterohepatische circulatie, zoals colestyramine en actieve kool, kan leiden tot systemische blootstelling aan MPA beneden de therapeutische niveaus en bijgevolg tot verminderde werkzaamheid.
Myfortic is een remmer van het enzym inosinemonofosfaatdehydrogenase (IMPDH).Om deze reden mag het niet worden gebruikt bij patiënten met zeldzame erfelijke aandoeningen waarbij sprake is van een tekort aan het enzym hypoxanthine-guanine-fosforibosyl-transferase (HGPRT), zoals het syndroom van Lesch-Nyhan en Kelley-Seegmiller-syndroom.
Behandeling met Myfortic mag niet worden gestart voordat een negatieve zwangerschapstest is verkregen.Effectieve anticonceptie dient te worden gebruikt voorafgaand aan de start van de behandeling met Myfortic, tijdens de behandeling en gedurende zes weken na het stoppen (zie paragraaf 4.6).
Teratogene effecten
Mycofenolaat is een krachtig humaan teratogeen Spontane abortus (percentage 45-49%) en aangeboren misvormingen (geschat percentage 23-27%) zijn gemeld na blootstelling aan mycofenolaatmofetil tijdens de zwangerschap. Daarom is Myfortic gecontra-indiceerd tijdens de zwangerschap, tenzij er adequate alternatieve behandelingen zijn om transplantaatafstoting te voorkomen. Vrouwelijke en mannelijke patiënten die zwanger kunnen worden, moeten voor, tijdens en na de behandeling met Myfortic worden geïnformeerd over de risico's en de aanbevelingen in rubriek 4.6 volgen (bijv. anticonceptiemethoden, zwangerschapstesten). Artsen dienen ervoor te zorgen dat zowel vrouwen als mannen die met mycofenolaat worden behandeld, het risico op schade aan de foetus en de noodzaak van effectieve anticonceptie begrijpen en onmiddellijk medische hulp inroepen als er een kans op zwangerschap bestaat.
Anticonceptie (zie rubriek 4.6)
Vanwege het genotoxische en teratogene potentieel van Myfortic moeten vrouwen in de vruchtbare leeftijd twee betrouwbare anticonceptiemethoden tegelijkertijd gebruiken voordat de behandeling met Myfortic wordt gestart, tijdens de behandeling en gedurende zes weken na het stoppen van de behandeling, tenzij de gekozen methode wordt gebruikt. onthouding.
Seksueel actieve mannen wordt aangeraden condooms te gebruiken tijdens de behandeling en gedurende ten minste 90 dagen na het stoppen van de behandeling. Het gebruik van condooms is geldig voor zowel vruchtbare mannen als voor degenen die een vasectomie hebben ondergaan, aangezien de risico's die gepaard gaan met de passage van zaadvocht ook gelden voor mannen die een vasectomie hebben ondergaan.Bovendien wordt het gebruik van vrouwelijke partners van patiënten die met Myfortic worden behandeld aanbevolen zeer effectieve anticonceptie tijdens de behandeling en gedurende in totaal 90 dagen na de laatste dosis Myfortic.
Educatief materiaal
Om patiënten te helpen blootstelling van de foetus aan mycofenolaat te vermijden en om aanvullende belangrijke veiligheidsinformatie te verstrekken, zal de houder van de vergunning voor het in de handel brengen voorlichtingsmateriaal aan beroepsbeoefenaren in de gezondheidszorg verstrekken. advies over de noodzaak van een zwangerschapstest. De arts dient volledige patiënteninformatie te verstrekken over teratogene risico's en methoden voor zwangerschapspreventie aan vrouwen in de vruchtbare leeftijd en, waar relevant, aan mannelijke patiënten.
Aanvullende voorzorgsmaatregelen
Patiënten mogen geen bloed doneren tijdens de behandeling of gedurende ten minste 6 weken na het stoppen met mycofenolaat Mannen mogen geen sperma doneren tijdens de behandeling of gedurende ten minste 90 dagen na het stoppen met mycofenolaat.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
De volgende interacties tussen mycofenolzuur en andere geneesmiddelen zijn gemeld:
Aciclovir en ganciclovir
De mogelijkheid van myelosuppressie bij patiënten die Myfortic in combinatie met aciclovir of ganciclovir gebruiken, is niet onderzocht. Als Myfortic wordt gegeven in combinatie met aciclovir/ganciclovir, kan een verhoging van de MPAG- (mycofenolzuurglucuronaatmetaboliet) en aciclovir/ganciclovir-spiegels worden verwacht, mogelijk als gevolg van concurrentie voor het tubulaire secretiemechanisme.Dit is onwaarschijnlijk.dat veranderingen in de farmacokinetiek van MPAG optreden. van klinische relevantie bij patiënten met een adequate nierfunctie. In aanwezigheid van nierinsufficiëntie is er een kans op verhoogde plasmaconcentraties van MPAG en aciclovir/ganciclovir; in dit geval moeten patiënten nauwlettend worden gecontroleerd en moeten de dosisaanbevelingen voor aciclovir/ganciclovir worden gevolgd.
Gastroprotectors:
Antacida op basis van magnesium en aluminium:
Een afname van de mycofenolzuur AUC en Cmax van respectievelijk ongeveer 37% en 25% werd waargenomen wanneer Myfortic werd toegediend in combinatie met een enkele dosis magnesium-aluminium antacidum. Magnesium-aluminiumantacida kunnen af en toe worden gebruikt om occasionele dyspepsie te behandelen.Het dagelijkse chronische gebruik van magnesium-aluminiumantacida in combinatie met Myfortic wordt echter niet aanbevolen vanwege hun potentieel om de blootstelling aan mycofenolzuur te verminderen en bijgevolg de werkzaamheid ervan te verminderen.
Protonpompremmers:
Bij gezonde vrijwilligers werden geen veranderingen in de farmacokinetiek van MPA waargenomen na gelijktijdige toediening van Myfortic en pantoprazol in een dosis van 40 mg tweemaal daags in de voorgaande vier dagen. Er zijn geen gegevens beschikbaar over andere protonpompremmers die in hoge doses worden gegeven.
Orale anticonceptiva
Interactiestudies uitgevoerd met MMF (mycofenolaatmofetil) en orale anticonceptiva hebben geen interacties tussen deze geneesmiddelen aangetoond. Op basis van het metabole profiel van MPA zijn er geen interacties te verwachten tussen Myfortic en orale anticonceptiva.
Colestyramine en geneesmiddelen die zich binden aan galzuren
Er moet aandacht worden besteed aan het gelijktijdig gebruik van geneesmiddelen of therapieën die zich aan galzuren kunnen binden, zoals galzuurbindende harsen of orale actieve kool, vanwege hun potentieel om de blootstelling aan MPA te verminderen en daardoor de "werkzaamheid van Myfortic te verminderen.
Cyclosporine
De farmacokinetiek van ciclosporine die werd onderzocht bij stabiele niertransplantatiepatiënten werd niet beïnvloed door de steady-state toediening van Myfortic-dosering. Aan de andere kant is het bekend dat de gelijktijdige toediening van ciclosporine met mycofenolaatmofetil de blootstelling aan mycofenolzuur vermindert.Daarom wordt aangenomen dat ciclosporine, toegediend met Myfortic, op vergelijkbare wijze de bloedconcentraties van mycofenolzuur kan verlagen (ongeveer 20%, gebaseerd op gegevens verkregen met mycofenolaatmofetil), maar de precieze omvang van deze afname is niet bekend aangezien deze interactie niet is onderzocht. Aangezien echter alle werkzaamheidsonderzoeken zijn uitgevoerd in combinatie met ciclosporine, verandert deze interactie de dosering niet Als de behandeling met ciclosporine wordt onderbroken of stopgezet, moet de dosering van Myfortic opnieuw worden geëvalueerd volgens het nieuwe immunosuppressieve regime.
Tacrolimus
In een cross-over klinisch onderzoek naar calcineurine bij stabiele niertransplantatiepatiënten, werd de steady-state farmacokinetiek van Myfortic gemeten tijdens behandeling met zowel Neoral als tacrolimus. De gemiddelde waarde van de AUC van mycofenolzuur was groter dan 19% (90% BI: - 3, +47), terwijl de gemiddelde waarde van de AUC van de metaboliet MPAG (fenolglucuronide van mycofenolzuur) ongeveer 30% (90% CI: 16, 42) tijdens behandeling met tacrolimus vergeleken met Neoral. Bovendien was de variabiliteit in mycofenolzuur AUC die werd waargenomen bij proefpersonen verdubbeld na overschakeling van behandeling met Neoral naar tacrolimus. Artsen dienen rekening te houden met zowel de toename van de AUC van mycofenolzuur als de variabiliteit, en de dosisaanpassing van Myfortic moet worden bepaald door de klinische situatie. Wanneer u van plan bent om van de ene calcineurineremmer naar de andere over te schakelen, dient nauwlettend klinisch toezicht te worden gehouden.
Levende verzwakte vaccins
Levende vaccins mogen niet worden gegeven aan patiënten met een verminderde immuunrespons. De antilichaamrespons op vaccins van andere typen kan verminderd zijn.
04.6 Zwangerschap en borstvoeding
Vrouwen in de vruchtbare leeftijd
Start de behandeling met Myfortic niet voordat u een zwangerschapstest heeft gedaan, deze moet negatief zijn.
Anticonceptie bij mannen en vrouwen
Myfortic is gecontra-indiceerd bij vrouwen in de vruchtbare leeftijd die geen zeer effectieve anticonceptiemethoden gebruiken.
Vanwege het genotoxische en teratogene potentieel van Myfortic moeten vrouwen in de vruchtbare leeftijd twee betrouwbare anticonceptiemethoden tegelijkertijd gebruiken voordat de behandeling met Myfortic wordt gestart, tijdens de behandeling met Myfortic en gedurende zes weken na de laatste dosis Myfortic, tenzij de gekozen anticonceptiemethode is geen onthouding.
Seksueel actieve mannen wordt aangeraden condooms te gebruiken tijdens de behandeling met Myfortic en gedurende ten minste 90 dagen na het stoppen van de behandeling. vasectomie ondergaan. Daarnaast wordt aanbevolen dat vrouwelijke begeleiders van mannelijke patiënten die met Myfortic worden behandeld, zeer effectieve anticonceptie gebruiken tijdens de behandeling en gedurende in totaal 90 dagen na de laatste dosis Myfortic.
Zwangerschap
Myfortic is gecontra-indiceerd tijdens de zwangerschap, tenzij er geen geschikte alternatieve behandeling is om transplantaatafstoting te voorkomen. De behandeling mag niet worden gestart zonder de uitslag van een zwangerschapstest om onbedoeld gebruik van het geneesmiddel tijdens de zwangerschap uit te sluiten.
Vrouwelijke en mannelijke patiënten die zwanger kunnen worden, moeten aan het begin van de behandeling worden geïnformeerd over het verhoogde risico op zwangerschapsverlies en aangeboren afwijkingen en moeten worden geadviseerd over zwangerschapspreventie en -planning.
Voordat de behandeling met Myfortic wordt gestart, moeten vrouwen in de vruchtbare leeftijd een zwangerschapstest ondergaan om onbedoelde blootstelling van het embryo aan mycofenolaat uit te sluiten. Twee serum- of urinezwangerschapstesten met een gevoeligheid van minimaal 25 mIU/ml worden aanbevolen; de tweede test (indien van toepassing) moet 8 tot 10 dagen na de eerste en onmiddellijk voor aanvang van de behandeling met Myfortic worden gedaan. Zwangerschapstesten moeten zo nodig klinisch worden herhaald (bijv. na elke melding van onderbreking van de anticonceptie). De resultaten van alle zwangerschapstesten moeten met de patiënte worden besproken. Patiënten moeten worden geadviseerd om onmiddellijk hun arts te raadplegen als ze zwanger zijn.
Mycofenolaat is een krachtig teratogeen bij de mens, met een verhoogd risico op miskramen en aangeboren afwijkingen bij blootstelling aan het geneesmiddel tijdens de zwangerschap:
• Spontane abortussen zijn gemeld bij 45-49% van de zwangere vrouwen die werden blootgesteld aan mycofenolaatmofetil, vergeleken met een gerapporteerd percentage van 12 tot 33% bij patiënten met een orgaantransplantatie die werden behandeld met andere immunosuppressiva dan mycofenolaatmofetil.
• Volgens de literatuur kwamen misvormingen voor bij 23-27% van de levendgeborenen van moeders die tijdens de zwangerschap aan mycofenolaatmofetil waren blootgesteld (vergeleken met 2-3% van de levendgeborenen in de totale populatie en ongeveer 4-5% van de levendgeborenen van proefpersonen die solide orgaantransplantatie behandeld met andere immunosuppressiva dan mycofenolaatmofetil).
Aangeboren misvormingen, waaronder meldingen van meerdere misvormingen, zijn post-marketing waargenomen bij kinderen van patiënten die tijdens de zwangerschap aan mycofenolaatmofetil in combinatie met andere immunosuppressiva zijn blootgesteld. De volgende misvormingen werden het vaakst gemeld:
• Oorafwijkingen (bijv. misvormd of afwezig uitwendig/middenoor), atresie van de uitwendige gehoorgang;
• Aangeboren hartafwijkingen zoals atriale en ventriculaire septumdefecten;
• Gezichtsmisvormingen zoals hazenlip, gespleten gehemelte, micrognathie en hypertelorisme van de oogkassen;
• Oogafwijkingen (bijv. coloboom);
• vingerafwijkingen (bijv. polydactylie, syndactylie);
• Tracheo-oesofageale malformaties (bijv. oesofageale atresie);
• Zenuwstelselmisvormingen zoals spina bifida;
• Nierafwijkingen.
Daarnaast zijn er geïsoleerde meldingen van de volgende misvormingen:
• Microftalmie;
• Congenitale cyste van de choroïde plexus;
• Agenese van het septum pellucidum;
• Agenese van de reukzenuw.
Uit dieronderzoek is reproductietoxiciteit gebleken (zie rubriek 5.3).
Voedertijd
Bij ratten wordt mycofenolzuur uitgescheiden in de moedermelk Het is niet bekend of Myfortic ook wordt uitgescheiden in de moedermelk, maar aangezien mycofenolzuur mogelijk ernstige bijwerkingen kan veroorzaken bij de zuigeling, is toediening van Myfortic gecontra-indiceerd tijdens borstvoeding. 4.3).
Vruchtbaarheid
Er zijn geen specifieke studies uitgevoerd met Myfortic bij mensen om de effecten op de vruchtbaarheid te evalueren In een mannelijke en vrouwelijke vruchtbaarheidsstudie bij ratten werden geen effecten waargenomen tot doses van respectievelijk 40 mg/kg en 20 mg/kg (zie rubriek 5.3). ).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er is geen onderzoek gedaan naar de effecten op de rijvaardigheid en op het vermogen om machines te bedienen. Het werkingsmechanisme, het farmacodynamische profiel en de gemelde bijwerkingen maken een dergelijk effect onwaarschijnlijk.
04.8 Bijwerkingen
De volgende bijwerkingen verwijzen naar bijwerkingen die zijn waargenomen in klinische onderzoeken.
neoplasmata
Patiënten die een immunosuppressieve therapie krijgen bestaande uit een combinatie van geneesmiddelen, waaronder mycofenolzuur, hebben een verhoogd risico op het ontwikkelen van lymfomen of andere maligniteiten, vooral van de huid (zie rubriek 4.4). de-novo (0,9%) en bij 2 onderhoudspatiënten (1,3%) die Myfortic gedurende één jaar gebruikten. Bij 0,9% van de patiënten de-novo en bij 1,8% van de onderhoudspatiënten die Myfortic gedurende één jaar gebruikten, werd niet-melanoom huidkanker gezien; andere vormen van kanker werden gezien bij 0,5% van de patiënten de-novo en bij 0,6% van de patiënten in de onderhoudsfase.
Opportunistische infecties
Het risico op opportunistische infecties neemt toe bij alle transplantatiepatiënten, het risico neemt toe met de totale immunosuppressieve belasting (zie rubriek 4.4). De meest voorkomende opportunistische infecties bij niertransplantatiepatiënten de-novo behandeld met Myfortic in combinatie met andere immunosuppressiva waargenomen in gecontroleerde klinische onderzoeken van niertransplantatiepatiënten gevolgd gedurende 1 jaar waren CMV (cytomegalovirus), candidiasis en herpes simplex CMV-infecties (serologie, viremie of vastgestelde ziekte) waren 21,6% bij niertransplantatiepatiënten de-novo en 1,9% bij patiënten met onderhoudstherapie.
Bejaarden
Over het algemeen kunnen oudere patiënten een verhoogd risico lopen op het ontwikkelen van bijwerkingen als gevolg van immunosuppressie.
Andere bijwerkingen van geneesmiddelen
De volgende tabel 1 geeft een overzicht van de bijwerkingen die mogelijk of waarschijnlijk verband houden met Myfortic, gemeld in gecontroleerde klinische onderzoeken bij niertransplantatiepatiënten waarbij Myfortic werd toegediend in combinatie met ciclosporine-micro-emulsie en corticosteroïden in een dosis van 1440 mg/dag gedurende 12 maanden. tabel is samengesteld volgens de MedDRA-classificatie per orgaansysteemklasse:
Bijwerkingen zijn gerangschikt in de volgende categorieën:
Zeer vaak (≥ 1/10)
Vaak (> 1/100,
Soms (> 1/1000,
Zeldzaam (> 1 / 10.000,
Erg zeldzaam (
tafel 1
gebeurtenis gemeld bij slechts één patiënt (van de 372).
Opmerking: Niertransplantatiepatiënten werden gedurende maximaal één jaar met Myfortic 1440 mg/dag behandeld. Het bijwerkingenprofiel is vergelijkbaar bij patiënten de-novo en bij de populatie die onderhoudstherapie krijgt na transplantatie, zelfs als de incidentie van bijwerkingen lager lijkt te zijn in de laatste populatie.
Uit postmarketingervaring zijn huiduitslag en agranulocytose als bijwerkingen geïdentificeerd.
De volgende aanvullende bijwerkingen zijn als klasse-effect toegeschreven aan mycofenolzuurderivaten:
Infecties en parasitaire aandoeningen:
Ernstige, levensbedreigende infecties, waaronder meningitis, infectieuze endocarditis, tuberculose en atypische mycobacteriële infecties. Gevallen van BK-virus-geassocieerde nefropathie evenals gevallen van JC-virus-geassocieerde progressieve multifocale leuko-encefalopathie (PML) zijn gemeld bij patiënten die werden behandeld met immunosuppressiva, waaronder Myfortic (zie rubriek 4.4).
Aandoeningen van het bloed en het lymfestelsel:
Neutropenie, pancytopenie.
Er zijn gevallen van pure red cell aplasia (PRCA) gemeld bij patiënten die werden behandeld met mycofenolzuurderivaten (zie rubriek 4.4).
Aandoeningen van het immuunsysteem
Hypogammaglobulinemie is gemeld bij patiënten die Myfortic kregen in combinatie met andere immunosuppressiva.
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen:
Er zijn geïsoleerde meldingen van interstitiële longziekte bij patiënten die werden behandeld met Myfortic in combinatie met andere immunosuppressiva. Er zijn ook meldingen geweest van bronchiëctasie in combinatie met andere immunosuppressiva.
Geïsoleerde gevallen van morfologische afwijkingen van neutrofielen, waaronder de verworven Pelger-Huet-afwijking, zijn
zijn gemeld bij patiënten die werden behandeld met mycofenolzuurderivaten.Deze veranderingen gaan echter niet gepaard met een verminderde functionaliteit van neutrofielen.Deze veranderingen kunnen wijzen op een fenomeen van linker shift rijping van neutrofielen, wat verkeerd kan worden geïnterpreteerd als een teken van infectie bij patiënten met immunosuppressie, zoals patiënten die met Myfortic worden behandeld.
Maagdarmstelselaandoeningen:
Colitis, CMV gastritis, darmperforatie, maagzweer, ulcus duodeni.
Zwangerschap, kraambed en perinatale aandoeningen:
Gevallen van spontane abortus zijn gemeld bij patiënten die voornamelijk in het eerste trimester aan mycofenolaat werden blootgesteld (zie rubriek 4.6).
Aangeboren aandoeningen:
Aangeboren misvormingen zijn postmarketing waargenomen bij kinderen van patiënten die werden blootgesteld aan mycofenolaat in combinatie met andere immunosuppressiva (zie rubriek 4.6).
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres www. agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Er zijn meldingen geweest van opzettelijke of onopzettelijke overdoses met Myfortic, hoewel niet alle patiënten gerelateerde bijwerkingen hebben ervaren.
In die gevallen van overdosering waarvoor bijwerkingen zijn gemeld, vallen de voorvallen binnen de reikwijdte van het bekende veiligheidsprofiel van de klasse (voornamelijk bloeddyscrasieën, sepsis ...) (zie rubrieken 4.4 en 4.8).
Dialyse kan worden gebruikt om de inactieve metaboliet van mycofenolzuur (MPAG) te verwijderen, maar zal naar verwachting geen klinisch significante hoeveelheden van het actieve deel van mycofenolzuur verwijderen.Dit is voornamelijk te wijten aan de hoge eiwitbinding van mycofenolzuur plasma, gelijk aan Geneesmiddelen die galzuur sekwestreren, zoals colestyramine, kunnen, door de enterohepatische circulatie van mycofenolzuur te verstoren, de systemische blootstelling aan mycofenolzuur verminderen.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: immunosuppressiva, ATC-code: L04 AA06.
Mycofenolzuur is een krachtige, selectieve, niet-competitieve en reversibele remmer van het enzym inosinemonofosfaatdehydrogenase; het remt de syntheseroute de-novo van het guanosine-nucleotide, zonder te worden opgenomen in het DNA. De proliferatie van T- en B-lymfocyten is kritisch afhankelijk van synthese de-novo van purines, in tegenstelling tot andere celtypen die een alternatief mechanisme kunnen gebruiken, is de cytostatische werking van mycofenolzuur op lymfocyten krachtiger dan die op andere celtypen.
05.2 Farmacokinetische eigenschappen
Absorptie
Na orale toediening wordt natriummycofenolaat in hoge mate geabsorbeerd. In overeenstemming met de kenmerken van de gastro-enterische formulering, is de Tmax (tijd om de maximale concentratie te bereiken) van mycofenolzuur ongeveer 1,5 - 2 uur Ongeveer 10% van de farmacokinetische profielen bepaald na ochtendtoediening vertoonde soms een verlenging van de waarde van Tmax van enkele uren, zonder enige geschatte invloed op de blootstelling aan mycofenolzuur in de 24 uur.
Bij stabiele niertransplantatiepatiënten die een immunosuppressieve behandeling met ciclosporine kregen, was de gastro-intestinale absorptie van mycofenolzuur 93% en de absolute biologische beschikbaarheid 72%. De farmacokinetiek van Myfortic was dosisproportioneel en lineair over het geteste dosisbereik (180 - 2160 mg). Toediening van een enkelvoudige dosis Myfortic (720 mg) met vetrijke voedingsmiddelen (50 g vet, 1000 calorieën) veranderde de AUC (de meest belangrijke farmacokinetische parameter gecorreleerd met werkzaamheid) van mycofenolzuur vergeleken met toediening van het geneesmiddel in nuchtere toestand; de Cmax van mycofenolzuur was echter met 33% verlaagd.Bovendien werd bij veel patiënten een gemiddelde verlenging van de tlag- en Tmax-waarden van 3-5 uur waargenomen, met Tmax-waarden> 15 uur. "Voedselinname op de farmacokinetiek van Myfortic kan daarom leiden tot overlapping in absorptie van het ene dosisbereik naar het andere." Dit effect vertoonde echter geen klinische betekenis.
Verdeling
Het steady-state distributievolume van mycofenolzuur is 50 liter Zowel mycofenolzuur als zijn glucuronaatmetaboliet zijn sterk gebonden aan plasma-eiwitten (respectievelijk 97% en 82%). De concentratie van vrij mycofenolzuur kan toenemen onder omstandigheden waarbij de eiwitbindingsplaatsen afnemen (uremie, leverinsufficiëntie, hypoalbuminemie, gelijktijdig gebruik van geneesmiddelen met een hoge plasma-eiwitbinding). Dit kan leiden tot een verhoogd risico op aan mycofenolzuur gerelateerde bijwerkingen.
Biotransformatie
Mycofenolzuur wordt gemetaboliseerd door het enzym glucuronyltransferase tot fenolglucuronide van mycofenolzuur (MPAG).MPAG is de belangrijkste metaboliet van mycofenolzuur en heeft geen biologische activiteit. Bij stabiele patiënten die ciclosporine krijgen na niertransplantatie, wordt ongeveer 28% van de oraal toegediende dosis Myfortic gemetaboliseerd tot MPAG door presystemisch metabolisme. De halfwaardetijd van deze metaboliet, die langer is dan die van mycofenolzuur, is ongeveer 16 uur en de klaring is 0,45 l/u.
Eliminatie
De halfwaardetijd van mycofenolzuur is ongeveer 12 uur en de klaring is 8,6 l/uur. Hoewel er verwaarloosbare hoeveelheden mycofenolzuur in de urine aanwezig zijn (gal is beschikbaar voor deconjugatie door de darmflora en het mycofenolzuur dat door dit proces wordt gevormd, kan dan opnieuw worden geabsorbeerd. Ongeveer 6-8 uur na toediening van Myfortic is het in feite mogelijk een tweede piekconcentratie van mycofenolzuur waargenomen, gecorreleerd met de reabsorptie van het gedeconjugeerde mycofenolzuur./ml) werd 's ochtends waargenomen bij ongeveer 2% van de patiënten die met Myfortic werden behandeld. ), wat indicatief is voor de totale blootstelling, vertoonde minder variabiliteit dan die van de minimale plasmaconcentratie (Cdal).
Farmacokinetiek bij niertransplantatiepatiënten die een immunosuppressieve behandeling met ciclosporine krijgen:
De volgende tabel 2 toont de gemiddelde farmacokinetische parameters van mycofenolzuur na toediening van Myfortic In de periode direct na de transplantatie waren de gemiddelde waarden van AUC en Cmax van mycofenolzuur ongeveer de helft van de waarden bepaald zes maanden na transplantatie .
Tabel 2 Farmacokinetische parameters (gemiddelde en SD) gerelateerd aan MPA na orale toediening van Myfortic bij niertransplantatiepatiënten die ciclosporine-immunosuppressie krijgen
Nierfunctiestoornis
De farmacokinetiek van mycofenolzuur lijkt onveranderd te zijn vanaf het stadium van normale nierfunctie tot nierfalen.Daarentegen neemt de blootstelling aan de MPAG-metaboliet toe met een verminderde nierfunctie en is deze ongeveer 8 keer hoger in aanwezigheid van anurie.De klaring van het mycofenolzuur en die van de MPAG-metaboliet werden niet beïnvloed door "hemodialyse. L" Vrij mycofenolzuur kan ook een significante toename van aandoeningen van nierinsufficiëntie, waarschijnlijk als gevolg van een afname van de binding van mycofenolzuur aan plasma-eiwitten in aanwezigheid van hoge bloedconcentraties van ureum.
leverfunctiestoornis
De hepatische glucuronidering van mycofenolzuur wordt nauwelijks veranderd door de aanwezigheid van pathologieën van het leverparenchym, zoals waargenomen bij vrijwilligers met alcoholische cirrose. De effecten van een leverziekte op het geneesmiddelmetabolisme hangen waarschijnlijk af van het type pathologie: een leverziekte met overheersende schade aan galwegen, zoals primaire biliaire cirrose, kunnen een ander effect hebben op het metabolisme van mycofenolzuur.
Pediatrische en adolescente populatie
Er zijn beperkte gegevens beschikbaar over het gebruik van Myfortic bij kinderen en adolescenten.Tabel 2 hierboven beschrijft de gemiddelde (SD) farmacokinetische parameters van mycofenolzuur bij stabiele pediatrische niertransplantatiepatiënten in de leeftijd van 5-16 jaar die een behandeling ondergaan, immunosuppressief met ciclosporine. De gemiddelde AUC van mycofenolzuur bij een dosis van 450 mg/m2 was vergelijkbaar met de AUC bepaald bij volwassenen die werden behandeld met Myfortic in een dosis van 720 mg De gemiddelde schijnbare klaring van mycofenolzuur was ongeveer 6,7 l/u/m2.
Type
Er zijn geen klinisch significante sekseverschillen in de farmacokinetiek van Myfortic.
Bejaarden
De farmacokinetiek bij ouderen is niet geëvalueerd in geschikte onderzoeken Blootstelling aan mycofenolzuur lijkt niet significant te variëren met de leeftijd.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
In toxiciteitsstudies met herhaalde dosering die zijn uitgevoerd met natriummycofenolaat bij ratten en muizen, waren de belangrijkste aangetaste organen het hematopoëtische en lymfoïde systeem. Aplastische, regeneratieve anemie werd geïdentificeerd als een uitdrukking van dosisbeperkende toxiciteit bij knaagdieren die waren blootgesteld aan MPA. Evaluatie van myelogrammen onthulde een duidelijke afname van erytroïde cellen (normoblasten en polychromatische erytroblasten), een dosisafhankelijke "milthypertrofie en een toename van extra- medullaire hematopoëse Deze effecten traden op bij systemische blootstellingsniveaus gelijk aan of lager dan die waargenomen in de klinische setting bij niertransplantatiepatiënten met de aanbevolen Myfortic-dosis van 1,44 g/dag.
Gastro-intestinale effecten werden waargenomen bij honden bij systemische blootstellingsniveaus gelijk aan of lager dan die waargenomen in de klinische setting met de aanbevolen dosis.
Het toxicologische profiel van mycofenolzuur (als natriumzout) dat resulteert uit preklinische onderzoeken komt daarom overeen met de bijwerkingen die zijn waargenomen in klinische onderzoeken, die veiligheidsgegevens opleveren die relevanter zijn voor de patiëntenpopulatie (zie rubriek 4.8).
In drie genotoxiciteitstesten (in vitro muis lymfoom test, Chinese hamster V79 cel micronuclei en in vivo muis beenmerg micronuclei test), "biedde mycofenolzuur het potentieel om chromosomale aberraties te veroorzaken. E" Het is mogelijk dat de waargenomen effecten gerelateerd zijn aan de farmacodynamisch werkingsmechanisme, dwz de remming van de nucleotidesynthese in gevoelige cellen. In andere in vitro tests om de inductie van genetische mutaties te evalueren, vertoonde mycofenolzuur geen genotoxische activiteit.
Mycofenolzuur (als natriumzout) was niet carcinogeen bij ratten en muizen In carcinogeniteitsstudies bij dieren komt de maximale geteste dosis overeen met een systemische blootstelling (AUC of Cmax) van ongeveer 0,6-5 keer die gezien bij niertransplantatiepatiënten die werden behandeld met de aanbevolen dosis Myfortic van 1,44 g / dag.
Mycofenolzuur (als natriumzout), zelfs in doses die algemene toxiciteit en embryotoxiciteit hebben veroorzaakt, heeft geen effect op de vruchtbaarheid van mannelijke en vrouwelijke ratten.
In een onderzoek naar teratogenese bij ratten met mycofenolzuur (als natriumzout) in een dosis van 1 mg/kg werden misvormingen bij het nageslacht waargenomen, waaronder anoftalmie, exencefalie en navelbreuk. De systemische blootstelling die overeenkomt met deze dosis is gelijk aan 0,05 maal de klinische blootstelling met de Myfortic-dosis van 1,44 mg/dag (zie rubriek 4.6).
In een pre- en postnataal ontwikkelingsonderzoek bij ratten veroorzaakte mycofenolzuur (als natriumzout) ontwikkelingsachterstanden (abnormale pupilreflex bij de vrouw en scheiding van de voorhuid bij de man) bij de maximale dosis van 3 mg/kg die ook induceert misvormingen. .
In een essay in vitro van fototoxiciteit 3T3 NRU mycofenolzuur (als natriumzout) vertoonde fototoxisch potentieel.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Kern:
Maïszetmeel
Povidon (K30)
Crospovidon
Watervrije lactose
Watervrij colloïdaal silica
Magnesium stearaat
Bekleding:
Hypromellose ftalaat
Titaandioxide (E171)
Geel ijzeroxide (E172)
Rood ijzeroxide (E172)
06.2 Incompatibiliteit
Niet relevant
06.3 Geldigheidsduur
30 maanden
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 30°C.
Bewaren in de oorspronkelijke verpakking om het geneesmiddel tegen vocht te beschermen.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
De tabletten zijn verpakt in blisterverpakkingen van polyamide/aluminium/PVC/aluminium, elk met 10 tabletten, in hoeveelheden per doos van 50, 100, 120 en 250 tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Om de enterische coating intact te houden, mogen Myfortic-tabletten niet worden fijngemaakt (zie rubriek 4.2).
Mycofenolzuur heeft teratogene effecten (zie rubriek 4.6).
Als Myfortic-tabletten fijngemaakt moeten worden, vermijd dan inademing of direct contact van het poeder met de huid of slijmvliezen.
Ongebruikte medicijnen en afval afkomstig van dit medicijn moeten worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Farma S.p.A.
Largo Umberto Boccioni, 1
Origgio (VA)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
360 mg maagsapresistente tabletten - 50 tabletten AIC n.: 036511069
360 mg maagsapresistente tabletten - 100 tabletten AIC n.: 036511071
360 mg maagsapresistente tabletten - 120 tabletten AIC n.: 036511083
360 mg maagsapresistente tabletten - 250 tabletten AIC n.: 036511095
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste vergunning: 13 juni 2005
Verlengingsdatum: 10 oktober 2008
10.0 DATUM VAN HERZIENING VAN DE TEKST
07/2016