De elementaire analyse van eiwitten geeft de volgende gemiddelde waarden: 55% koolstof, 7% waterstof en 16% stikstof; het is duidelijk dat eiwitten van elkaar verschillen, maar hun gemiddelde elementaire samenstelling verschilt weinig van de hierboven aangegeven waarden .
Grondwettelijk zijn eiwitten macromoleculen gevormd uit natuurlijke α-aminozuren; de aminozuren komen samen door de amidebinding die tot stand wordt gebracht door de reactie tussen een aminogroep van een a-aminozuur en de carboxyl van een ander a-aminozuur.
Deze binding (-CO-NH-) wordt ook wel een peptidebinding genoemd omdat het peptiden (aminozuren in combinatie) bindt:
de verkregen is een dipeptide omdat het bestaat uit twee aminozuren. Omdat een dipeptide aan het ene uiteinde een vrije aminogroep (NH2) en aan het andere uiteinde een carboxyl bevat (COOH), kan het reageren met een of meer aminozuren en de keten verlengen, zowel van rechts als van links, met dezelfde reactie hierboven gezien.
De opeenvolging van reacties (die overigens niet zo eenvoudig zijn) kan oneindig doorgaan: totdat er een polymeer is genaamd polypeptide of eiwit. Het onderscheid tussen peptiden en eiwitten is gekoppeld aan het molecuulgewicht: meestal spreken we bij molecuulgewichten hoger dan 10.000 van eiwitten.
Het aan elkaar binden van aminozuren om zelfs kleine eiwitten te verkrijgen is een moeilijke taak, hoewel recentelijk een automatische methode is ontwikkeld om eiwitten uit aminozuren te produceren die uitstekende resultaten geeft.
Het eenvoudigste eiwit bestaat dus uit 2 aminozuren: volgens internationale afspraak gaat de geordende nummering van aminozuren in een eiwitstructuur uit van het aminozuur met de vrije a-aminogroep.
coderen voor dit eiwit) die niet te verwaarlozen chemische problemen ondervindt.
Het was mogelijk om de volgorde van aminozuren te bepalen door Edman-degradatie: het eiwit wordt gereageerd met fenylisothiocyanaat (FITC), aanvankelijk valt het α-aminostikstofdoublet het fenylisothiocyanaat aan en vormt het thiocarbamylderivaat; vervolgens cycliseert het verkregen product en geeft het fenylthiohydantoïnederivaat dat fluorescerend is.
Edman heeft een machine bedacht, een sequencer genaamd, die automatisch de parameters (tijd, reagentia, pH, enz.) voor degradatie aanpast en de primaire structuur van eiwitten levert (hiervoor ontving hij de Nobelprijs).
De primaire structuur is niet voldoende om de eigenschappen van de eiwitmoleculen volledig te interpreteren; er wordt aangenomen dat deze eigenschappen op een essentiële manier afhangen van de ruimtelijke configuratie die de eiwitmoleculen geneigd zijn aan te nemen, waarbij ze op verschillende manieren vouwen: dat wil zeggen, uitgaande van wat is gedefinieerd als secundaire structuur van eiwitten.
De secundaire structuur van eiwitten flikkert, dat wil zeggen, het heeft de neiging om te desintegreren door verhitting; dan denatureren de eiwitten zichzelf en verliezen veel van hun karakteristieke eigenschappen. Naast verhitting boven 70°C kan denaturatie ook veroorzaakt worden door bestraling of door inwerking van reactanten (van bijvoorbeeld sterke zuren).
De denaturatie van eiwitten door het thermische effect wordt bijvoorbeeld waargenomen door het eiwit te verhitten: men ziet dat het zijn gelatineuze uiterlijk verliest en verandert in een onoplosbare witte substantie. De denaturatie van eiwitten leidt echter tot de vernietiging van hun secundaire structuur, maar laat hun primaire structuur ongewijzigd (de aaneenschakeling van de verschillende aminozuren).
Eiwitten nemen de tertiaire structuur aan wanneer hun keten, hoewel nog steeds flexibel ondanks de buiging van de secundaire structuur, zodanig vouwt dat een verwrongen driedimensionale opstelling in de vorm van een vast lichaam ontstaat. Verantwoordelijk voor de tertiaire structuur zijn vooral de disulfidebindingen die kunnen worden vastgesteld tussen de cysteïne-SH verspreid over het molecuul.
De quaternaire structuur daarentegen behoort alleen tot eiwitten die worden gevormd door twee of meer subeenheden. Hemoglobine, bijvoorbeeld, is samengesteld uit twee paar eiwitten (dat wil zeggen in alle vier de eiwitketens) die zich op de hoekpunten van een tetraëder bevinden, zodat een bolvormige structuur ontstaat; de vier eiwitketens worden bij elkaar gehouden door ionische en niet-covalente bindingen.
Een ander voorbeeld van een quaternaire structuur is die van insuline, dat lijkt te bestaan uit maar liefst zes eiwitsubeenheden die in paren zijn gerangschikt op de hoekpunten van een driehoek met in het midden twee zinkatomen.
vezelige eiwitten
Het zijn eiwitten met een bepaalde stijfheid en met een veel langere as dan de andere; het vezelachtige eiwit dat in grotere hoeveelheden in de natuur aanwezig is, is collageen (of collageen).
Een vezelig eiwit kan verschillende secundaire structuren aannemen: α-helix, β-sheet en, in het geval van collageen, triple helix; α-helix is de meest stabiele structuur, gevolgd door de β-sheet, terwijl de minst stabiele van de drie de triple helix is.
Rechtsaf als, in navolging van het hoofdskelet (gericht van onder naar boven), een beweging wordt uitgevoerd die lijkt op het indraaien van een rechtse schroef; terwijl de helix uit is linkerhand als de beweging analoog is aan het aandraaien van een linksdraaiende schroef In de rechter α-helices staan de -R substituenten van de aminozuren loodrecht op de hoofdas van het eiwit en zijn naar buiten gericht, terwijl in de linker- hand a-helices de -R substituenten naar binnen gericht. Rechtshandige a-helices zijn stabieler dan linkshandige omdat er tussen de vati -R c "minder interactie en minder sterische hinder is. Alle a-helices die in eiwitten worden gevonden, zijn rechtshandig.
De structuur van de α-helix wordt gestabiliseerd door de waterstofbruggen (waterstofbruggen) die gevormd worden tussen de carboxylgroep (-C=O) van elk aminozuur en de aminogroep (-NH) die later in de lineaire volgorde.
Een voorbeeld van een eiwit met een a-helixstructuur is haarkeratine.
Door de -helixstructuur te verlengen, wordt de overgang van α-helix naar β-sheet uitgevoerd; ook de warmte of de mechanische spanning laten toe om van de α-helix naar de β-plaatstructuur te gaan.
Gewoonlijk liggen in een eiwit de β-sheetstructuren dicht bij elkaar omdat waterstofbruggen tussen de ketens tussen delen van het eiwit zelf tot stand kunnen worden gebracht.
In vezelachtige eiwitten is het grootste deel van de eiwitstructuur georganiseerd in een -helix of β-sheet.
bolvormige eiwitten
Ze hebben een bijna bolvormige ruimtelijke structuur (vanwege de talrijke richtingsveranderingen van de polypeptideketen); sommige delen van het zijn kunnen worden herleid tot een α-helix- of β-sheetstructuur en andere delen zijn daarentegen niet toe te schrijven aan deze vormen: de rangschikking is niet willekeurig, maar georganiseerd en repetitief.
De tot nu toe genoemde eiwitten zijn stoffen met een volledig homogene samenstelling: dat wil zeggen zuivere sequenties van gecombineerde aminozuren; dergelijke eiwitten worden gezegd eenvoudig; er zijn eiwitten die bestaan uit een eiwitdeel en een niet-eiwitdeel (prostaatgroep) genaamd eiwitten conjugeren.
, in de nagels, in het hoornvlies en in de ooglens, tussen de interstitiële ruimten van sommige organen (bijv. lever) enzovoort.
Zijn structuur geeft het bijzondere mechanische mogelijkheden; het heeft een grote mechanische sterkte geassocieerd met een hoge elasticiteit (bijv. in pezen) of hoge stijfheid (bijv. in botten), afhankelijk van de functie die het moet vervullen.
Een van de merkwaardigste eigenschappen van collageen is zijn constitutieve eenvoud: het bestaat uit ongeveer 30% proline en ongeveer 30% glycine; de andere 18 aminozuren hoeven alleen de resterende 40% van de eiwitstructuur te delen. De aminozuurvolgorde van collageen is opmerkelijk regelmatig: voor elke drie resten is de derde glycine.
Proline is een cyclisch aminozuur waarbij de R-groep zich bindt aan de α-aminostikstof en dit geeft het een zekere stijfheid.
De uiteindelijke structuur is een zich herhalende keten in de vorm van een "helix; binnen de collageenketen zijn waterstofbruggen afwezig. Collageen is een "linkerhandhelix met een spoed (lengte die overeenkomt met één draaiing van de helix) groter dan de" α-helix; de collageenhelix is zo los dat drie eiwitketens zich om elkaar kunnen wikkelen en een " enkel touw: triple helix structuur.
De drievoudige helix van collageen is echter minder stabiel dan zowel de α-helix als de β-sheetstructuur.
Laten we nu eens kijken naar het mechanisme waarmee collageen wordt geproduceerd; denk bijvoorbeeld aan de breuk van een bloedvat: deze breuk gaat gepaard met een groot aantal signalen met als doel het vat te sluiten en zo het stolsel te vormen.
Coagulatie vereist ten minste dertig gespecialiseerde enzymen. Na het stolsel is het noodzakelijk om door te gaan met het herstel van het weefsel; cellen dicht bij de wond produceren ook collageen. Hiervoor wordt eerst de expressie van een gen geïnduceerd, d.w.z. organismen die uitgaande van de informatie van een gen het eiwit kunnen produceren (de genetische informatie wordt getranscribeerd op het mRNA dat de kern verlaat en de ribosomen bereikt in de cytoplasma waar de genetische informatie wordt vertaald in eiwit. Vervolgens wordt het collageen gesynthetiseerd in de ribosomen (het ziet eruit als een linker helix samengesteld uit ongeveer 1200 aminozuren en met een molecuulgewicht van ongeveer 150.000 d) en hoopt zich vervolgens op in de lumen waar het wordt een substraat voor enzymen die in staat zijn om post-translationele modificaties uit te voeren (modificaties van de taal vertaald door "mRNA); in collageen bestaan deze modificaties in de hydroxylering van sommige zijketens, vooral proline en lysine.
Het falen van de enzymen die tot deze veranderingen leiden, veroorzaakt scheurbuik: het is een ziekte die aanvankelijk leidt tot het breken van bloedvaten, het breken van de tanden, wat kan worden gevolgd door interintestinale bloedingen en overlijden; het kan worden veroorzaakt door het continue gebruik van houdbaar voedsel.
Vervolgens treden door de werking van andere enzymen andere modificaties op die bestaan in de glycosidatie van de hydroxylgroepen van proline en lysine (een suiker bindt zich aan de zuurstof van de OH); deze enzymen worden gevonden in andere gebieden dan het lumen, daarom migreert het eiwit, terwijl het modificaties ondergaat, in het endoplasmatisch reticulum om te eindigen in zakjes (vesicles) die zichzelf sluiten en loskomen van het reticulum: daarin zit het geglycosideerde pro - collageenmonomeer; dit laatste bereikt het Golgi-apparaat waar bepaalde enzymen de cysteïne herkennen die aanwezig is in het carboxy-terminale deel van het geglycosideerde pro-collageen en ervoor zorgen dat de verschillende ketens elkaar naderen en disulfidebruggen vormen: op deze manier drie ketens van geglycosideerd pro-collageen wordt met elkaar verbonden verkregen en dit is het startpunt waarvan de drie ketens, elkaar doordringend, dan, spontaan, aanleiding geven tot de drievoudige helix. De drie ketens van geglycosideerd pro-collageen die met elkaar verbonden zijn, bereiken dan een blaasje dat, verstikkend in zichzelf, maakt zich los van het Golgi-apparaat en transporteert de drie ketens naar de periferie van de cel waar, door de fus ion met het plasmamembraan, wordt de trimeter uit de cel verdreven.
In de extracellulaire ruimte bevinden zich bepaalde enzymen, de pro-collageen peptidasen, die uit de soort die uit de cel is verdreven, drie fragmenten (één voor elke helix) van 300 aminozuren l "één, van het terminale carboxydeel en drie verwijderen. fragmenten (één voor elke helix) van ongeveer 100 aminozuren elk, van het aminoterminale deel: er blijft een drievoudige helix bestaande uit ongeveer 800 aminozuren per helix bekend als tropocollageen.
Tropocollageen heeft het uiterlijk van een vrij stijve staaf; de verschillende trimeren associëren met covalente bindingen om grotere structuren te geven: de microfibrillen. In de microfibrillen zijn de verschillende trimeren verspringend gerangschikt; veel microfibrillen vormen tropocollageenbundels.
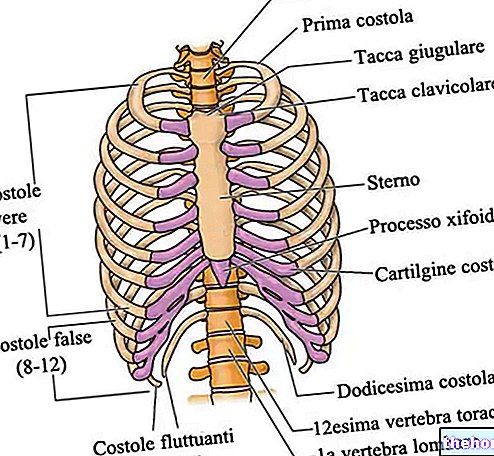
In de botten, tussen de collageenvezels, bevinden zich interstitiële ruimten waarin sulfaten en fosfaten van calcium en magnesium zijn afgezet: deze zouten bedekken ook alle vezels; hierdoor worden de botten stijf.
In pezen zijn interstitiële ruimten minder rijk aan kristallen dan in botten, terwijl kleinere eiwitten aanwezig zijn dan in tropocollageen: dit geeft pezen elasticiteit.
Osteoporose is een ziekte die wordt veroorzaakt door een tekort aan calcium en magnesium, waardoor het onmogelijk is om zouten in de interstitiële gebieden van de tropocollageenvezels te fixeren.






.jpg)