Actieve ingrediënten: Bortezomib
VELCADE 3,5 mg poeder voor oplossing voor injectie.
Indicaties Waarom wordt Velcade gebruikt? Waar is het voor?
VELCADE bevat de werkzame stof bortezomib, een zogenaamde 'proteasoomremmer'. Proteasomen spelen een belangrijke rol bij het regelen van de celfunctie en groei. Door hun functie te verstoren, kan bortezomib kankercellen doden.
VELCADE wordt gebruikt voor de behandeling van multipel myeloom (een type maligniteit van het beenmerg) bij patiënten ouder dan 18 jaar:
- alleen of samen met de geneesmiddelen gepegyleerd liposomaal doxorubicine of dexamethason, voor patiënten met een verergerende (progressieve) ziekte na ten minste één eerdere behandeling of bij wie bloedstamceltransplantatie is mislukt of niet haalbaar is
- in combinatie met de geneesmiddelen melfalan en prednison voor patiënten met een niet eerder behandelde ziekte die geen hoge doses chemotherapie kunnen krijgen bij bloedstamceltransplantatie.
- in combinatie met dexamethason of dexamethason samen met thalidomide, voor patiënten met een niet eerder behandelde ziekte en vóór het ontvangen van een hoge dosis chemotherapie met bloedstamceltransplantatie (inductiebehandeling)
VELCADE wordt gebruikt voor de behandeling van mantelcellymfoom (een soort maligniteit die de lymfeklieren aantast) bij patiënten van 18 jaar of ouder. In dit geval wordt VELCADE gebruikt in combinatie met de geneesmiddelen rituximab, cyclofosfamide, doxorubicine en prednison, voor patiënten met een niet eerder behandelde ziekte en voor wie bloedstamceltransplantatie niet haalbaar is.
Contra-indicaties Wanneer Velcade niet mag worden gebruikt
Gebruik VELCADE niet
- als u allergisch bent voor bortezomib, boor of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6)
- als u ernstige long- of hartproblemen heeft.
Voorzorgsmaatregelen bij gebruik Wat u moet weten voordat u Velcade inneemt
Vertel het uw arts als u:
- laag aantal rode bloedcellen of witte bloedcellen
- bloedingsproblemen en/of laag aantal bloedplaatjes
- diarree, constipatie, misselijkheid of braken
- eerdere ervaringen met flauwvallen, duizeligheid of een licht gevoel in het hoofd
- nierproblemen
- matige tot ernstige leverproblemen
- eerdere klachten zoals gevoelloosheid, tintelingen of pijn in handen of voeten (neuropathie)
- hart- of bloeddrukstoornis
- kortademigheid of hoesten
- stuiptrekkingen
- gordelroos (ook rond de ogen of verspreid naar de rest van het lichaam)
- symptomen van tumorlysissyndroom zoals bijvoorbeeld spierkrampen, spierzwakte, verwardheid, verstoord zicht of verlies van gezichtsvermogen en kortademigheid
- geheugenverlies, moeite met denken, moeite met lopen of verlies van gezichtsvermogen.Dit kunnen tekenen zijn van een ernstige herseninfectie en uw arts kan verdere tests en controles voorschrijven.
Voor en tijdens de behandeling met VELCADE moet u regelmatig bloedonderzoek ondergaan om uw bloedcelwaarden constant te controleren.
Als u mantelcellymfoom heeft en rituximab samen met VELCADE krijgt, moet u uw arts vertellen:
- als u denkt dat u hepatitis heeft of dit in het verleden heeft gehad. In sommige gevallen kunnen patiënten die hepatitis B hebben gehad een nieuwe hepatitis-aanval krijgen, die fataal kan zijn.Als u in het verleden een hepatitis B-infectie heeft gehad, zal uw arts u nauwlettend moeten controleren op tekenen en symptomen van actieve hepatitis B.
Lees de bijsluiters van alle geneesmiddelen die u in combinatie met VELCADE gebruikt voor informatie over deze geneesmiddelen voordat u met de behandeling met VELCADE begint.
Wanneer VELCADE gelijktijdig wordt toegediend met thalidomide, let dan vooral op het advies over zwangerschapstesten en het zwangerschapspreventieprogramma (zie "Zwangerschap en borstvoeding" in deze rubriek).
Kinderen en adolescenten
VELCADE mag niet worden gebruikt bij kinderen en jongeren tot 18 jaar omdat niet bekend is hoe het geneesmiddel bij deze mensen werkt.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Velcade veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Vertel het uw arts in het bijzonder als u geneesmiddelen gebruikt die een van de volgende werkzame stoffen bevatten:
- ketoconazol, gebruikt voor de behandeling van schimmelinfecties
- ritonavir, gebruikt voor de behandeling van hiv-infectie - rifampicine, een antibioticum dat wordt gebruikt om bacteriële infecties te behandelen
- carbamazepine, fenytoïne of fenobarbital, gebruikt voor de behandeling van epilepsie
- Sint-janskruid (Hypericum perforatum), gebruikt voor de behandeling van depressie of andere aandoeningen
- orale antidiabetica.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
U mag VELCADE niet gebruiken als u zwanger bent, tenzij strikt noodzakelijk.
Mannen en vrouwen die met VELCADE worden behandeld, dienen effectieve anticonceptie te gebruiken tijdens en tot 3 maanden na de behandeling. Als u ondanks deze voorzorgsmaatregelen toch zwanger wordt, neem dan onmiddellijk contact op met uw arts.
U mag geen borstvoeding geven tijdens het gebruik van VELCADE Bespreek met uw arts wat de beste tijd is om de borstvoeding te hervatten na het einde van de therapie.
Het geneesmiddel thalidomide veroorzaakt geboorteafwijkingen en foetale sterfte. Wanneer VELCADE gelijktijdig wordt toegediend met thalidomide, moet u het zwangerschapspreventieprogramma van thalidomide volgen (zie de bijsluiter van thalidomide).
Rijvaardigheid en het gebruik van machines
VELCADE kan vermoeidheid, duizeligheid, flauwvallen of wazig zien veroorzaken. Bestuur geen auto en bedien geen machines als u een van deze symptomen ervaart. Let ook goed op als deze effecten niet optreden.
Dosis, wijze en tijdstip van toediening Hoe Velcade te gebruiken: Dosering
Uw arts zal de dosis VELCADE berekenen in verhouding tot uw lengte en gewicht. De standaard startdosering van VELCADE is 1,3 mg/m2 lichaamsoppervlak tweemaal per week. Uw arts kan de dosis en het totale aantal behandelingskuren wijzigen, afhankelijk van uw reactie op de behandeling, het optreden van bepaalde bijwerkingen en uw algemene gezondheidstoestand (bijv. leverproblemen).
Progressief multipel myeloom
Als VELCADE alleen wordt gegeven, krijgt u 4 doses VELCADE intraveneus of subcutaan op dag 1, 4, 8 en 11. Dit wordt gevolgd door een "off"-periode van 10 dagen zonder behandeling.
Deze periode van 21 dagen (3 weken) komt overeen met één behandelingskuur.
U kunt maximaal 8 cycli (24 weken) krijgen. U kunt VELCADE ook krijgen samen met de geneesmiddelen met gepegyleerd liposomaal doxorubicine of dexamethason.
Als VELCADE samen met gepegyleerd liposomaal doxorubicine wordt gegeven, krijgt u een 21-daagse kuur met intraveneuze of subcutane VELCADE en 30 mg/m2 gepegyleerde liposomale doxorubicine op dag 4 van de 21-daagse behandelingscyclus van VELCADE als een infuus. intraveneus na injectie van VELCADE.
U kunt maximaal 8 cycli krijgen (24 weken behandeling).
Wanneer VELCADE gelijktijdig wordt toegediend met dexamethason, krijgt u een behandeling van 21 dagen met intraveneuze of subcutane VELCADE en orale dexamethason in een dosis van 20 mg op dag 1, 2, 4, 5, 8, 9, 11 en 12, van de 21-daagse behandelingskuur met VELCADE.
U kunt maximaal 8 cycli krijgen (24 weken behandeling).
Eerder onbehandeld multipel myeloom
Als u nog nooit eerder bent behandeld voor multipel myeloom en u komt niet in aanmerking voor bloedstamceltransplantatie, dan krijgt u VELCADE samen met twee andere geneesmiddelen: melfalan en prednison.
In dit geval is de duur van een kuur 42 dagen (6 weken). Hij krijgt 9 cycli (54 weken).
- In cycli 1-4 wordt VELCADE tweemaal per week toegediend op dag 1, 4, 8, 11, 22, 25, 29 en 32.
- In cycli 5-9 wordt VELCADE eenmaal per week toegediend op dag 1, 8, 22 en 29.
Melfalan (9 mg/m2) en prednison (60 mg/m2) worden via de mond toegediend op dag 1, 2, 3 en 4 van de eerste week van elke cyclus.
Als u nog nooit eerder bent behandeld voor multipel myeloom en u in aanmerking komt voor bloedstamceltransplantatie, krijgt u VELCADE intraveneus of subcutaan toegediend samen met de geneesmiddelen: dexamethason, of dexamethason en thalidomide, als inductiebehandeling.
Wanneer VELCADE gelijktijdig wordt toegediend met dexamethason, krijgt u een 21-daagse behandelingskuur met intraveneuze of subcutane VELCADE en orale dexamethason 40 mg op dag 1, 2, 3, 4, 8, 9, 10 en 11 van de cyclus. -dag VELCADE-behandeling.
U krijgt 4 cycli (12 weken behandeling).
Wanneer VELCADE samen met thalidomide en dexamethason wordt gegeven, duurt de behandelingskuur 28 dagen (4 weken).
Dexamethason 40 mg wordt oraal toegediend op dag 1, 2, 3, 4, 8, 9, 10 en 11 van de 28-daagse behandelingscyclus met VELCADE en thalidomide wordt oraal toegediend in een dosis van 50 mg per dag tot dag 14 van de eerste cyclus en, indien getolereerd, wordt de dosis thalidomide verhoogd tot 100 mg op dag 15-28 en kan daarna worden verhoogd tot 200 mg per dag vanaf de tweede cyclus. U kunt maximaal 6 cycli krijgen (24 weken behandeling).
Eerder onbehandeld mantelcellymfoom
Als u in het verleden nog nooit een specifieke behandeling voor mantelcellymfoom heeft gekregen, krijgt u VELCADE intraveneus of subcutaan toegediend samen met de geneesmiddelen rituximab, cyclofosfamide, doxorubicine en prednison.
VELCADE wordt intraveneus of subcutaan toegediend op dag 1, 4, 8 en 11, gevolgd door een rustperiode zonder behandeling. De duur van de behandelingskuur is 21 dagen (3 weken).
U kunt maximaal 8 kuren krijgen (24 weken).
De volgende geneesmiddelen worden toegediend op dag 1 van elke 21-daagse behandelingscyclus van VELCADE als een intraveneuze infusie: rituximab 375 mg/m2, cyclofosfamide 750 mg/m2 en doxorubicine 50 mg/m2.
Prednison wordt oraal toegediend in een dosis van 100 mg/m2 op dag 1, 2, 3, 4 en 5 van de VELCADE-behandelingscyclus.
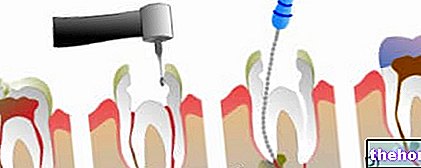
Hoe VELCADE wordt gegeven
Dit geneesmiddel is voor intraveneus of subcutaan gebruik. VELCADE zal worden toegediend door een beroepsbeoefenaar in de gezondheidszorg met ervaring in het gebruik van cytotoxische geneesmiddelen. Het poeder van VELCADE moet vóór toediening worden opgelost. Dit zal worden gedaan door een beroepsbeoefenaar in de gezondheidszorg. De resulterende oplossing wordt dan snel in een ader of subcutaan geïnjecteerd. L " injectie in een ader is snel, gedurende een periode van 3 tot 5 seconden. De subcutane injectie kan zowel in de dij als in de buik worden toegediend.
Overdosering Wat te doen als u te veel Velcade heeft ingenomen
Aangezien dit geneesmiddel door uw arts of verpleegkundige wordt gegeven, is het onwaarschijnlijk dat u meer zult innemen dan u zou mogen.In het onwaarschijnlijke geval van een overdosis zal uw arts controleren op bijwerkingen.
Bijwerkingen Wat zijn de bijwerkingen van Velcade
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken. Sommige van deze effecten kunnen ernstig zijn.
Als u VELCADE krijgt voor multipel myeloom of mantelcellymfoom, vertel het dan onmiddellijk aan uw arts als u een van de volgende symptomen opmerkt:
- spierkrampen, spierzwakte
- verwardheid, verstoord zicht of verlies van gezichtsvermogen, blindheid, toevallen, hoofdpijn
- kortademigheid, zwelling van de voeten of veranderingen in de hartslag, hoge bloeddruk, vermoeidheid, flauwvallen
- hoesten en moeite met ademhalen of beklemd gevoel op de borst.
Behandeling met VELCADE kan zeer vaak een daling van het aantal rode en witte bloedcellen en bloedplaatjes veroorzaken. Daarom moet u voor en tijdens de behandeling met VELCADE regelmatig bloedonderzoeken ondergaan om uw bloedceltellingen regelmatig te controleren. U kunt een vermindering van het aantal ervaren:
- bloedplaatjes, waardoor u vatbaarder bent voor blauwe plekken of bloedingen zonder duidelijk letsel (bijvoorbeeld bloeding in de darmen, maag, mond en tandvlees of bloeding in de hersenen of lever)
- rode bloedcellen, die bloedarmoede kunnen veroorzaken, met symptomen zoals vermoeidheid en bleekheid
- witte bloedcellen, waardoor u vatbaarder kunt worden voor infecties of griepachtige symptomen.
Als u VELCADE krijgt voor de behandeling van multipel myeloom, staan de bijwerkingen die kunnen optreden hieronder vermeld.
Zeer vaak voorkomende bijwerkingen (kunnen voorkomen bij meer dan 1 op de 10 mensen)
- Overgevoeligheid, gevoelloosheid, tintelend of branderig gevoel van de huid, of pijn in de handen of voeten als gevolg van zenuwbeschadiging.
- Vermindering van het aantal rode en/of witte bloedcellen (zie hierboven).
- Koorts.
- Gevoel van misselijkheid of braken, verlies van eetlust.
- Obstipatie met of zonder overtollig gas (kan ernstig zijn).
- Diarree: als dit gebeurt, is het belangrijk dat u veel meer water drinkt dan normaal. Uw arts kan medicijnen voorschrijven om diarree onder controle te houden.
- Vermoeidheid (vermoeidheid), gevoel van zwakte.
- Spierpijn, botpijn.
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 mensen)
- Lage bloeddruk, plotselinge bloeddrukdaling bij het staan, wat kan leiden tot flauwvallen.
- Verhoogde bloeddruk.
- Verminderde functie van de nieren.
- Hoofdpijn.
- Algemeen onwel voelen, pijn, duizeligheid, licht gevoel in het hoofd, gevoel van zwakte of bewustzijnsverlies.
- Rillingen.
- Infecties, waaronder longontsteking, luchtweginfecties, bronchitis, schimmelinfectie, hoesten met slijm, griepachtige ziekte.
- Herpes zoster-infectie (plaatselijk, ook rond de ogen, of verspreid over het lichaam).
- Pijn op de borst of moeite met ademhalen tijdens lichamelijke activiteit.
- Verschillende soorten huiduitslag (uitslag).
- Jeukende huid, bultjes op de huid of een droge huid.
- Roodheid van het gezicht of kleine breuken in de haarvaten.
- Roodheid van de huid.
- uitdroging.
- Brandend maagzuur, opgeblazen gevoel, boeren, gas, maagpijn, darm- of maagbloeding.
- Verandering van de leverfunctie.
- Irritatie van de mond of lippen, droge mond, mondzweren of keelpijn.
- Gewichtsverlies, verlies van smaak.
- Spierkrampen, spierspasmen, spierzwakte, pijn in armen en benen.
- Wazig zicht.
- Infectie van de buitenste laag van de ogen en het binnenoppervlak van de oogleden (conjunctivitis).
- Neusbloeding (bloeding).
- Slaapstoornissen of -problemen, zweten, angst, stemmingswisselingen, depressieve stemming, rusteloosheid of opwinding, veranderingen in mentale toestand, desoriëntatie.
- Zwelling van het lichaam, inclusief zwelling rond de ogen en andere delen van het lichaam.
Soms voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 100 mensen)
- Hartfalen, hartaanval, pijn op de borst, ongemak op de borst, verhoogde of verlaagde hartslag.
- Nierfalen.
- Ontsteking van een ader, bloedstolsels in de aderen en longen.
- Bloedstollingsproblemen.
- Storing in de bloedsomloop.
- Ontsteking van het membraan rond het hart of de aanwezigheid van vocht rond het hart.
- Infecties waaronder urineweginfecties, griep, herpesvirusinfecties, oorinfecties en cellulitis.
- Bloed in de ontlasting of bloeding van de slijmvliezen, bijv. mond, vagina.
- Cerebrovasculaire aandoeningen.
- Verlamming, stuiptrekkingen, vallen, bewegingsstoornissen, abnormale, veranderde of verminderde gevoeligheid (voelen, horen, proeven, ruiken), aandachtsstoornis, tremor, krampen.
- Artritis, inclusief ontsteking van de gewrichten van de vingers, tenen en kaak.
- Aandoeningen die de longen aantasten, waardoor uw lichaam onvoldoende zuurstof krijgt. Enkele hiervan zijn ademhalingsmoeilijkheden, kortademigheid, piepende ademhaling, zelfs zonder lichamelijke activiteit, moeite met oppervlakkig ademhalen of moeten stoppen, piepende ademhaling.
- Hik, spraakstoornissen.
- Verhoogde of verminderde urineproductie (nierbeschadiging), pijnlijk urineren of bloed/eiwit in de urine, vochtretentie.
- Veranderde niveaus van bewustzijn, verwarring, geheugenverlies of geheugenverlies.
- Overgevoeligheid.
- Gehoorverlies, doofheid of oorsuizen, ongemak in het oor.
- Hormonale veranderingen die de reabsorptie van zouten en water kunnen beïnvloeden.
- Hyperactiviteit van de schildklier.
- Onvermogen om voldoende insuline te produceren of weerstand tegen normale insulinespiegels.
- Pijnlijke of ontstoken ogen, extreem natte ogen, oogpijn, droge ogen, ooginfecties, oogafscheiding, gezichtsstoornissen, oogbloedingen.
- Vergrote lymfeklieren.
- Gewrichts- of spierstijfheid, zwaar gevoel, pijn in de lies.
- Haaruitval of abnormale haartextuur.
- Allergische reacties.
- Roodheid of pijn op de injectieplaats.
- Pijn in de mond.
- Infectie of ontsteking van de mond, zweren in de mond, slokdarm, maag en darmen, soms gepaard gaande met pijn of bloedingen, verminderde darmmotiliteit (inclusief darmblokkade), buikpijn of slokdarmklachten, moeite met slikken, bloed overgeven.
- Huidinfecties.
- Bacteriële en virale infecties.
- Tand infectie.
- Ontsteking van de alvleesklier, obstructie van de galwegen.
- Pijn in de geslachtsdelen, erectieproblemen.
- Gewichtstoename.
- Dorst voelen.
- Hepatitis.
- Aandoeningen op de injectieplaats of katheterplaats.
- Huidreacties of aandoeningen (die ernstig en levensbedreigend kunnen zijn), huidzweren.
- Kneuzingen, vallen en verwondingen.
- Ontsteking of bloeding van bloedvaten die zich kan manifesteren als kleine rode of paarse stippen (meestal op de benen) die kunnen lijken op grote blauwe plekken op de huid of het weefsel.
- Goedaardige cysten.
- Een ernstige en omkeerbare aandoening van de hersenen die toevallen, hoge bloeddruk, hoofdpijn, vermoeidheid, verwardheid, blindheid of andere problemen met het gezichtsvermogen omvat.
Zelden voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 1.000 mensen)
- Hartproblemen, waaronder een hartaanval, angina.
- Spoelt.
- Verkleuring van de aderen.
- Ontsteking van de spinale zenuw.
- Oorproblemen, bloeding uit het oor.
- Verminderde activiteit van de schildklier.
- Budd-Chiari-syndroom (klinische symptomen worden veroorzaakt door verstopping van de leveraders).
- Verandering of abnormale darmfunctie.
- Hersenbloeding (bloeding).
- Gele verkleuring van de ogen en huid (geelzucht).
- Symptomen van ernstige allergische reactie (anafylactische shock) zijn onder meer ademhalingsmoeilijkheden, pijn op de borst of beklemd gevoel op de borst en/of zich duizelig/zwak voelen, ernstige jeukende huid of bulten op de huid, zwelling van het gezicht, de lippen, tong en/of keel die moeite met slikken, collaps.
- Borstaandoeningen.
- Vaginale afscheiding.
- Zwelling van de geslachtsdelen.
- Onvermogen om alcoholgebruik te tolereren.
- Verspilling of verlies van lichaamsmassa.
- Verhoogde eetlust.
- fistels.
- Gezamenlijke effusie.
- Cyste op het membraan dat de gewrichten bedekt (synoviale cysten).
- Breuken.
- Afbraak van spiervezels leidt tot andere complicaties.
- Vergrote lever, leverbloeding.
- Nierkanker.
- Huidaandoening vergelijkbaar met psoriasis.
- Huidkanker.
- Bleekheid van de huid.
- Toename van bloedplaatjes of plasmacellen (een type witte bloedcel) in het bloed.
- Abnormale reactie op bloedtransfusie.
- Gedeeltelijk of totaal verlies van het gezichtsvermogen.
- Verminderd libido.
- Verlies van speeksel.
- Oog uitsteeksel.
- Fotofobie (overmatige gevoeligheid van het oog voor licht).
- Snel ademhalen.
- Pijn in het rectum.
- Galstenen.
- Hernia.
- Blessures.
- Broze of zwakke nagels.
- Abnormale eiwitafzetting in vitale organen.
- coma.
- Darmzweren.
- Schade aan meerdere organen.
- Dood.
Als u VELCADE samen met andere geneesmiddelen krijgt voor de behandeling van mantelcellymfoom, worden de bijwerkingen die kunnen optreden hieronder vermeld.
Zeer vaak voorkomende bijwerkingen (kunnen voorkomen bij meer dan 1 op de 10 mensen)
- Longontsteking.
- Verlies van eetlust.
- Overgevoeligheid, gevoelloosheid, tintelend of branderig gevoel van de huid, of pijn in de handen of voeten als gevolg van zenuwbeschadiging.
- Misselijkheid en braken.
- Diarree.
- Mondzweren.
- Intestinale constipatie.
- Spierpijn, botpijn.
- Haaruitval of abnormale haartextuur.
- Vermoeidheid, gevoel van zwakte.
- Koorts.
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 mensen)
- Herpes zoster-infectie (plaatselijk, ook rond de ogen of verspreid over het lichaam).
- Herpesvirusinfectie.
- Bacteriële en virale infecties.
- Luchtweginfecties, bronchitis, hoesten met slijm, griepachtige ziekte.
- Schimmelinfecties.
- Overgevoeligheid (allergische reactie).
- Onvermogen om voldoende insuline te produceren of weerstand tegen normale insulinespiegels.
- Water afstotend.
- Moeilijkheden of problemen met slapen.
- Verlies van bewustzijn.
- Veranderde bewustzijnsniveaus, verwarde toestand.
- Duizelig voelen.
- Verhoogde hartslag, hoge bloeddruk, zweten.
- Visuele stoornissen, wazig zien.
- Hartfalen, hartaanval, pijn op de borst, ongemak op de borst, verhoogde of verlaagde hartslag.
- Hoge of lage bloeddruk.
- Plotselinge bloeddrukdaling bij het staan, wat kan leiden tot flauwvallen.
- Kortademigheid tijdens lichamelijke activiteit.
- Hoest.
- Hik.
- Oorsuizen, ongemak in het oor.
- Darm- of maagbloeding.
- Maagpijn.
- Buikpijn, opgeblazen gevoel.
- Moeite met slikken.
- Infectie of ontsteking van de maag en darmen.
- Buikpijn.
- Irritatie van de mond of lippen, keelpijn.
- Verandering van de leverfunctie.
- Jeukende huid.
- Roodheid van de huid.
- Uitslag.
- Spiertrekkingen.
- Urineweginfectie.
- Pijn in de ledematen.
- Zwelling van het lichaam, inclusief zwelling rond de ogen en andere delen van het lichaam.
- Rillingen.
- Roodheid en pijn op de injectieplaats.
- Gevoel van algemene malaise.
- Verlies van lichaamsgewicht.
- Gewichtstoename.
Soms voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 100 mensen)
- Hepatitis.
- Ernstige allergische reactie (anafylactische reactie) waarvan de verschijnselen kunnen zijn: ademhalingsmoeilijkheden, pijn op de borst of beklemd gevoel op de borst en/of zich duizelig/zwak voelen, ernstige jeukende huid of bulten op de huid, zwelling van het gezicht, de lippen, de tong en/of of keel wat slikproblemen kan veroorzaken, collaps.
- Bewegingsstoornissen, verlamming, weeën.
- Duizeligheid.
- Gehoorverlies, doofheid.
- Aandoeningen die de longen aantasten, waardoor uw lichaam onvoldoende zuurstof krijgt. Enkele hiervan zijn ademhalingsmoeilijkheden, kortademigheid, piepende ademhaling, zelfs zonder lichamelijke activiteit, ademhaling die oppervlakkig of moeilijk wordt of stopt, piepende ademhaling.
- Bloedstolsels in de longen.
- Gele verkleuring van de ogen en huid (geelzucht).
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de injectieflacon en de doos na EXP.
Bewaren bij een temperatuur van maximaal 30 ° C. Bewaar de injectieflacon in de buitenverpakking om het geneesmiddel tegen licht te beschermen.
De gereconstitueerde oplossing moet onmiddellijk na bereiding worden gebruikt. Als de gereconstitueerde oplossing niet onmiddellijk wordt gebruikt, vallen de voorwaarden en tijden van gebruik onder de verantwoordelijkheid van de bereider. De gereconstitueerde oplossing is echter vóór toediening 8 uur stabiel bij 25°C indien bewaard in de oorspronkelijke injectieflacon en/of in een spuit, met een maximale bewaartijd voor het gereconstitueerde geneesmiddel van niet meer dan 8 uur.
VELCADE is uitsluitend voor eenmalig gebruik. Ongebruikt product en afval moeten worden afgevoerd in overeenstemming met de geldende lokale regelgeving.
Deadline "> Overige informatie
Wat bevat VELCADE
- Het werkzame bestanddeel is bortezomib. Elke injectieflacon bevat 3,5 mg bortezomib (als boorzuurester van mannitol). Na reconstitutie bevat 1 ml oplossing voor injectie 1 mg bortezomib.
- De andere stoffen in dit middel zijn mannitol (E421) en stikstof.
Reconstitutie voor intraveneus gebruik: Na reconstitutie bevat 1 ml oplossing voor intraveneuze injectie 1 mg bortezomib.
Reconstitutie voor subcutaan gebruik: Na reconstitutie bevat 1 ml oplossing voor subcutane injectie 2,5 mg bortezomib.
Beschrijving van hoe VELCADE eruit ziet en de inhoud van de verpakking
VELCADE poeder voor oplossing voor injectie is wit tot roomwit.
Elke verpakking VELCADE 3,5 mg bevat 1 glazen injectieflacon van 10 ml met een blauwe dop, in een doorzichtige blisterverpakking.
Deadline "> Informatie voor zorgprofessionals
De volgende informatie is alleen bedoeld voor beroepsbeoefenaren in de gezondheidszorg:
RECONSTITUTIE VOOR INTRAVENEUZE INJECTIE
Opmerking: VELCADE is een cytotoxisch middel. Daarom moet speciale aandacht worden besteed aan het hanteren en bereiden. Het wordt aanbevolen om handschoenen en andere beschermende kleding te dragen, om contact met de huid te voorkomen.
WEGENS DE AFWEZIGHEID VAN ENIGE SOORT CONSERVEERMIDDELEN, MOETEN ASEPTISCHE TECHNISCHE NORMEN WORDEN GEVOLGD TIJDENS HET HANTEREN VAN VELCADE.
- Bereiding van de 3,5 mg injectieflacon: Voeg 3,5 ml steriele natriumchloride 9 mg/ml (0,9%) oplossing voor injectie toe aan de injectieflacon met het VELCADE-poeder. Het gevriesdroogde poeder lost volledig op in minder dan 2 minuten.
De concentratie van de verkregen oplossing is gelijk aan 1 mg / ml. De oplossing zal helder en kleurloos zijn met een uiteindelijke pH tussen 4 en 7. Het is niet nodig om de pH van de oplossing te controleren.
- De oplossing moet vóór toediening visueel worden geïnspecteerd om te controleren op deeltjes of kleurverandering.In aanwezigheid van deeltjes of kleurverandering mag de oplossing niet worden gebruikt en moet deze worden weggegooid.
Bevestig de concentratie op de injectieflacon om er zeker van te zijn dat de juiste dosis intraveneus wordt toegediend (1 mg/ml).
- De gereconstitueerde oplossing is vrij van conserveringsmiddelen en dient direct na bereiding te worden gebruikt terwijl deze 8 uur chemisch en fysisch stabiel is bij 25°C in de originele injectieflacon en/of in een spuit met een maximum van 8 uur in de spuit. De totale bewaartijd van het gereconstitueerde geneesmiddel mag niet langer zijn dan 8 uur voorafgaand aan toediening. Als de gereconstitueerde oplossing niet onmiddellijk na bereiding wordt gebruikt, is het de verantwoordelijkheid van de gebruiker om vóór gebruik de bewaarcondities en -tijden van het product in acht te nemen.
Het is niet nodig om het gereconstitueerde geneesmiddel tegen licht te beschermen.
ADMINISTRATIE
- Zodra de oplossing is opgelost, trekt u de juiste hoeveelheid van de gereconstitueerde oplossing op in overeenstemming met de dosis die is berekend op basis van het lichaamsoppervlak van de patiënt.
- Bevestig vóór gebruik de dosis en concentratie in de spuit (controleer of de spuit is gemarkeerd voor intraveneuze toediening).
- Injecteer de oplossing intraveneus als een bolus van 3-5 seconden, via een perifere of centrale intraveneuze katheter.
- Spoel de intraveneuze katheter met steriele natriumchloride 9 mg/ml (0,9%) oplossing voor injectie.
VELCADE 3,5 mg poeder voor oplossing voor injectie IS VOOR SUBCUTAAN OF INTRAVENEUS GEBRUIK. Niet via andere routes toedienen. Intrathecale toediening leidde tot overlijden.
BESCHIKBAARHEID
De injectieflacon is uitsluitend voor eenmalig gebruik en de resterende oplossing moet worden weggegooid.
Ongebruikte medicijnen en afval van dit medicijn moeten worden vernietigd in overeenstemming met de lokale regelgeving.
De volgende informatie is alleen bedoeld voor beroepsbeoefenaren in de gezondheidszorg:
Alleen de injectieflacon van 3,5 mg kan subcutaan worden toegediend zoals hieronder beschreven.
RECONSTITUTIE VOOR SUBCUTANE INJECTIE
Opmerking: VELCADE is een cytotoxisch middel. Daarom moet speciale aandacht worden besteed aan het hanteren en bereiden. Het wordt aanbevolen om handschoenen en andere beschermende kleding te dragen, om contact met de huid te voorkomen.
WEGENS DE AFWEZIGHEID VAN ENIGE SOORT CONSERVEERMIDDELEN, MOETEN ASEPTISCHE TECHNISCHE NORMEN WORDEN GEVOLGD TIJDENS HET HANTEREN VAN VELCADE.
- Bereiding van de 3,5 mg injectieflacon: Voeg 1,4 ml steriele natriumchloride 9 mg/ml (0,9%) oplossing voor injectie toe aan de injectieflacon met het VELCADE-poeder. Het gevriesdroogde poeder lost volledig op in minder dan 2 minuten.
De concentratie van de verkregen oplossing is gelijk aan 2,5 mg/ml. De oplossing zal helder en kleurloos zijn met een uiteindelijke pH tussen 4 en 7. Het is niet nodig om de pH van de oplossing te controleren.
- De oplossing moet vóór toediening visueel worden geïnspecteerd om te controleren op deeltjes of kleurverandering.In aanwezigheid van deeltjes of kleurverandering mag de oplossing niet worden gebruikt en moet worden weggegooid.
Bevestig de concentratie op de injectieflacon om er zeker van te zijn dat de juiste dosis subcutaan wordt toegediend (2,5 mg/ml).
- De gereconstitueerde oplossing is vrij van conserveringsmiddelen en dient direct na bereiding te worden gebruikt terwijl deze 8 uur chemisch en fysisch stabiel is bij 25°C in de originele injectieflacon en/of in een spuit met een maximum van 8 uur in de spuit. De totale bewaartijd van het gereconstitueerde geneesmiddel mag niet langer zijn dan 8 uur voorafgaand aan toediening. Als de gereconstitueerde oplossing niet onmiddellijk na bereiding wordt gebruikt, is het de verantwoordelijkheid van de gebruiker om vóór gebruik de bewaarcondities en -tijden van het product in acht te nemen.
Het is niet nodig om het gereconstitueerde geneesmiddel tegen licht te beschermen.
ADMINISTRATIE
- Zodra de oplossing is opgelost, trekt u de juiste hoeveelheid van de gereconstitueerde oplossing op in overeenstemming met de dosis die is berekend op basis van het lichaamsoppervlak van de patiënt.
- Bevestig vóór gebruik de dosis en concentratie in de spuit (controleer of de spuit is gemarkeerd voor subcutane toediening).
- Injecteer de oplossing subcutaan, in een hoek van 45-90 °
- De gereconstitueerde oplossing wordt subcutaan toegediend in de dijen (rechts of links) of buik (rechts of links)
- Bij volgende toedieningen is het noodzakelijk om de injectieplaats afwisselend te wisselen.
- Als lokale reacties optreden op de injectieplaats na subcutane injectie van VELCADE, kan een lagere concentratie van VELCADE 3,5 mg oplossing (1 mg/ml in plaats van 2,5 mg/ml) worden toegediend of het wordt aanbevolen om over te schakelen op "intraveneuze injectie".
VELCADE 3,5 mg poeder voor oplossing voor injectie IS VOOR SUBCUTAAN OF INTRAVENEUS GEBRUIK. Niet via andere routes toedienen. Intrathecale toediening leidde tot overlijden.
BESCHIKBAARHEID
De injectieflacon is uitsluitend voor eenmalig gebruik en de resterende oplossing moet worden weggegooid.
Ongebruikte medicijnen en afval van dit medicijn moeten worden vernietigd in overeenstemming met de lokale regelgeving.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL -
VELCADE 3,5 MG POEDER VOOR OPLOSSING VOOR INJECTIE
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING -
Elke injectieflacon bevat 3,5 mg bortezomib (als boorzuurester van mannitol).
Na reconstitutie bevat 1 ml oplossing voor injectie voor subcutaan gebruik 2,5 mg bortezomib.
Na reconstitutie bevat 1 ml oplossing voor injectie voor intraveneus gebruik 1 mg bortezomib.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM -
Poeder voor oplossing voor injectie.
Wit tot roomwit poeder (al dan niet samengeperst).
04.0 KLINISCHE INFORMATIE -
04.1 Therapeutische indicaties -
VELCADE als monotherapie of in combinatie met gepegyleerd liposomaal doxorubicine of dexamethason is geïndiceerd voor de behandeling van volwassen patiënten met progressief multipel myeloom die al minstens één eerdere behandelingslijn hebben gekregen en die al een stamceltransplantatie hebben ondergaan of niet in aanmerking komen voor stamceltransplantatie. .
VELCADE in combinatie met melfalan en prednison is geïndiceerd voor de behandeling van volwassen patiënten met niet eerder behandeld multipel myeloom die niet in aanmerking komen voor hooggedoseerde chemotherapie met hematopoëtische stamceltransplantatie.
VELCADE in combinatie met dexamethason of met dexamethason en thalidomide is geïndiceerd voor de inductiebehandeling van volwassen patiënten met niet eerder behandeld multipel myeloom die in aanmerking komen voor hooggedoseerde chemotherapie met hematopoëtische stamceltransplantatie.
VELCADE in combinatie met rituximab, cyclofosfamide, doxorubicine en prednison is geïndiceerd voor de behandeling van volwassen patiënten met niet eerder behandeld mantelcellymfoom die niet in aanmerking komen voor hematopoëtische stamceltransplantatie.
04.2 Dosering en wijze van toediening -
De behandeling dient te worden gestart en toegediend onder toezicht van een arts die getraind en ervaren is in het gebruik van chemotherapeutische middelen VELCADE dient te worden gereconstitueerd door een beroepsbeoefenaar in de gezondheidszorg.
Dosering voor de behandeling van progressief multipel myeloom (patiënten die ten minste één eerdere behandelingslijn hebben gekregen)
Monotherapie
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11 in één behandelcyclus van 21 dagen Deze periode van 3 weken wordt beschouwd als een behandelingscyclus.
Het wordt aanbevolen dat patiënten 2 kuren VELCADE krijgen nadat is bevestigd dat een volledige respons is bereikt.
Patiënten die op de behandeling reageren maar geen volledige remissie bereiken, wordt aanbevolen om in totaal 8 kuren VELCADE toe te dienen.
Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Dosisaanpassingen tijdens de behandeling en hervatting als monotherapie
De behandeling met VELCADE dient te worden gestaakt bij het begin van een niet-hematologische toxiciteit van graad 3 of elke hematologische toxiciteit van graad 4, met uitzondering van neuropathie, zoals hieronder aangegeven (zie ook rubriek 4.4) toxiciteit, de behandeling met VELCADE kan worden hervat met een 25% lagere dosis ( 1,3 mg/m² verlaagd tot 1,0 mg/m², 1,0 mg/m² verlaagd tot 0,7 mg/m²) als de symptomen van toxiciteit niet zijn verdwenen, of als ze terugkeren bij een verlaagde dosis, moet staken van de behandeling met VELCADE worden overwogen, tenzij de voordelen van therapie duidelijk opwegen tegen de risico's.
Neuropathische pijn en/of perifere neuropathie
Patiënten die aan bortezomib gerelateerde neuropathische pijn en/of perifere neuropathie ervaren, moeten worden behandeld volgens tabel 1 (zie rubriek 4.4).
Patiënten met reeds bestaande ernstige neuropathie kunnen alleen met VELCADE worden behandeld na een "zorgvuldige risico-batenanalyse".
Tabel 1: Aanbevolen dosisaanpassingen * in geval van neuropathie gerelateerd aan de toediening van bortezomib
Combinatietherapie met gepegyleerd liposomaal doxorubicine
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11 in één behandelcyclus van 21 dagen Deze periode van 3 weken wordt beschouwd als een behandelingscyclus Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Gepegyleerd liposomaal doxorubicine wordt toegediend in een dosis van 30 mg/m² op dag 4 van de VELCADE-behandelingscyclus als een intraveneuze infusie van 1 uur na de injectie met VELCADE.
Er kunnen maximaal 8 cycli van deze combinatietherapie worden gegeven totdat patiënten progressie vertonen en de behandeling verdragen. Patiënten die een volledige respons bereiken, kunnen de behandeling voortzetten gedurende ten minste 2 cycli na het eerste bewijs van een volledige respons, zelfs als hiervoor een behandeling van meer dan 8 cycli nodig is. Patiënten bij wie de paraproteïnespiegels na 8 cycli blijven dalen, kunnen de behandeling voortzetten zolang de behandeling wordt verdragen en een respons blijven vertonen.
Raadpleeg voor meer informatie over gepegyleerd liposomaal doxorubicine de respectievelijke samenvatting van de productkenmerken.
Combinatie met dexamethason
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11 in één behandelcyclus van 21 dagen Deze periode van 3 weken wordt beschouwd als een behandelingscyclus Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Dexamethason wordt oraal toegediend in een dosis van 20 mg op de dagen 1, 2, 4, 5, 8, 9, 11 en 12 van de VELCADE-behandelingscyclus.
Patiënten die na 4 cycli van deze combinatietherapie een ziekterespons of stabilisatie bereiken, kunnen dezelfde combinatie gedurende maximaal 4 extra cycli blijven ontvangen.
Raadpleeg de respectievelijke samenvatting van de productkenmerken voor meer informatie over dexamethason.
Dosisaanpassing voor combinatietherapie bij patiënten met progressief multipel myeloom
Voor dosisaanpassingen van VELCADE in combinatietherapie volgt u de aanbevelingen voor dosisaanpassing beschreven in het gedeelte over monotherapie hierboven.
Dosering voor de behandeling van niet eerder behandeld multipel myeloom bij patiënten die niet in aanmerking komen voor hooggedoseerde chemotherapie met hematopoëtische stamceltransplantatie.
Combinatietherapie met melfalan en prednison
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in combinatie met oraal melfalan en oraal prednison, zoals aangegeven in Tabel 2. Een periode van 6 weken wordt als een behandelingskuur beschouwd. In cycli 1-4 wordt VELCADE tweemaal per week gegeven op dag 1, 4, 8, 11, 22, 25, 29 en 32. In cycli 5-9 wordt VELCADE eenmaal per week gegeven op dag 1, 8, 22 en 29. Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Melfalan en prednison moeten beide oraal worden toegediend op dag 1, 2, 3 en 4 van de eerste week van elke behandelingscyclus met VELCADE. Er worden 9 behandelcycli van deze combinatietherapie toegediend.
Tabel 2: Schema van de aanbevolen dosering van VELCADE in combinatie met melfalan en prednison
Dosisaanpassingen tijdens de behandeling en hervatting ervan in combinatie met melfalan en prednison
Voordat u met een nieuwe therapiekuur begint:
• het aantal bloedplaatjes moet ≥ 70 x 109 / l zijn en het absolute aantal neutrofielen (ANC) ≥ 1,0 x 109 / l
• Niet-hematologische toxiciteiten moeten zijn afgenomen tot graad 1 of baseline
Tabel 3: Veranderingen in dosering tijdens volgende kuren van VELCADE-therapie in combinatie met melfalan en prednison
Raadpleeg voor meer informatie over melfalan en prednison hun respectievelijke samenvattingen van productkenmerken.
Dosering voor de behandeling van niet eerder behandeld multipel myeloom bij patiënten die in aanmerking komen voor hematopoëtische stamceltransplantatie (inductietherapie).
Combinatietherapie met dexamethason
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11 in één behandelcyclus van 21 dagen Deze periode van 3 weken wordt beschouwd als een behandelingscyclus Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Dexamethason wordt oraal toegediend in een dosis van 40 mg op de dagen 1, 2, 3, 4, 8, 9, 10 en 11 van de VELCADE-behandelingscyclus.
Van deze combinatietherapie worden vier behandelcycli toegediend.
Combinatietherapie met thalidomide en dexamethason
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11 in één behandelcyclus van 28 dagen Deze periode van 4 weken wordt beschouwd als een behandelingscyclus.
Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Dexamethason wordt oraal toegediend in een dosis van 40 mg op de dagen 1, 2, 3, 4, 8, 9, 10 en 11 van de VELCADE-behandelingscyclus.
Thalidomide wordt oraal toegediend in een dagelijkse dosis van 50 mg op dag 1-14; indien getolereerd, wordt de dosis verhoogd tot 100 mg op dag 15-28 en kan vervolgens vanaf cyclus 2 verder worden verhoogd tot 200 mg per dag (zie tabel 4).
Van deze combinatietherapie worden vier behandelcycli toegediend.
Voor patiënten die ten minste een gedeeltelijke respons bereiken, worden 2 extra behandelingskuren aanbevolen.
Tabel 4: Dosering van combinatietherapie met VELCADE voor de behandeling van niet eerder behandeld multipel myeloom bij patiënten die in aanmerking komen voor hematopoëtische stamceltransplantatie.
Dosisaanpassing voor transplantatiekandidaten
Raadpleeg Tabel 1 voor VELCADE-dosisaanpassing voor neuropathie.
Wanneer VELCADE wordt toegediend in combinatie met andere chemotherapeutische middelen, dient bovendien een passende dosisverlaging van deze geneesmiddelen te worden overwogen in geval van toxiciteit volgens de aanbevelingen in de relevante Samenvatting van de productkenmerken.
Dosering voor patiënten met niet eerder behandeld mantelcellymfoom (MCL)
Combinatietherapie met rituximab, cyclofosfamide, doxorubicine en prednison (VcR-CAP)
VELCADE 3,5 mg poeder voor oplossing voor injectie wordt intraveneus of subcutaan toegediend in de aanbevolen dosis van 1,3 mg/m² lichaamsoppervlak tweemaal per week gedurende twee weken op dag 1, 4, 8 en 11, gevolgd door een rustperiode van 10 dagen op dag 12 tot 21. Deze periode van 3 weken wordt beschouwd als een behandelingskuur. Er moet ten minste 72 uur verstrijken tussen de toediening van twee opeenvolgende doses VELCADE.
Er worden 6 behandelcycli met deze combinatietherapie aanbevolen. Patiënten met een gedocumenteerde eerste respons op cyclus 6 kunnen 2 aanvullende behandelingskuren krijgen.
De volgende geneesmiddelen worden toegediend als een intraveneuze infusie op dag 1 van elke 3-weekse behandelingscyclus met VELCADE: rituximab in een dosis van 375 mg/m², cyclofosfamide in een dosis van 750 mg/m² en doxorubicine in een dosis van 50 mg / m².
Prednison wordt oraal toegediend in een dosis van 100 mg/m² op dag 1, 2, 3, 4 en 5 van elke VELCADE-behandelingscyclus.
Dosisaanpassing tijdens behandeling van patiënten met niet eerder behandeld MCL
Voordat u met een nieuwe therapiekuur begint:
• Het aantal bloedplaatjes moet ≥ 100.000 cellen/mcL zijn en het absolute aantal neutrofielen (ANC) moet ≥ 1.500 cellen/mcL zijn
• Het aantal bloedplaatjes moet ≥ 75.000 cellen/mcL zijn bij patiënten met beenmerginfiltratie of miltsekwestratie
• Hemoglobine moet ≥ 8 g / dL . zijn
• Niet-hematologische toxiciteiten moeten worden teruggebracht tot graad 1 of baseline.
De behandeling met VELCADE dient te worden gestaakt bij het begin van een graad ≥ 3 VELCADE-gerelateerde niet-hematologische toxiciteit (exclusief neuropathie) of graad ≥ 3 hematologische toxiciteiten (zie ook rubriek 4.4).Voor dosisaanpassing, zie tabel 5 hieronder.
In geval van hematologische toxiciteit kunnen granulocytgroeifactoren worden toegediend volgens de lokale standaardpraktijk. Preventief gebruik van granulocyt-groeifactoren moet worden overwogen in geval van herhaalde vertragingen in de toediening van therapieën.Wanneer klinisch aangewezen, dient transfusie van bloedplaatjes te worden overwogen voor de behandeling van trombocytopenie.
Tabel 5: Dosisaanpassing tijdens behandeling van patiënten met niet eerder behandelde MCL
Wanneer VELCADE wordt toegediend in combinatie met andere chemotherapeutische middelen, moet bovendien een "passende dosisverlaging van deze geneesmiddelen worden overwogen in geval van toxiciteit, volgens de aanbevelingen in de respectieve samenvatting van de productkenmerken".
Speciale populaties
Oudere patiënten
Er is geen klinisch bewijs dat erop wijst dat de dosis moet worden aangepast bij patiënten ouder dan 65 jaar met multipel myeloom of mantelcellymfoom.
Er zijn geen onderzoeken naar het gebruik van VELCADE bij oudere patiënten met niet eerder behandeld multipel myeloom die in aanmerking komen voor hooggedoseerde chemotherapie met hematopoëtische stamceltransplantatie.
Daarom kunnen bij deze populatie geen dosisaanbevelingen worden gedaan.
In een onderzoek bij niet eerder behandelde patiënten met mantelcellymfoom waren respectievelijk 42,9% en 10,4% van de aan VELCADE blootgestelde patiënten tussen 65-74 jaar en ≥ 75 jaar oud. Bij patiënten ≥ 75 jaar werden beide regimes, VELCADE in combinatie met rituximab, cyclofosfamide, doxorubicine en prednison (VcR-CAP) en rituximab, cyclofosfamide, doxorubicine, vincristine en prednison (R-CHOP), minder verdragen (zie paragraaf 4.8 ).
Leverfunctiestoornis
Patiënten met een lichte leverfunctiestoornis hebben geen dosisaanpassing nodig en dienen met de aanbevolen dosering te worden behandeld. Patiënten met een matige of ernstige leverfunctiestoornis dienen de behandeling met VELCADE te starten met een verlaagde dosis van 0,7 mg/m² per injectie tijdens de eerste behandelingskuur, en een daaropvolgende dosisverhoging tot 1,0 mg/m² of een verdere dosisverlaging tot 0,5 mg/m² kan worden overwogen op basis van de tolerantie van de patiënt (zie Tabel 6 en rubrieken 4.4 en 5.2).
Tabel 6: Aanbevolen initiële dosisaanpassingen van VELCADE voor patiënten met leverinsufficiëntie
Nierdisfunctie
De farmacokinetiek van bortezomib wordt niet beïnvloed bij patiënten met een lichte tot matige nierfunctiestoornis (creatinineklaring [CrCL]> 20 ml/min/1,73 m²); daarom zijn er bij deze patiënten geen dosisaanpassingen nodig. Het is niet bekend of de farmacokinetiek van bortezomib veranderd is bij patiënten met een ernstige nierfunctiestoornis die niet gedialyseerd worden (CrCL
Pediatrische populatie
De veiligheid en werkzaamheid van VELCADE bij patiënten jonger dan 18 jaar zijn niet vastgesteld (zie rubrieken 5.1 en 5.2) Er zijn geen gegevens beschikbaar.
Wijze van toediening
VELCADE 3,5 mg poeder voor oplossing voor injectie is bedoeld voor intraveneuze of subcutane toediening.
VELCADE 1 mg poeder voor oplossing voor injectie is uitsluitend bedoeld voor intraveneuze toediening.
VELCADE mag niet via andere routes worden toegediend. Intrathecale toediening veroorzaakte de dood.
Intraveneuze injectie
De gereconstitueerde oplossing van VELCADE 3,5 mg wordt intraveneus toegediend als een bolus van 3-5 seconden, via een perifere of centrale intraveneuze katheter, gevolgd door spoelen met natriumchloride 9 mg/ml (0,9%). Er moet ten minste 72 uur zitten tussen twee opeenvolgende doses VELCADE.
Subcutane injectie
De gereconstitueerde oplossing van VELCADE 3,5 mg wordt subcutaan toegediend in de dijen (rechts of links) of buik (rechts of links) De oplossing moet subcutaan worden geïnjecteerd in een hoek van 45-90 °.
Injectieplaatsen moeten afwisselend worden gewisseld voor volgende injecties.
Als reacties op de injectieplaats optreden na subcutane toediening van VELCADE, kan een minder geconcentreerde oplossing van VELCADE (VELCADE 3,5 mg gereconstitueerd in 1 mg/ml in plaats van 2,5 mg/ml) subcutaan worden toegediend of wordt aanbevolen om over te schakelen op intraveneuze toediening.
Als VELCADE wordt toegediend in combinatie met andere geneesmiddelen, raadpleeg dan de Samenvatting van de productkenmerken van deze geneesmiddelen voor instructies over toediening.
04.3 Contra-indicaties -
Overgevoeligheid voor de werkzame stof, voor boor of voor één van de in rubriek 6.1 vermelde hulpstoffen.
Acute diffuse infiltratieve longziekte en pericardiopathie.
Als VELCADE in combinatie met andere geneesmiddelen wordt gegeven, raadpleeg dan de relevante samenvatting van de productkenmerken voor aanvullende contra-indicaties.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik -
Wanneer VELCADE wordt toegediend in combinatie met andere geneesmiddelen, dient de relevante samenvatting van de productkenmerken te worden geraadpleegd voordat de behandeling met VELCADE wordt gestart. Bijzondere aandacht moet worden besteed aan zwangerschapstesten en voorschriften voor zwangerschapspreventie wanneer thalidomide wordt toegediend (zie rubriek 4.6).
Intrathecale toediening
Er zijn sterfgevallen na onbedoelde intrathecale toediening van VELCADE. VELCADE 1 mg poeder voor oplossing voor injectie is uitsluitend bedoeld voor intraveneus gebruik, terwijl VELCADE 3,5 mg poeder voor oplossing voor injectie bedoeld is voor intraveneus of subcutaan gebruik. VELCADE mag niet intrathecaal worden toegediend.
Gastro-intestinale toxiciteit
Gastro-intestinale toxische effecten, waaronder misselijkheid, diarree, braken en constipatie, komen zeer vaak voor tijdens behandeling met VELCADE. Gevallen van paralytische ileus zijn soms gemeld (zie rubriek 4.8). Daarom moeten patiënten die constipatie ervaren nauwlettend worden gevolgd.
Hematologische toxiciteit
Behandeling met VELCADE gaat heel vaak gepaard met hematologische toxische effecten (trombocytopenie, neutropenie en anemie). In onderzoeken uitgevoerd bij patiënten met recidiverend multipel myeloom die werden behandeld met VELCADE en bij patiënten met niet eerder behandeld MCL die werden behandeld met VELCADE in combinatie met rituximab, cyclofosfamide, doxorubicine en prednison (VcR-CAP), was een van de meest voorkomende hematologische toxiciteiten voorbijgaande trombocytopenie.Bloedplaatjes waren op hun laagste niveau op dag 11 van elke VELCADE-behandelingscyclus en keerden gewoonlijk terug naar het uitgangsniveau in de volgende cyclus. Er waren geen aanwijzingen voor cumulatieve trombocytopenie. Het nadir van de gemiddelde bloedplaatjeswaarde was ongeveer 40% van de uitgangswaarde in de multipel myeloom-onderzoeken met VELCADE als monotherapie en 50% in het MCL-onderzoek. Bij patiënten met gevorderd myeloom was de ernst van trombocytopenie gerelateerd aan de bloedplaatjeswaarden vóór de behandeling: voor de bloedplaatjeswaarden bij baseline 75.000 / mcl had slechts 14% van de 309 patiënten een aantal bloedplaatjes ≤ 25.000 / mcl tijdens het onderzoek.
Bij patiënten met MCL (onderzoek LYM-3002) was er een hogere incidentie (56,7% versus 5,8%) Graad ≥ 3 trombocytopenie in de VELCADE-behandelingsgroep (VcR-CAP) versus de niet-VELCADE-groep (rituximab, cyclofosfamide, doxorubicine, vincristine en prednison [R-CHOP]). De twee behandelingsgroepen waren vergelijkbaar in zowel de totale incidentie van bloedingen van alle gradaties (6,3% in de VcR-CAP-groep en 5,0% in de R-CHOP-groep) als in graad 3 en ernstige bloedingen (VcR-CAP: 4 patiënten [ 1,7%]; R-CHOP: 3 patiënten [1,2%]) In de VcR-CAP-groep ontving 22,5% van de patiënten een trombocytentransfusie vergeleken met 2,9% van de patiënten in de R-CHOP-groep.
Gastro-intestinale en intracerebrale bloedingen zijn gemeld in verband met behandeling met VELCADE. Daarom moeten de bloedplaatjesspiegels worden gecontroleerd voordat elke dosis VELCADE wordt toegediend. De behandeling met VELCADE moet worden stopgezet wanneer het aantal bloedplaatjes waarden bereikt
Het volledige bloedbeeld, met differentiële tellingen en inclusief het aantal bloedplaatjes, moet regelmatig worden gecontroleerd tijdens de behandeling met VELCADE Indien klinisch aangewezen, moet bloedplaatjestransfusie worden overwogen (zie rubriek 4.2).
Bij MCL-patiënten zonder bewijs van cumulatieve neutropenie werd tussen de behandelingskuren voorbijgaande reversibele neutropenie waargenomen. Neutrofielen waren op hun laagste niveau op dag 11 van elke VELCADE-behandelingscyclus en keerden gewoonlijk terug naar de uitgangswaarde in de volgende cyclus. In onderzoek LYM-3002 werd groeifactorondersteuning toegepast bij 78% van de patiënten in de VcR-CAP-arm en bij 61% van de patiënten in de R-CHOP-arm. Aangezien patiënten met neutropenie een verhoogd risico op infecties hebben, moeten ze worden gecontroleerd op tekenen en symptomen van infectie en onmiddellijk worden behandeld. Voor de behandeling van hematologische toxiciteit kunnen volgens lokale standaardpraktijken granulocytgroeifactoren worden toegediend. In het geval van herhaald uitstel van de toediening van therapiekuren, dient het preventieve gebruik van granulocytgroeifactoren te worden overwogen (zie rubriek 4.2).
Reactivering van het herpes zoster-virus
Toediening van antivirale profylaxe wordt aanbevolen bij patiënten die VELCADE krijgen. In de fase III-studie die werd uitgevoerd bij patiënten met niet eerder behandeld multipel myeloom, kwam de algehele incidentie van herpes zoster-reactivatie vaker voor bij patiënten die werden behandeld met VELCADE + Melfalan + Prednison dan bij patiënten die werden behandeld met Melfalan + Prednison (respectievelijk 14% versus 4%).
Bij patiënten met MCL (onderzoek LYM-3002) was de incidentie van herpes zoster-infectie 6,7% in de VcR-CAP-arm en 1,2% in de R-CHOP-arm (zie rubriek 4.8).
Reactivering en infectie met hepatitis B-virus (HBV)
Wanneer rituximab wordt gebruikt in combinatie met VELCADE, moeten patiënten met een risico op HBV-infectie altijd op HBV worden gescreend voordat met de behandeling wordt begonnen. Dragers van hepatitis B en patiënten met een voorgeschiedenis van hepatitis B moeten tijdens en na behandeling met rituximab in combinatie met VELCADE nauwlettend worden gecontroleerd op klinische en laboratoriumsymptomen van actieve HBV-infectie. Antivirale profylaxe moet worden overwogen. Raadpleeg de samenvatting van de productkenmerken van rituximab voor meer informatie.
Progressieve multifocale leuko-encefalopathie (PML)
Zeer zeldzame gevallen van infectie met het John Cunningham-virus (JC) resulterend in PML en overlijden zijn gemeld bij patiënten die met VELCADE werden behandeld, met onbekende causaliteit. Patiënten met de diagnose PML hadden eerder een immunosuppressieve therapie ondergaan of gebruikten deze gelijktijdig. De meeste gevallen van PML werden gediagnosticeerd binnen 12 maanden na inname van de eerste dosis VELCADE. Patiënten moeten regelmatig worden gecontroleerd op nieuwe of verergerende neurologische symptomen of tekenen die kunnen wijzen op PML bij de differentiële diagnoses van problemen met het centrale zenuwstelsel. Als een diagnose van PML wordt vermoed, moeten patiënten worden doorverwezen naar een arts die gespecialiseerd is in de behandeling van PML en moeten passende diagnostische maatregelen voor PML worden genomen. In het geval van een bevestigde diagnose van PML, moet de behandeling met VELCADE worden stopgezet.
Perifere neuropathie
Behandeling met VELCADE gaat meestal gepaard met het ontstaan van perifere, voornamelijk sensorische neuropathie. Er zijn echter gevallen van ernstige motorische neuropathie met of zonder perifere sensorische neuropathie gemeld.
De incidentie van perifere neuropathie neemt vroeg in de behandeling toe en piekt in cyclus 5.
Patiënten moeten nauwlettend worden gecontroleerd op symptomen van neuropathie zoals een branderig gevoel, hyperesthesie, hypesthesie, paresthesie, malaise, neuropathische pijn of zwakte.
In het klinische fase III-onderzoek waarin intraveneuze toediening van VELCADE werd vergeleken met de subcutane toedieningsweg, was de incidentie van perifere neuropathie van graad 2 24% in de groep met subcutane toediening en 41% in de groep met intraveneuze injectie (p = 0,0124). neuropathie trad op bij 6% van de patiënten in de subcutane behandelingsgroep vergeleken met 16% in de intraveneuze behandelingsgroep (p = 0,0264) alle graden van perifere neuropathie bij intraveneuze toediening van VELCADE waren lager in eerdere onderzoeken waarbij VELCADE intraveneus werd toegediend dan in onderzoek MMY -3021.
Neurologische evaluatie wordt aanbevolen bij patiënten met aanvang of verergering van perifere neuropathie, voor wie een wijziging van de dosis of het regime of een wijziging van de toedieningsweg naar de subcutane toedieningsweg nodig kan zijn (zie rubriek 4.2). Neuropathie werd behandeld met ondersteunende of andere therapieën.
Vroege en regelmatige controle op symptomen van behandelingsgerelateerde neuropathie met een neurologische evaluatie moet worden overwogen bij patiënten die VELCADE krijgen in combinatie met geneesmiddelen waarvan bekend is dat ze in verband worden gebracht met neuropathie (bijv. thalidomide) en er moet passende aandacht worden besteed aan dosisverlaging of stopzetting van de behandeling .
Naast perifere neuropathie kan autonome neuropathie bijdragen aan het ontstaan van sommige bijwerkingen, zoals orthostatische hypotensie en ernstige ileusconstipatie.Er is nog steeds beperkte informatie beschikbaar over autonome neuropathie en de bijdrage ervan aan deze bijwerkingen.
stuiptrekkingen
Toevallen zijn soms gemeld bij patiënten zonder voorgeschiedenis van toevallen of epilepsie. Speciale zorg is vereist bij de behandeling van patiënten met een verhoogd risico op epileptische aanvallen.
Hypotensie
Behandeling met VELCADE wordt vaak geassocieerd met orthostatische/orthostatische hypotensie. De meeste bijwerkingen zijn licht tot matig van ernst en zijn waargenomen tijdens de behandeling. Patiënten die orthostatische hypotensie ondervonden met VELCADE (intraveneus geïnjecteerd) hadden voorafgaand aan de behandeling geen eerdere episodes van orthostatische hypotensie. Bij de meeste patiënten was therapie voor de behandeling van orthostatische hypotensie vereist Een minderheid van de patiënten met orthostatische hypotensie kreeg te maken met syncope-episodes Orthostatische/orthostatische hypotensie was niet acuut gerelateerd aan een bolusinfusie van VELCADE.
Het mechanisme van deze gebeurtenis is onbekend, hoewel een component kan worden bepaald door autonome neuropathie. Autonome neuropathie kan verband houden met bortezomib, of het is mogelijk dat het geneesmiddel een reeds bestaande aandoening, zoals diabetische of amyloïdische neuropathie, kan verergeren. De uiterste voorzichtigheid is geboden bij de behandeling van patiënten met een voorgeschiedenis van syncope die worden behandeld met geneesmiddelen waarvan bekend is dat ze verband houden met hypotensie, of patiënten die uitdroging vertonen als gevolg van terugkerende diarree of braken Orthostatische/orthostatische hypotensie kan worden behandeld met een dosisaanpassing van antihypertensiva, rehydratatie of toediening van mineralocorticosteroïden en/of sympathicomimetica Patiënten dienen geadviseerd te worden hun arts te raadplegen bij duizeligheid, een licht gevoel in het hoofd of korte perioden van flauwvallen.
Posterieur reversibel encefalopathiesyndroom (PRES)
Er zijn meldingen geweest van PRES bij patiënten die VELCADE kregen. PRES is een zeldzame neurologische vorm die wordt gekenmerkt door een snelle, vaak omkeerbare evolutie die zich kan manifesteren met toevallen, hypertensie, hoofdpijn, lethargie, verwardheid, blindheid en andere visuele en neurologische veranderingen. De diagnose wordt bevestigd door radiologische beelden van de hersenstructuren, bij voorkeur verkregen met Nucleaire Magnetische Resonantie (MRI). Bij patiënten die PRES ontwikkelen, moet de behandeling met VELCADE worden stopgezet.
Hartfalen
Acuut begin of verergering van congestief hartfalen en/of ontwikkeling van verminderde linkerventrikelejectiefractie is waargenomen tijdens behandeling met bortezomib Vochtretentie kan een predisponerende factor zijn voor tekenen en symptomen van hartfalen Patiënten met hartfalen of met risicofactoren voor hartfalen moeten zorgvuldig worden gecontroleerd.
Elektrocardiografische onderzoeken
In klinische onderzoeken zijn geïsoleerde gevallen van verlenging van het QT-interval waargenomen, waarvan de causaliteit niet is vastgesteld.
Pulmonale veranderingen
Zeldzame gevallen van acute diffuse infiltratieve longziekte met onbekende etiologie, zoals pneumonie, interstitiële pneumonie, pulmonale infiltratie en acute respiratory distress syndrome (ARDS), zijn gemeld bij patiënten die VELCADE kregen (zie rubriek 4.8). Sommige van deze afleveringen waren fataal. Een thoraxfoto voorafgaand aan de behandeling wordt aanbevolen als referentiepunt voor mogelijke pulmonale veranderingen na de behandeling.
In het geval van het ontstaan of verergeren van longsymptomen (bijv. hoesten, dyspneu), moet een snelle diagnostische evaluatie van de patiënt en de daaruit voortvloeiende passende behandeling worden uitgevoerd. De risico-batenverhouding moet worden afgewogen voordat de behandeling met VELCADE wordt voortgezet.
In een klinische studie stierven twee van de twee patiënten die een hoge dosis cytarabine (2 g/m² per dag) kregen als een 24-uurs continue infusie in combinatie met daunorubicine en VELCADE voor de behandeling van recidiverende acute myeloïde leukemie als gevolg van ARDS. in de beginfase van de therapie werd de studie stopgezet. Dit specifieke combinatietherapieregime met hoge doses cytarabine (2 g/m² per dag) in continue 24-uurs infusie wordt daarom niet aanbevolen.
Verminderde nierfunctie
Niercomplicaties komen vaak voor bij patiënten met multipel myeloom. Patiënten met nierinsufficiëntie moeten zorgvuldig worden gecontroleerd (zie rubrieken 4.2 en 5.2).
Verminderde leverfunctie
Bortezomib wordt gemetaboliseerd door leverenzymen. Bij patiënten met een matige of ernstige leverfunctiestoornis is de blootstelling aan bortezomib verhoogd; deze patiënten moeten worden behandeld met een verlaagde dosis VELCADE en moeten zorgvuldig worden gecontroleerd op het optreden van toxiciteit (zie rubrieken 4.2 en 5.2. ).
Leverreacties
Zeldzame gevallen van leverfalen zijn gemeld bij patiënten die VELCADE en gelijktijdige medicamenteuze therapieën kregen en met een ernstige onderliggende ziekte. Andere leverreacties zoals verhoogde leverenzymen, hyperbilirubinemie en hepatitis zijn gemeld. Deze veranderingen kunnen omkeerbaar zijn na stopzetting van de behandeling met bortezomib (zie rubriek 4.8).
Tumorlysissyndroom
Aangezien bortezomib een cytotoxische stof is en daarom in staat is kwaadaardige plasmacellen en MCL-cellen snel te vernietigen, kunnen complicaties van het tumorlysissyndroom worden waargenomen. Patiënten met een risico op het ontwikkelen van het tumorlysissyndroom zijn patiënten die een hoge tumorlast hebben laten zien voordat ze met de behandeling beginnen.Deze patiënten dienen zorgvuldig te worden gecontroleerd en er dienen voorzorgsmaatregelen te worden genomen.
Gelijktijdige toediening van andere geneesmiddelen
Patiënten die gelijktijdig worden behandeld met bortezomib en krachtige CYP3A4-remmers moeten zorgvuldig worden gecontroleerd. Bijzondere voorzichtigheid is geboden bij gelijktijdige toediening van bortezomib en CYP3A4- of CYP2C19-substraten (zie rubriek 4.5).
Normale leverfunctie moet worden bevestigd bij patiënten die orale hypoglykemieën krijgen en die met voorzichtigheid worden behandeld (zie rubriek 4.5).
Mogelijk door immuuncomplex gemedieerde reacties
Mogelijke immuuncomplexgerelateerde reacties, zoals serumziekte, polyartritis met huiduitslag en proliferatieve glomerulonefritis, zijn soms gemeld. De toediening van bortezomib moet worden gestaakt in geval van ernstige gebeurtenissen.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie -
Opleiding in vitro geven aan dat bortezomib een zwakke remmer is van cytochroom P450 iso-enzymen (CYP) 1A2, 2C9, 2C19, 2D6 en 3A4. Gezien de beperkte bijdrage (7%) van het CYP2D6-iso-enzym aan het metabolisme van bortezomib, wordt niet aangenomen dat dit lage metaboliserende fenotype de algehele beschikbaarheid van bortezomib beïnvloedt.
Een klinisch geneesmiddelinteractieonderzoek, gebaseerd op gegevens van 12 patiënten, om het effect van ketoconazol, een krachtige CYP3A4-remmer, op de farmacokinetiek van bortezomib (intraveneus geïnjecteerd) te onderzoeken, toonde een gemiddelde toename van de AUC van bortezomib met 35% (90%) CI [1.032-1.772)] Daarom moeten patiënten die gelijktijdig worden behandeld met bortezomib en krachtige CYP3A4-remmers (bijv. ketoconazol, ritonavir) nauwlettend worden gecontroleerd.
In een klinisch geneesmiddelinteractieonderzoek, gebaseerd op gegevens van 17 patiënten, om het effect van omeprazol, een krachtige CYP2C19-remmer, op de farmacokinetiek van bortezomib (intraveneus geïnjecteerd) te onderzoeken, was er geen bewijs van een effect. bortezomib.
Een geneesmiddelinteractiestudie, gebaseerd op gegevens van 6 patiënten, om het effect van rifampicine, een krachtige CYP3A4-inductor, op de farmacokinetiek van bortezomib (intraveneus geïnjecteerd) te onderzoeken, liet een gemiddelde verlaging van de AUC zien: 45% bortezomib. van bortezomib met krachtige CYP3A4-inductoren (bijv. rifampicine, carbamazepine, fenytoïne, fenobarbital en sint-janskruid) wordt niet aanbevolen omdat de werkzaamheid kan worden verminderd.
In hetzelfde geneesmiddelinteractieonderzoek, op gegevens van 7 patiënten, om het effect van dexamethason, een zwakke CYP3A4-inductor, op de farmacokinetiek van bortezomib (intraveneus geïnjecteerd) te verifiëren, was er geen significant effect op de farmacokinetiek van bortezomib.
Een geneesmiddelinteractieonderzoek, gebaseerd op gegevens van 21 patiënten, om het effect van melfalan-prednison op de farmacokinetiek van bortezomib (intraveneus geïnjecteerd) te evalueren, liet een toename van de AUC van bortezomib met 17% zien.
Dit werd niet als klinisch relevant beschouwd.
In klinische onderzoeken werden soms hypoglykemie en hyperglykemie gemeld bij diabetespatiënten die orale hypoglykemische geneesmiddelen kregen. Patiënten die orale antidiabetica krijgen en VELCADE krijgen, kunnen een zorgvuldige bloedglucosecontrole en aanpassing van de dosering van antidiabetica nodig hebben.
04.6 Zwangerschap en borstvoeding -
Anticonceptie bij mannen en vrouwen
Mannen en vrouwen die zwanger kunnen worden, moeten adequate anticonceptiemaatregelen nemen tijdens de toediening en gedurende 3 maanden na de behandeling.
Zwangerschap
Er zijn geen klinische gegevens beschikbaar over blootstelling aan bortezomib tijdens de zwangerschap Het teratogene potentieel van bortezomib is niet volledig onderzocht.
In preklinische onderzoeken vertoonde toediening van bortezomib in de maximaal getolereerde doses door de moeder geen effect op de embryofoetale ontwikkeling bij ratten en konijnen. Er zijn geen dierstudies uitgevoerd om effecten op de bevalling en postnatale ontwikkeling vast te stellen (zie rubriek 5.3). VELCADE mag niet tijdens de zwangerschap worden gebruikt, tenzij de klinische toestand van de patiënt het gebruik ervan vereist.
De patiënt moet worden geïnformeerd over de mogelijke risico's voor de foetus als VELCADE tijdens de zwangerschap wordt toegediend of als de patiënte tijdens de behandeling zwanger wordt.
Thalidomide is een krachtig humaan teratogeen en veroorzaakt ernstige, levensbedreigende geboorteafwijkingen Thalidomide is gecontra-indiceerd tijdens de zwangerschap en bij vrouwen die zwanger kunnen worden, tenzij aan alle voorwaarden van het thalidomide-programma voor zwangerschapspreventie is voldaan. Patiënten die VELCADE in combinatie met thalidomide krijgen, moeten zich houden aan de thalidomide Zwangerschapspreventieprogramma Raadpleeg de samenvatting van de productkenmerken van thalidomide voor aanvullende informatie.
Voedertijd
Het is niet bekend of bortezomib wordt uitgescheiden in de moedermelk. Vanwege de mogelijkheid van ernstige bijwerkingen van VELCADE bij zuigelingen die borstvoeding krijgen, moet de borstvoeding worden gestaakt tijdens de behandeling met VELCADE.
Vruchtbaarheid
Er zijn geen vruchtbaarheidsonderzoeken uitgevoerd met VELCADE (zie rubriek 5.3).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen -
VELCADE kan de rijvaardigheid of het vermogen om machines te bedienen matig beïnvloeden.
VELCADE kan zeer vaak in verband worden gebracht met vermoeidheid, vaak met duizeligheid, soms met syncope, vaak met orthostatische/orthostatische hypotensie of wazig zien. Patiënten dienen uiterst voorzichtig te zijn bij het besturen van voertuigen of het bedienen van machines (zie rubriek 4.8).
05.0 FARMACOLOGISCHE EIGENSCHAPPEN -
05.1 "Farmacodynamische eigenschappen -
Farmacotherapeutische categorie: antineoplastische geneesmiddelen, overige antineoplastische geneesmiddelen.
ATC-code: L01XX32.
Werkingsmechanisme
Bortezomib is een proteasoomremmer. Het is specifiek geïndiceerd om de chymotrypsine-achtige activiteit van het 26S-proteasoom in zoogdiercellen te remmen. Het 26S-proteasoom is een groot polypeptidecomplex dat verantwoordelijk is voor de afbraak van ubiquinated eiwitten. De ubiquitine-proteasoom metabole route speelt een essentiële rol bij het beheersen van de omzet van specifieke eiwitten, waardoor de homeostase in de cellen behouden blijft. Remming van het 26S-proteasoom voorkomt deze gerichte proteolyse en beïnvloedt de signaaloverdracht in de cel, wat resulteert in de dood van kankercellen.
Bortezomib is zeer selectief voor het proteasoom. Bij concentraties van 10 M remt bortezomib geen van de talrijke onderzochte receptoren en proteasen en is het meer dan 1500 keer selectiever voor het proteasoom dan het tweede doelenzym. Proteosoomremmingskinetiek werd geëvalueerd in vitro en bortezomib dissocieert van het proteasoom met een t½ van 20 minuten, waarmee wordt aangetoond dat bortezomib-remming omkeerbaar is.
Door bortezomib gemedieerde remming van het proteasoom heeft talrijke effecten op kankercellen, waaronder, maar niet beperkt tot, de "verandering van regulerende eiwitten die de voortgang van de celcyclus controleren en" activering van nucleaire factor kB (NF-kB). L " remming van de proteasoom leidt tot stopzetting van de celcyclus en apoptose.
NF-kB is een transcriptiefactor waarvan de activering vereist is in vele stadia van carcinogenese, waaronder celgroei en overleving, angiogenese, celinteractie en metastase. Bij myeloom beïnvloedt bortezomib het vermogen van myeloomcellen om te interageren met de micro-omgeving van het beenmerg.
Proeven hebben aangetoond dat bortezomib cytotoxisch is voor tal van soorten kankercellen en dat deze cellen veel gevoeliger zijn voor de pro-apoptotische effecten van proteasoomremming dan normale.Bortezomib veroorzaakt een vermindering van de tumorgroei. in vivo in veel preklinische kankermodellen, waaronder multipel myeloom.
Gegevens in vitro, ex vivo en in diermodellen suggereren dat bortezomib de differentiatie en activiteit van osteoblasten verhoogt en de osteoclastische functie remt. Deze effecten zijn waargenomen bij patiënten met multipel myeloom met gevorderde osteolytische ziekte en die werden behandeld met bortezomib.
Klinische werkzaamheid bij niet eerder behandeld multipel myeloom
Een internationale, gerandomiseerde (1: 1), open-label, prospectieve fase III (MMY-3002 VISTA) klinische studie werd uitgevoerd bij 682 patiënten om te evalueren of VELCADE (Vc) (1,3 mg/m² intraveneus geïnjecteerd) in combinatie met melfalan ( M) (9 mg/m²) en prednison (P) (60 mg/m²) verbeterde tijd tot progressie (TTP) vergeleken met melfalan (9 mg/m²) en prednison (60 mg/m²) bij patiënten met niet eerder behandeld multipel myeloom . De behandeling werd gegeven gedurende maximaal 9 cycli (ongeveer 54 weken) en werd vroegtijdig stopgezet in geval van ziekteprogressie of onaanvaardbare toxiciteit. In het onderzoek was de mediane leeftijd van de patiënten 71 jaar, 50% was man, 88% was blank en de mediane Karnofsky-score voor prestatiestatus van de patiënten was 80.Patiënten hadden in 63% / 25% / 8% van de gevallen IgG / IgA / lichte keten-myeloom, een mediane hemoglobine van 105 g / l en een mediane aantal bloedplaatjes van 221,5 x 109 / l. Het percentage patiënten met een creatinineklaring ≤ 30 ml/min (3% in elke arm) was vergelijkbaar in de twee groepen.
Ten tijde vantussentijdse analyse gepland, het primaire eindpunt, de tijd tot progressie, was bereikt en patiënten in de M + P-arm kregen een behandeling met Vc + M + P. De mediane follow-up was 16,3 maanden Na een mediane follow-up Het uiteindelijke overlevingscijfer werd bijgewerkt Er werd een statistisch significant overlevingsvoordeel waargenomen in het voordeel van de Vc + M + P-behandelingsgroep (HR = 0,695, p = 0,00043) ondanks daaropvolgende therapieën, waaronder op VELCADE gebaseerde regimes. Mediane overleving in de Vc + M + P-behandeling groep was 56,4 maanden vergeleken met 43,1 maanden in de behandelingsgroep M + P. De werkzaamheidsresultaten worden weergegeven in Tabel 11.
Tabel 11: Werkzaamheidsresultaten na definitieve update van VISTA-overlevingsgegevens
Kandidaat-patiënten voor stamceltransplantatie
Er zijn twee gerandomiseerde, open-label multicenter klinische fase III-onderzoeken (IFM-2005-01, MMY-3010) uitgevoerd om de veiligheid en werkzaamheid van VELCADE in dubbele en driedubbele combinatie met andere chemotherapeutische middelen aan te tonen als inductietherapie vóór stamceltransplantatie bij patiënten die eerder onbehandeld voor multipel myeloom.
In onderzoek IFM-2005-01 werd VELCADE in combinatie met dexamethason [VcDx, n = 240] vergeleken met vincristine-doxorubicine-dexamethason [VDDx, n = 242]. Patiënten in de VcDx-groep kregen vier cycli van 21 dagen, die elk bestonden uit VELCADE (1,3 mg/m² tweemaal per week intraveneus toegediend op dag 1, 4, 8 en 11) en oraal dexamethason (40 mg/m²). dag 1 t/m 4 en op dag 9 t/m 12, in cycli 1 en 2, en op dag 1 t/m 4 in cycli 3 en 4).
Honderd achtennegentig patiënten (82%) en 208 patiënten (87%) in respectievelijk de VDDx- en VcDx-groepen hadden een autologe stamceltransplantatie ondergaan; de meeste patiënten ondergingen een enkele transplantatie. De demografische gegevens van patiënten en ziektekenmerken bij baseline waren vergelijkbaar tussen de twee behandelingsgroepen. In de studie was de mediane leeftijd van de patiënten 57 jaar, 55% was man en 48% van de patiënten had een hoog cytogenetisch risico.De mediane duur van de behandeling was 13 weken voor de VDDx-groep en 11 weken voor de VDDx-groep. VcDx Het mediane aantal cycli dat door beide groepen werd ontvangen, was 4 cycli.
Het primaire werkzaamheidseindpunt van het onderzoek was het responspercentage na inductie (CR + nCR). Er werd een statistisch significant verschil in CR + nCR waargenomen in het voordeel van de VELCADE-groep in combinatie met dexamethason. Secundaire werkzaamheidseindpunten waren onder meer responspercentages (CR + nCR, CR). + nCR + VGPR + PR) post-transplantatie, progressievrije overleving en algehele overleving De belangrijkste werkzaamheidsresultaten worden weergegeven in Tabel 12.
Tabel 12: Werkzaamheidsresultaten in onderzoek IFM-2005-01
In studie MMY-3010 werd VELCADE in combinatie met thalidomide en dexamethason [VcTDx, n = 130] vergeleken met thalidomide-dexamethason [TDx, n = 127]. Patiënten in de VcTDx-groep kregen zes cycli van 4 weken, die elk bestonden uit VELCADE (1,3 mg/m² tweemaal per week toegediend op dag 1, 4, 8 en 11, gevolgd door een rustperiode van 17 dagen 12 tot en met 28), dexamethason (40 mg oraal toegediend op dag 1 tot 4 en dag 8 tot en met 11), en thalidomide (50 mg per dag oraal toegediend op dag 1-14, met dosisverhoging tot 100 mg op dag 15-28 en daarna tot 200 mg per dag).
Honderdvijf patiënten (81%) en 78 patiënten (61%) in respectievelijk de VcTDx- en TDx-groepen. ze hadden een enkele autologe stamceltransplantatie ondergaan. De demografische gegevens van patiënten en ziektekenmerken bij baseline waren vergelijkbaar tussen de twee behandelingsgroepen. Patiënten in respectievelijk de VcTDx- en TDx-groepen hadden een mediane leeftijd van 57 en 56 jaar, 99% en 98% van de patiënten was blank; 58% en 54% waren man. In de VcTDx-groep werd 12% van de patiënten cytogenetisch geclassificeerd als hoog risico vergeleken met 16% van de patiënten in de TDx-groep. De mediane duur van de behandeling was 24,0 weken en het mediane aantal ontvangen behandelingscycli was 6,0 en was consistent in alle behandelingsgroepen.
De primaire werkzaamheidseindpunten van het onderzoek waren post-inductie en post-transplantatie responspercentages (CR + nCR). Een statistisch significant verschil in CR + nCR werd waargenomen in het voordeel van de behandelingsgroep met VELCADE in combinatie met dexamethason en thalidomide. Secundaire werkzaamheidseindpunten waren progressievrije overleving en algehele overleving. De belangrijkste werkzaamheidsresultaten worden weergegeven in tabel 13.
Tabel 13: Werkzaamheidsresultaten van onderzoek MMY-3010
Klinische werkzaamheid bij patiënten met recidiverend of refractair multipel myeloom
De veiligheids- en werkzaamheidsprofielen van VELCADE (intraveneus geïnjecteerd) werden geëvalueerd in twee onderzoeken met de aanbevolen dosis van 1,3 mg/m²: een gerandomiseerde, gecontroleerde dexamethason (Dex) fase III (APEX) studie uitgevoerd bij 669 patiënten met recidiverend en refractair multipel myeloom , die 1 tot 3 eerdere behandelingslijnen en een eenarmige fase II-studie hebben ondergaan, uitgevoerd bij 202 patiënten met recidiverend en refractair multipel myeloom, die na de laatste therapie ten minste twee eerdere behandelingslijnen met ziekteprogressie hebben ondergaan.
In de fase III-studie resulteerde behandeling met VELCADE bij alle patiënten, inclusief degenen die slechts één eerdere therapielijn hadden gekregen, in een significante verlenging van de tijd tot progressie, een significante verlenging van de overleving en een significante toename van het responspercentage. vergeleken met behandeling met dexamethason (zie tabel 14).
Op basis van de gegevens uit de "tussentijdse analyse De monitoringcommissie adviseerde vooraf geplande stopzetting van de behandeling met dexamethason ten gunste van behandeling met VELCADE voor alle patiënten die waren gerandomiseerd naar behandeling met dexamethason, ongeacht de ziektestatus. Vanwege deze vroege cross-over was de mediane duur van de follow-up bij levende patiënten 8,3 maanden. In de VELCADE-behandelarm was de algehele overleving langer en was het responspercentage hoger bij zowel patiënten die ongevoelig waren voor hun laatste therapie als degenen die dat niet deden.
Van de 669 patiënten die deelnamen, waren 245 (37%) 65 jaar of ouder. Zowel responsparameters als TTP waren significant beter voor VELCADE, ongeacht de leeftijd.Alle werkzaamheidsparameters (tijd tot progressie, algehele overleving en responspercentage) waren significant verbeterd in de VELCADE-arm, ongeacht de niveaus van b2-microglobuline bij baseline.
In de refractaire populatie van de Fase II-studie werden de reacties beoordeeld door een onafhankelijke commissie en de toegepaste responscriteria zijn vastgesteld. door de European Bone Marrow Transplant Group. De gemiddelde algehele overleving van alle patiënten die deelnamen aan het onderzoek was 17 maanden (bereik Performance Status, door de deletiestatus van chromosoom 13, of door het aantal of type eerdere therapieën. Het responspercentage van patiënten die al 2-3 of meer dan 7 behandelingslijnen was het respectievelijk 32% (10/32) en 31% (21/67).
Tabel 14: Samenvatting van de werkzaamheidsresultaten van fase III- (APEX) en II-onderzoeken
In de fase II-studie werden patiënten die geen optimale respons bereikten op VELCADE-monotherapie, behandeld met hoge doses dexamethason en VELCADE. Dankzij het protocol konden patiënten die een minder dan optimale respons bereikten op VELCADE-monotherapie dexamethason krijgen.
In totaal werden 74 evalueerbare patiënten behandeld met dexamethason en VELCADE. Door de gecombineerde behandeling kon bij 18% van de patiënten een respons of een verbetering van de respons [MR 11% of PR 7%] worden verkregen.
Klinische werkzaamheid bij patiënten met recidiverend/refractair multipel myeloom bij subcutane toediening van VELCADE
Een non-inferioriteit, open-label, gerandomiseerde klinische fase III-studie vergeleek de werkzaamheid en veiligheid van subcutane toediening van VELCADE versus intraveneuze toediening. Deze studie omvatte 222 patiënten met recidiverend/refractair multipel myeloom, gerandomiseerd in een verhouding van 2: 1 om 1,3 mg/m² VELCADE subcutaan of intraveneus gedurende 8 cycli Voor die patiënten die geen optimale respons bereikten na 4 cycli op VELCADE alleen (minder dan Complete Response [CR]), 20 mg dexamethason op de dag van toediening van VELCADE en de dag erna Patiënten met baseline graad ≥ 2 perifere neuropathie of aantal bloedplaatjes
Deze studie voldeed aan de primaire doelstelling van non-inferioriteit, beoordeeld op responspercentage (CR + PR) na 4 cycli van VELCADE-monotherapie voor zowel subcutane als intraveneuze toedieningsroutes, met een responspercentage van 42% in beide. gerelateerd aan respons en tijd tot gebeurtenis vertoonden consistente resultaten voor zowel de subcutane als de intraveneuze routes (Tabel 15).
Tabel 15: Samenvatting van werkzaamheidsanalyses die subcutane en intraveneuze toedieningen van VELCADE . vergelijken
Behandeling met VELCADE in combinatie met gepegyleerd liposomaal doxorubicine (onderzoek DOXIL-MMY-3001)
Een open-label, gerandomiseerde fase III multicenter studie met parallelle groepen werd uitgevoerd bij 646 patiënten waarbij de veiligheid en werkzaamheid van VELCADE plus gepegyleerd liposomaal doxorubicine versus VELCADE monotherapie werden vergeleken bij patiënten met multipel myeloom die in het verleden ten minste 1 therapie hadden gekregen en die geen ziekteprogressie getoond tijdens antracyclinetherapie. Het primaire werkzaamheidseindpunt was tijd tot progressie (TTP), terwijl de secundaire werkzaamheidseindpunten de totale overleving (OS) en het totale responspercentage (ORR: (complete respons + partiële respons) waren volgens de criteria van de "Europese groep voor bloed en merg Transplantatie (EBMT).
De resultaten van de "tussentijdse analyse protocol-gedefinieerd (gebaseerd op 249 TTP-gebeurtenissen) leidde tot vroegtijdige beëindiging van de studie voor werkzaamheid. Deze tussentijdse analyse toonde een risicoreductie van 45% van TTP (95% BI; 29-57%, p
De uiteindelijke analyse voor totale overleving (OS) uitgevoerd na een mediane follow-up van 8,6 jaar toonde geen significant verschil in OS tussen de twee behandelingsarmen De mediane OS was 30,8 maanden (95% BI; 25,2-36,5 maanden) voor patiënten op VELCADE monotherapie en 33,0 maanden (95% BI; 28,9-37,1 maanden) voor patiënten op combinatietherapie met VELCADE en gepegyleerd liposomaal doxorubicine.
Behandeling met VELCADE in combinatie met dexamethason
Bij gebrek aan een directe vergelijking tussen VELCADE en VELCADE in combinatie met dexamethason bij patiënten met voortschrijdend multipel myeloom, werd een "gepaarde statistische analyse" uitgevoerd om de resultaten te vergelijken van de niet-gerandomiseerde arm van VELCADE in combinatie met dexamethason (studie Fase II open label MMY-2045), met resultaten verkregen in de VELCADE-behandelingsarmen voor monotherapie uit verschillende gerandomiseerde fase III-onderzoeken (M34101-039 [APEX] en DOXIL MMY-3001) voor dezelfde indicatie.
Matched-Pair Analyse is een statistische methode waarbij patiënten in de onderzochte behandelgroep (bijv. VELCADE in combinatie met dexamethason) en patiënten in de vergelijkingsgroep (bijv. VELCADE) vergelijkbaar zijn met betrekking tot verstorende factoren door individuele paring van proefpersonen. Deze methode minimaliseert de effecten van verstorende factoren die worden waargenomen bij het schatten van behandelingseffecten met behulp van niet-gerandomiseerde gegevens.
127 gepaarde patiëntparen werden geïdentificeerd. De analyse toonde een verbetering in het totale responspercentage (ORR: CR + PR) (odds ratio 3.769; 95% CI 2.045-6.947; p
Er is beperkte informatie beschikbaar over herbehandeling met VELCADE bij recidiverend multipel myeloom.
De Fase II MMY-2036 (RETRIEVE), eenarmige open-labelstudie werd uitgevoerd om de werkzaamheid en veiligheid van herbehandeling met VELCADE te bepalen Honderddertig patiënten (leeftijd ≥ 18 jaar) met multipel myeloom die eerder ten minste één partiële respons op een regime dat VELCADE bevatte werd na progressie opnieuw verminderd Ten minste 6 maanden na eerdere therapie werd VELCADE gestart met de laatst getolereerde dosis van 1,3 mg/m² (n = 93) of ≤ 1,0 mg/m² (n = 37) en toegediend op dag 1, 4, 8 en 11 elke 3 weken gedurende maximaal 8 cycli, hetzij als monotherapie of in combinatie met dexamethason volgens de standaardbehandeling. Dexamethason werd in combinatie met VELCADE toegediend aan 83 patiënten in cyclus 1 en nog eens 11 patiënten kregen dexamethason tijdens de volgende VELCADE-herbehandelingscycli.
Het primaire eindpunt was de best bevestigde respons op herbehandeling volgens de EBMT-criteria. Het beste totale responspercentage (CR + PR) voor herbehandeling bij 130 patiënten was 38,5% (95%-BI: 30,1; 47)., 4).
Klinische werkzaamheid bij niet eerder behandelde patiënten met mantelcellymfoom (MCL)
LYM-3002 is een gerandomiseerde, open-label fase III-studie waarin de werkzaamheid en veiligheid van de combinatie van VELCADE, rituximab, cyclofosfamide, doxorubicine en prednison (VcR-CAP; n = 243) worden vergeleken met die van rituximab. cyclofosfamide, doxorubicine, vincristine en prednison (R-CHOP; n = 244) bij niet eerder behandelde volwassen patiënten met MCL (stadium II, III of IV). Patiënten in de VcR-CAP-behandelarm kregen VELCADE (1,3 mg/m²; op dag 1, 4, 8, 11, rustperiode 12-21), rituximab 375 mg/m² IV op dag 1; cyclofosfamide 750 mg/m² IV op dag 1; doxorubicine 50 mg/m² IV op dag 1 en prednison 100 mg/m² oraal op dag 1 tot 5 van de 21-daagse VELCADE-behandelingscyclus. Patiënten met een gedocumenteerde eerste respons op cyclus 6 kregen nog twee behandelingskuren.
Het primaire werkzaamheidseindpunt was de progressievrije overleving op basis van een beoordeling door de Independent Review Committee (IRC). Secundaire eindpunten waren onder meer tijd tot progressie (TTP), tijd tot de volgende antilymfoombehandeling (TNT), duur van het "behandelingsvrije interval (TFI). ), totale responspercentage (ORR) en complete responspercentage (CR/CRu), algehele overleving (OS) en duur van de respons.
Demografische kenmerken en ziektekenmerken bij baseline waren over het algemeen goed in evenwicht tussen de twee behandelingsarmen: de mediane leeftijd van de patiënten was 66 jaar, 74% was man, 66% was blank en 32% Aziatisch, 69% van de patiënten had positieve beenmergaspiraat en / of MCL-positieve beenmergbiopsie, had 54% van de patiënten een International Prognostic Index (IPI)-score ≥ 3 en had 76% stadium IV-ziekte. De duur van de behandeling (mediaan = 17 weken) en de duur van de follow-up (mediaan = 40 maanden) waren vergelijkbaar in beide behandelarmen. Patiënten in beide behandelarmen kregen een mediaan van 6 cycli, waarbij 14% van de proefpersonen in de VcR-CAP-groep en 17% van de patiënten in de R-CHOP-groep de extra 2 cycli kregen. De meeste patiënten in beide groepen voltooiden de behandeling, 80% in de VcR-CAP-groep en 82% in de R-CHOP-groep. De werkzaamheidsresultaten worden weergegeven in Tabel 16:
Tabel 16: Werkzaamheidsresultaten van LYM-3002-onderzoek
De mediane PFS zoals bepaald door de onderzoeker was 30,7 maanden in de VcR-CAP-groep en 16,1 maanden in de R-CHOP-groep (Hazard Ratio [HR] = 0,51; p
De mediane duur van volledige respons was 42,1 maanden in de VcR-CAP-groep vergeleken met 18 maanden in de R-CHOP-groep. De totale responsduur was 21,4 maanden langer in de VcR-CAP-groep (mediaan 36,5 maanden versus 15,1 maanden in de R-CHOP-groep). Bij een mediane follow-upduur van 40 maanden was de mediane totale overleving (OS) in het voordeel van VcR-CAP (56,3 maanden in de R-CHOP-groep en niet bereikt in de VcR-CAP-groep), (HR-schatting = 0,80; p = 0,173). Er was een trend naar een langere algehele overleving in het voordeel van de VcR-CAP-groep; de geschatte 4-jaarsoverleving was 53,9% in de R-CHOP-groep en 64,4% in de VcR-CAP-groep.
Patiënten met eerder behandelde lichte keten (AL) amyloïdose
Er werd een open-label, niet-gerandomiseerde fase I/II-studie uitgevoerd om de veiligheid van VELCADE te bepalen bij patiënten met eerder behandelde amyloïdose van de lichte keten (AL). Tijdens het onderzoek werden geen nieuwe veiligheidsproblemen waargenomen en in het bijzonder leidde VELCADE niet tot verergering van orgaanschade (hart, nier en lever).
In een verkennende werkzaamheidsanalyse werd voor de twee geassocieerde dosiscohorten een responspercentage van 67,3% (waarvan 28,6% volledige respons) gerapporteerd in termen van hematologische respons (eiwit M), bij 49 evalueerbare patiënten die werden behandeld met de maximaal toegestane doses van 1,6 mg/m² eenmaal per week en 1,3 mg/m² tweemaal per week Voor de twee bijbehorende dosiskuren was de 1-jaarsoverleving 88,1%.
Pediatrische populatie
Het Europees Geneesmiddelenbureau heeft besloten af te zien van de verplichting om de resultaten in te dienen van onderzoek met VELCADE in alle subgroepen van pediatrische patiënten met multipel myeloom en mantelcellymfoom (zie rubriek 4.2 voor informatie over pediatrisch gebruik).
05.2 "Farmacokinetische eigenschappen -
Absorptie
Na intraveneuze bolustoediening van 1,0 mg/m² en 1,3 mg/m² aan 11 patiënten met multipel myeloom en creatinineklaringswaarden hoger dan 50 ml/min, waren de maximale gemiddelde plasmaconcentraties van bortezomib bij de eerste doses 57 en 112 ng/ml , respectievelijk. Bij volgende doses varieerden de gemiddelde maximale waargenomen plasmaconcentraties van 67 tot 106 ng/ml voor de dosis van 1,0 mg/m² en tussen 89 en 120 ng/ml voor de dosis van 1,3 mg/m².
Na herhaalde intraveneuze bolus- of subcutane injectie van een dosis van 1,3 mg/m² bij patiënten met multipel myeloom (n = 14 in de intraveneuze groep, n = 17 in de subcutane groep), was de totale systemische geneesmiddelblootstelling (AUClast) equivalent voor de subcutane en intraveneuze toedieningswegen Cmax na subcutane toediening (20,4 ng/ml) was lager dan intraveneuze (223 ng/ml) De geometrisch gemiddelde ratio AUC was 0,99 en met de 90%-betrouwbaarheidsintervallen waren ze 80,18% - 122,80%.
Verdeling
Bij patiënten met multipel myeloom varieerde het gemiddelde distributievolume (Vd) van bortezomib van 1659 tot 3294 l na enkelvoudige of herhaalde intraveneuze toediening van 1,0 mg/m² of 1,3 mg/m². Dit suggereert dat bortezomib wijd verspreid is in perifere weefsels. Bij een bortezomib-concentratiebereik van 0,01 tot 1,0 g/ml, binding aan humane plasma-eiwitten in vitro het bedroeg gemiddeld 82,9%. De plasma-eiwitgebonden fractie van bortezomib was niet concentratieafhankelijk.
Biotransformatie
Opleiding in vitro op humane levermicrosomen en op cytochroom P450 iso-enzymen tot expressie gebracht door humaan c-DNA geven aan dat bortezomib voornamelijk oxidatief wordt gemetaboliseerd via cytochroom P450-, 3A4-, 2C19- en 1A2-enzymen. De belangrijkste metabole route bestaat uit deboronatie, wat leidt tot twee gedeboroneerde metabolieten die vervolgens worden gehydroxyleerd tot verschillende metabolieten. De gedeboroneerde metabolieten van bortezomib zijn inactief als remmers van het 26S-proteasoom.
Eliminatie
De gemiddelde eliminatiehalfwaardetijd (t1/2) van bortezomib tijdens behandeling met meervoudige doses varieert van 40 tot 193 uur Bortezomib wordt sneller geklaard na de eerste dosis dan bij de volgende doses De gemiddelde totale klaring was 102 en 112 l/ h na de eerste dosis van respectievelijk 1,0 mg/m² en 1,3 mg/m² en tussen 15 en 32 l/h en tussen 18 en 32 l/h voor vervolgdoses van respectievelijk 1,0 mg/m² en 1,3 mg/m².
Speciale populaties
Leverinsufficiëntie
Het effect van leverinsufficiëntie op de farmacokinetiek van bortezomib werd onderzocht in een klinische fase I-studie bij 61 patiënten met primaire solide tumoren met verschillende gradaties van leverinsufficiëntie en behandeld met doseringen van bortezomib, waaronder tussen 0,5 en 1,3 mg/m².
Lichte leverinsufficiëntie veranderde de voor dosis genormaliseerde AUC van bortezomib niet in vergelijking met die gezien bij patiënten met een normale leverfunctie. De voor de dosis genormaliseerde gemiddelde AUC-waarden waren echter met ongeveer 60% verhoogd bij patiënten met een matige of ernstige leverfunctiestoornis. Een lagere startdosis wordt aanbevolen bij patiënten met een matige of ernstige leverfunctiestoornis. , en dergelijke patiënten moeten zorgvuldig worden gecontroleerd (zie paragraaf 4.2, Tabel 6).
Nierfalen
Er is een farmacokinetisch onderzoek uitgevoerd bij patiënten met verschillende gradaties van nierinsufficiëntie, die op basis van creatinineklaring (CrCL)-waarden werden ingedeeld in de volgende groepen: normaal (CrCL ≥60 ml/min/1,73 m², n = 12), mild ( CrCL = 40-59 ml / min / 1,73 m², n = 10), matig (CrCL = 20-39 ml / min / 1,73 m², n = 9) en ernstig (intraveneuze CrCL in doses variërend van 0,7 tot 1,3 mg / m² tweemaal per week Blootstelling aan VELCADE (dosis-genormaliseerde AUC en Cmax) was vergelijkbaar in alle patiëntengroepen (zie rubriek 4.2).
05.3 Gegevens uit het preklinisch veiligheidsonderzoek -
bij concentraties
Bortezomib toonde geen genotoxiciteit in de mutageniteitstest in vitro (Ames-test), noch in de micronucleus-test in vivo uitgevoerd bij muizen.
In ontwikkelingstoxiciteitsonderzoeken bij ratten en konijnen werd embryofoetale mortaliteit aangetoond bij maternale toxische doses, maar geen embryofoetale toxiciteit lager dan de maternale toxische dosis. Er zijn geen vruchtbaarheidsonderzoeken uitgevoerd, maar in algemene toxiciteitsonderzoeken is een evaluatie van de voortplantingsweefsels uitgevoerd. In de zes maanden durende studie bij ratten werden degeneratieve effecten op zowel de testikels als de eierstokken gevonden. Het is daarom waarschijnlijk dat bortezomib mogelijk een effect heeft op de mannelijke en vrouwelijke vruchtbaarheid. Er zijn geen onderzoeken naar de perinatale en postnatale ontwikkeling uitgevoerd.
Algemene toxiciteitsstudies met meerdere cycli uitgevoerd bij ratten en apen lieten zien dat de belangrijkste doelorganen waren: het maagdarmkanaal, resulterend in braken en/of diarree; hematopoëtische en lymfatische weefsels, resulterend in cytopenie in het perifere bloed, atrofie van het lymfatische weefsel en hematopoëtische hypocellulariteit van het beenmerg; perifere neuropathie (waargenomen bij apen, muizen en honden) die de axonen van de sensorische zenuwen aantasten; en kleine veranderingen in de nier. Na stopzetting van de behandeling vertoonden al deze doelorganen gedeeltelijk tot volledig herstel.
Op basis van dierstudies lijkt de passage van bortezomib door de bloed-hersenbarrière beperkt en de relevantie bij mensen is niet bekend.
Cardiovasculaire veiligheidsfarmacologische studies uitgevoerd bij apen en honden tonen aan dat intraveneuze toediening van mg/m2 doses 2 tot 3 maal de klinisch aanbevolen dosis resulteert in een verhoogde hartslag, verminderde hartcontractiliteit, hypotensie en overlijden. Bij honden werden verminderde hartcontractiliteit en hypotensie onder controle gebracht door acute behandeling met positieve inotrope middelen of vasopressoren en werd een lichte toename van het gecorrigeerde QT-interval waargenomen.
06.0 FARMACEUTISCHE INFORMATIE -
06.1 Hulpstoffen -
Mannitol (E421)
Stikstof
06.2 Incompatibiliteit "-
Dit geneesmiddel mag niet worden gemengd met andere producten dan die vermeld in rubriek 6.6.
06.3 Geldigheidsduur "-
ongeopende flacon
3 jaar.
Gereconstitueerde oplossing
De gereconstitueerde oplossing moet onmiddellijk na bereiding worden gebruikt.
Indien het niet onmiddellijk wordt gebruikt, is het de verantwoordelijkheid van de gebruiker om zich voor gebruik aan de voorwaarden en bewaartermijnen van het geneesmiddel te houden.
De fysische en chemische stabiliteit van de gereconstitueerde oplossing is echter aangetoond gedurende 8 uur bij 25°C indien bewaard in de originele injectieflacon en/of in een injectiespuit. De totale bewaartijd van het gereconstitueerde geneesmiddel vóór toediening mag niet langer zijn dan 8 uur.
06.4 Speciale voorzorgsmaatregelen bij bewaren -
Bewaren bij een temperatuur van maximaal 30 ° C.
Bewaar de injectieflacon in de buitenverpakking om het geneesmiddel tegen licht te beschermen.
Voor de bewaarcondities na reconstitutie van het geneesmiddel, zie rubriek 6.3.
06.5 Aard van de primaire verpakking en inhoud van de verpakking -
Type I glazen injectieflacon van 10 ml, met een grijze broombutyl stop en een aluminium verzegeling, met een koningsblauwe dop bevat 3,5 mg bortezomib.
De injectieflacon zit in een transparante blister die bestaat uit een bakje met een deksel.
Elke verpakking bevat 1 injectieflacon voor eenmalig gebruik.
06.6 Instructies voor gebruik en verwerking -
Algemene voorzorgsmaatregelen
Bortezomib is een cytotoxisch middel. Daarom moet speciale aandacht worden besteed aan het hanteren en bereiden van VELCADE. Het wordt aanbevolen om handschoenen en andere beschermende kleding te dragen om contact met de huid te voorkomen.
De hantering van VELCADE moet gebeuren met strikte naleving van aseptische technieken vanwege de afwezigheid van conserveermiddelen.
Er zijn gevallen van overlijden geweest na onbedoelde intrathecale toediening van VELCADE. VELCADE 1 mg poeder voor oplossing voor injectie is alleen voor intraveneus gebruik, terwijl VELCADE 3,5 mg poeder voor oplossing voor injectie bedoeld is voor intraveneus of subcutaan gebruik VELCADE mag niet intrathecaal worden toegediend.
Instructies voor reconstitutie
VELCADE moet worden gereconstitueerd door een beroepsbeoefenaar in de gezondheidszorg.
Intraveneuze injectie
Elke injectieflacon van 10 ml met VELCADE 3.5 poeder voor oplossing voor injectie moet worden gereconstitueerd met 3,5 ml natriumchloride 9 mg/ml (0,9%) oplossing voor injectie. Het oplossen van het gevriesdroogde poeder duurt minder dan 2 minuten. Na reconstitutie bevat elke ml oplossing 1 mg bortezomib. De gereconstitueerde oplossing is helder en kleurloos, met een uiteindelijke pH tussen 4 en 7. De gereconstitueerde oplossing moet vóór toediening visueel worden geïnspecteerd om te controleren op deeltjes of verkleuring. In aanwezigheid van deeltjes of verandering van kleur. oplossing mag niet worden gebruikt en moet worden weggegooid.
Subcutane injectie
Elke injectieflacon van 10 ml met VELCADE 3.5 poeder voor oplossing voor injectie moet worden gereconstitueerd met 1,4 ml natriumchloride 9 mg/ml (0,9%) oplossing voor injectie. Het oplossen van het gevriesdroogde poeder duurt minder dan 2 minuten. Na reconstitutie bevat elke ml oplossing 2,5 mg bortezomib. De gereconstitueerde oplossing is helder en kleurloos, met een uiteindelijke pH tussen 4 en 7. De gereconstitueerde oplossing moet vóór toediening visueel worden geïnspecteerd om te controleren op deeltjes of verkleuring. In aanwezigheid van deeltjes of verandering van kleur. oplossing mag niet worden gebruikt en moet worden weggegooid.
Beschikbaarheid
VELCADE is uitsluitend voor eenmalig gebruik.
Ongebruikte medicijnen en afval van dit medicijn moeten worden vernietigd in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE "VERGUNNING VOOR HET IN DE HANDEL BRENGEN" -
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 Beerse
België
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN -
EU / 1/04/274/001
036559019
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING -
Datum eerste vergunning: 26 april 2004
Datum van de laatste verlenging van de vergunning: 26 april 2014
10.0 DATUM VAN HERZIENING VAN DE TEKST -
04/2015