Actieve ingrediënten: Denosumab
XGEVA 120 mg oplossing voor injectie
Waarom wordt Xgeva gebruikt? Waar is het voor?
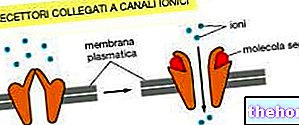
XGEVA bevat denosumab, een eiwit (monoklonaal antilichaam) dat de botafbraak vermindert die wordt veroorzaakt door de verspreiding van kanker naar het bot (botmetastasen) of reuscelkanker van het bot.
XGEVA wordt gebruikt bij volwassenen met kanker om ernstige complicaties veroorzaakt door botmetastasen te voorkomen (bijv. fracturen, druk op het beenmerg of de noodzaak van bestralingstherapie of chirurgie). XGEVA wordt ook gebruikt voor de behandeling van reuscelkanker van het bot, dat niet operatief kan worden behandeld of waarbij een operatie niet de beste optie is, bij volwassenen en adolescenten bij wie de botten niet meer groeien.
Contra-indicaties Wanneer Xgeva niet mag worden gebruikt
Gebruik XGEVA niet
- als u allergisch bent voor denosumab of voor één van de andere bestanddelen van XGEVA.
Uw beroepsbeoefenaar in de gezondheidszorg zal u XGEVA niet geven als u een zeer laag calciumgehalte in uw bloed heeft dat niet is behandeld.
Uw beroepsbeoefenaar in de gezondheidszorg zal u XGEVA niet geven als u wonden heeft die niet zijn genezen door tandheelkundige of kaakchirurgie.
Voorzorgen bij gebruik Wat u moet weten voordat u Xgeva inneemt
Calcium- en vitamine D-supplement
U moet calcium- en vitamine D-supplementen innemen terwijl u met XGEVA wordt behandeld, tenzij uw bloedcalciumspiegels hoog zijn. Uw arts zal dit met u bespreken. Als uw bloedcalciumspiegel laag is, kan uw arts besluiten u calciumsupplementen te geven voordat de behandeling met XGEVA wordt gestart.
Lage calciumspiegels in het bloed
Vertel het uw arts onmiddellijk als u last krijgt van spierspasmen, spiertrekkingen of krampen en/of gevoelloosheid of tintelingen in de vingers en tenen of rond de mond en/of epileptische aanvallen, verwardheid of bewustzijnsverlies terwijl u XGEVA gebruikt. Mogelijk heeft u een laag calciumgehalte in het bloed.
Vertel het uw arts als u ernstige nierproblemen of nierinsufficiëntie heeft of ooit heeft gehad, of als u dialyse ondergaat, aangezien dit het risico op een laag calciumgehalte in het bloed kan verhogen, vooral als u geen calciumsupplementen gebruikt.
Problemen met uw mond, tanden of kaak
Een bijwerking genaamd osteonecrose van de kaak (ernstige botdegeneratie van de kaak) is vaak gemeld (kan voorkomen bij maximaal 1 op de 10 mensen) bij patiënten die XGEVA-injecties kregen voor kankergerelateerde aandoeningen.
Osteonecrose van de kaak kan ook optreden na het stoppen van de behandeling.
Het is belangrijk om te proberen de ontwikkeling van osteonecrose van de kaak te voorkomen, aangezien het een pijnlijke aandoening is die moeilijk te behandelen kan zijn.Om het risico op het ontwikkelen van osteonecrose van de kaak te verminderen, moet u bepaalde voorzorgsmaatregelen nemen.
Vertel uw arts/verpleegkundige (beroepsbeoefenaar in de gezondheidszorg) voordat u behandeld wordt als u problemen heeft met uw mond of tanden. Uw arts moet de start van de behandeling uitstellen als u wonden in uw mond heeft die niet zijn genezen door tandheelkundige ingrepen of kaakchirurgie.Uw arts kan u vragen om een tandheelkundig onderzoek te ondergaan voordat u met de behandeling met XGEVA begint.
Tijdens de behandeling is het noodzakelijk om een goede mondhygiëne te behouden en periodieke tandheelkundige controles te ondergaan. Als u prothesen draagt, moet u ervoor zorgen dat deze correct worden ingebracht.
Als u een tandheelkundige behandeling ondergaat of van plan bent een tandheelkundige ingreep te ondergaan (bijv. het trekken van tanden), informeer dan uw tandheelkundige behandelend arts en vertel uw tandarts dat u wordt behandeld met XGEVA.
Neem onmiddellijk contact op met uw arts en tandarts als u problemen met uw mond of tanden opmerkt, zoals tandenzwaaien, pijn of zwelling, of niet-genezende zweertjes in de mond of afscheiding, aangezien dit tekenen kunnen zijn van osteonecrose van de onderkaak/maxilla .
Patiënten die chemotherapie en/of radiotherapie ondergaan, die steroïden of anti-angiogene geneesmiddelen (gebruikt om kanker te behandelen), die een tandheelkundige ingreep ondergaan, die geen routinematige tandheelkundige zorg krijgen of die last hebben van tandvlees, rokers zijn, kunnen een hoger risico op het ontwikkelen van osteonecrose van de kaak.
Ongebruikelijke fracturen van het dijbeen
Sommige mensen hebben ongewone fracturen in het dijbeen gekregen tijdens de behandeling met XGEVA. Neem contact op met uw arts als u nieuwe of ongebruikelijke pijn in uw heup, lies of dij krijgt.
Kinderen en adolescenten
XGEVA wordt niet aanbevolen voor kinderen en adolescenten jonger dan 18 jaar, behalve voor adolescenten met een reusceltumor van het bot bij wie de botten niet meer groeien.Het gebruik van XGEVA bij kinderen en adolescenten met andere tumoren die het bot zijn binnengedrongen, is niet onderzocht.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Xgeva . veranderen?
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt of kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken. Dit geldt ook voor geneesmiddelen die u zonder voorschrift kunt krijgen. Het is met name belangrijk dat u uw arts vertelt als u
- een ander geneesmiddel dat denosumab . bevat
- een bisfosfonaat.
U mag XGEVA niet gebruiken samen met andere geneesmiddelen die denosumab of bisfosfonaten bevatten
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
XGEVA is niet onderzocht bij zwangere vrouwen. Het is belangrijk dat u uw arts vertelt als u zwanger bent, vermoedt of van plan bent zwanger te worden. Het gebruik van XGEVA wordt niet aanbevolen als u zwanger bent Vrouwen die zwanger kunnen worden, moeten effectieve anticonceptie gebruiken tijdens het gebruik van XGEVA en gedurende ten minste 5 maanden na het stoppen met XGEVA.
Als u zwanger wordt tijdens de behandeling met XGEVA of minder dan 5 maanden na het stoppen van de behandeling met XGEVA, neem dan contact op met uw arts. Ze wordt aangemoedigd om zich in te schrijven voor het zwangerschapssurveillanceprogramma van Amgen. Details van de lokale Amgen-vertegenwoordiger worden gegeven in rubriek 6 van deze bijsluiter.
Het is niet bekend of XGEVA wordt uitgescheiden in de moedermelk. Het is belangrijk dat u uw arts vertelt als u borstvoeding geeft of van plan bent borstvoeding te geven. Uw arts zal u dan helpen beslissen of u moet stoppen met het geven van borstvoeding of met het gebruik van XGEVA, waarbij het voordeel van borstvoeding voor het kind en het voordeel van het gebruik van XGEVA voor de moeder in overweging moeten worden genomen.
Als u borstvoeding geeft terwijl u XGEVA gebruikt, informeer dan uw arts. Ze wordt aangemoedigd om zich in te schrijven voor Amgen's Lactation Surveillance Program Details over uw lokale Amgen-vertegenwoordiger vindt u in rubriek 6 van deze bijsluiter.
Vraag uw arts of apotheker om advies voordat u dit geneesmiddel gebruikt.
Rijvaardigheid en het gebruik van machines
XGEVA heeft geen of een verwaarloosbare invloed op de rijvaardigheid of op het vermogen om machines te bedienen.
XGEVA bevat sorbitol
Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt, aangezien het sorbitol (E420) bevat.
XGEVA bevat natrium
Dit geneesmiddel bevat minder dan 1 mmol natrium (23 mg) per 120 mg, dat wil zeggen dat het in wezen "natriumvrij" is.
Dosis, wijze en tijdstip van toediening Hoe Xgeva te gebruiken: Dosering
De aanbevolen dosis XGEVA is 120 mg eenmaal per 4 weken toegediend als een enkele injectie onder de huid (subcutaan). XGEVA wordt geïnjecteerd in de dij, buik of bovenarm Als u wordt behandeld voor reuscelkanker van het bot, krijgt u 1 week en 2 weken na de eerste dosis een extra dosis.
XGEVA moet worden toegediend onder de verantwoordelijkheid van een beroepsbeoefenaar in de gezondheidszorg.
Schud niet te veel.
Tijdens de behandeling met XGEVA moet u ook calcium- en vitamine D-supplementen innemen.Uw arts zal dit met u bespreken.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts, apotheker of verpleegkundige.
Bijwerkingen Wat zijn de bijwerkingen van Xgeva
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Vertel het uw arts onmiddellijk als u een van deze symptomen opmerkt tijdens het gebruik van XGEVA:
- spiertrekkingen, spiertrekkingen, gevoelloosheid of tintelingen in de vingers en tenen of rond de mond en/of toevallen, verwardheid of bewustzijnsverlies. Deze tekenen kunnen wijzen op een laag calciumgehalte in het bloed. Lage bloedcalciumspiegels kunnen ook leiden tot een verandering in het hartritme, QT-verlenging genaamd, die wordt gezien op elektrocardiografie (ECG).
Vertel het uw arts en tandarts onmiddellijk als u een van deze symptomen ervaart tijdens de behandeling met XGEVA of na het stoppen van de behandeling met XGEVA:
- pijn in de mond en/of kaak, zwelling of niet-genezende zweren in de mond of kaak, afscheiding, gevoelloosheid of een zwaar gevoel in de kaak, of wiebelen van een tand, aangezien deze tekenen kunnen wijzen op ernstige botdegeneratie van de kaak ( osteonecrose).
Zeer vaak voorkomende bijwerkingen (kunnen voorkomen bij meer dan 1 op de 10 mensen):
- pijn in de botten, gewrichten en/of spieren, soms hevig,
- piepende ademhaling (dyspneu),
- diarree.
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 mensen):
- laag calciumgehalte in het bloed (hypocalciëmie),
- laag fosfaatgehalte in het bloed (hypofosfatemie),
- aanhoudende pijn en/of niet-genezing van zweren in de mond of kaak (osteonecrose van de kaak),
- tand extractie,
- overmatig zweten.
Zelden voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 1.000 mensen):
- allergische reacties (bijv.piepende ademhaling of moeite met ademhalen; zwelling van het gezicht, lippen, tong, keel of andere delen van het lichaam; huiduitslag, jeuk of netelroos op de huid). In zeldzame gevallen kunnen allergische reacties ernstig zijn.
- nieuwe of ongebruikelijke pijn in de heup, lies of dij (dit kan een vroeg teken zijn van een mogelijke dijbeenbreuk).
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of verpleegkundige. Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V. Door bijwerkingen te melden, kunt u helpen meer informatie geven over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de vervaldatum die staat vermeld op het etiket en de doos na EXP De vervaldatum verwijst naar de laatste dag van die maand.
Bewaren in de koelkast (2 ° C - 8 ° C).
Niet bevriezen.
Bewaren in de oorspronkelijke verpakking om het geneesmiddel tegen licht te beschermen.
De injectieflacon kan vóór injectie buiten de koelkast worden bewaard om op kamertemperatuur (tot 25°C) te komen.Dit zal de injectie comfortabeler maken. Zodra de injectieflacon op kamertemperatuur is gekomen (tot 25°C), moet deze binnen 30 dagen worden gebruikt.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Deadline "> Overige informatie
Wat bevat XGEVA
- Het werkzame bestanddeel is denosumab. Elke injectieflacon bevat 120 mg in 1,7 ml oplossing (overeenkomend met 70 mg/ml).
- De andere stoffen in dit middel zijn ijsazijn, natriumhydroxide, sorbitol (E420) en water voor injecties.
Beschrijving van hoe XGEVA eruit ziet en de inhoud van het pakket
XGEVA is een oplossing voor injectie in een injectieflacon.
Elke verpakking bevat één, drie of vier injectieflacons.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
XGEVA is een heldere, kleurloze tot lichtgele oplossing. Het kan sporen van heldere tot witte deeltjes bevatten.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL -
XGEVA 120 MG OPLOSSING VOOR INJECTIE
▼ Geneesmiddel onderworpen aan aanvullende monitoring. Dit zal de snelle identificatie van nieuwe veiligheidsinformatie mogelijk maken. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor informatie over het melden van bijwerkingen.
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING -
Elke injectieflacon bevat 120 mg denosumab in 1,7 ml oplossing (70 mg/ml).
Denosumab is een humaan IgG2-type monoklonaal antilichaam geproduceerd in een zoogdiercellijn (CHO) door middel van recombinant-DNA-technologie.
Hulpstof(fen) met bekend effect
Elke 1,7 ml oplossing bevat 78 mg sorbitol (E420).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM -
Oplossing voor injectie (injectie).
Heldere, kleurloze tot lichtgele oplossing die sporen van doorschijnende tot witte eiwitdeeltjes kan bevatten.
04.0 KLINISCHE INFORMATIE -
04.1 Therapeutische indicaties -
Preventie van skeletgerelateerde voorvallen (pathologische fracturen, radiotherapie van het bot, compressie van het ruggenmerg of botchirurgie) bij volwassenen met botmetastasen van solide tumoren.
Behandeling van volwassen en adolescenten met een volgroeid skelet met een reusceltumor van het bot die niet reseceerbaar is of bij wie chirurgische resectie ernstige morbiditeit zou kunnen veroorzaken.
04.2 Dosering en wijze van toediening -
XGEVA moet worden toegediend onder de verantwoordelijkheid van een beroepsbeoefenaar in de gezondheidszorg.
Dosering
Suppletie van ten minste 500 mg calcium en 400 IE vitamine D per dag is vereist bij alle patiënten behalve hypercalciëmie (zie rubriek 4.4).
Patiënten die met XGEVA worden behandeld, dienen de bijsluiter en de herinneringskaart voor de patiënt te krijgen.
Preventie van skeletgerelateerde voorvallen bij volwassenen met botmetastasen van solide tumoren
De aanbevolen dosis is 120 mg toegediend als een enkelvoudige subcutane injectie, eenmaal per 4 weken in de dij, buik of bovenarm.
Reusceltumor van bot
De aanbevolen dosis XGEVA is 120 mg, gegeven als een enkelvoudige subcutane injectie, eenmaal per 4 weken in de dij, buik of bovenarm, met aanvullende doses van 120 mg op dag 8 en 15 van de behandeling in de eerste maand van de behandeling.
Patiënten in de fase II-studie die een volledige resectie van een reusceltumor van het bot ondergingen, kregen na de operatie nog eens 6 maanden behandeling volgens het onderzoeksprotocol.
Patiënten met een reusceltumor van het bot moeten met regelmatige tussenpozen worden geëvalueerd om te bepalen of ze nog steeds baat hebben bij de behandeling.Bij patiënten bij wie de ziekte onder controle wordt gehouden door XGEVA, is het effect van het stoppen of stoppen van de behandeling niet geëvalueerd, maar er zijn beperkte gegevens over deze patiënten wijzen niet op een rebound-effect na stopzetting van de behandeling.
Patiënten met nierinsufficiëntie
Er is geen dosisaanpassing nodig bij patiënten met nierinsufficiëntie (zie rubrieken 4.4 voor aanbevelingen voor het controleren van calciumspiegels, 4.8 en 5.2).
Patiënten met leverinsufficiëntie
De veiligheid en werkzaamheid van denosumab zijn niet onderzocht bij patiënten met een leverfunctiestoornis (zie rubriek 5.2).
Oudere patiënten (leeftijd ≥ 65 jaar)
Bij oudere patiënten is geen dosisaanpassing nodig (zie rubriek 5.2).
Pediatrische populatie
De veiligheid en werkzaamheid van XGEVA zijn niet vastgesteld bij pediatrische patiënten (leeftijd
XGEVA wordt niet aanbevolen bij pediatrische patiënten (leeftijd
Behandeling van adolescenten met een volgroeid skelet met inoperabele reusceltumor van het bot of bij wie chirurgische resectie ernstige morbiditeit zou kunnen veroorzaken: de dosering is dezelfde als voor volwassenen.
In dierstudies is remming van RANK/RANK-ligand (RANKL) in verband gebracht met remming van botgroei en het uitblijven van doorbraak en deze veranderingen waren gedeeltelijk reversibel na stopzetting van de RANKL-remming (zie paragraaf 5.3).
Wijze van toediening
Voor onderhuids gebruik.
Voor instructies over gebruik, verwerking en verwijdering, zie rubriek 6.6.
04.3 Contra-indicaties -
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
Ernstige, onbehandelde hypocalciëmie (zie rubriek 4.4).
Verwondingen die niet genezen zijn door tandheelkundige of kaakchirurgie.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik -
Calcium- en vitamine D-supplement
Het is belangrijk dat alle patiënten voldoende calcium en vitamine D binnenkrijgen, behalve in geval van hypercalciëmie (zie rubriek 4.2).
Hypocalciëmie
Reeds bestaande hypocalciëmie moet worden gecorrigeerd voordat de behandeling met XGEVA wordt gestart.
Hypocalciëmie kan op elk moment tijdens de behandeling met XGEVA optreden In geval van vermoede symptomen van hypocalciëmie dient de calciumspiegel te worden gecontroleerd vóór de aanvangsdosis van XGEVA, binnen twee weken na de aanvangsdosis (zie rubriek 4.8 voor de lijst met symptomen). . Bij patiënten met risicofactoren voor hypocalciëmie, of zoals anders aangegeven op basis van de klinische toestand van de patiënt, moet tijdens de behandeling aanvullende controle van de calciumspiegels worden overwogen.
Patiënten moeten worden aangemoedigd om symptomen te melden die wijzen op hypocalciëmie. Als zich hypocalciëmie ontwikkelt tijdens de toediening van XGEVA, zijn aanvullende calciumsupplementen en aanvullende monitoring vereist.
Tijdens postmarketinggebruik is ernstige symptomatische hypocalciëmie (inclusief gevallen met dodelijke afloop) gemeld (zie rubriek 4.8), waarbij de meeste gevallen binnen de eerste weken na het starten van de therapie optraden, maar later kunnen optreden.
Nierfunctiestoornis
Patiënten met een ernstige nierfunctiestoornis (dialyse van de creatinineklaring hebben een verhoogd risico op het ontwikkelen van hypocalciëmie. Het risico op het ontwikkelen van hypocalciëmie en de daaruit voortvloeiende verhogingen van de parathyroïdhormoonspiegels neemt toe met toenemende mate van nierfunctiestoornis. Regelmatige controle van de niveaus van nierziekte. Calcium is vooral belangrijk bij deze patiënten.
Osteonecrose van de kaak (ONJ)
ONJ is vaak gemeld bij patiënten die XGEVA kregen (zie rubriek 4.8).
Het starten van de behandeling/nieuwe behandeling moet worden uitgesteld bij patiënten met niet-genezen, open laesies van zacht weefsel in de mond. Voorafgaand aan de behandeling met XGEVA wordt een tandheelkundig onderzoek met tandheelkundige profylaxe en een individuele baten/risicobeoordeling aanbevolen.
De volgende risicofactoren moeten in overweging worden genomen bij het evalueren van het risico van een patiënt om ONJ te ontwikkelen:
• de potentie van het geneesmiddel dat botresorptie remt (het risico is hoger bij krachtigere geneesmiddelen), de toedieningsweg (het risico is hoger bij parenterale toediening) en de cumulatieve dosis van botresorptietherapie.
• tumor, comorbiditeit (bijv. anemie, coagulopathieën, infectie), roken.
• gelijktijdige therapieën: corticosteroïden, chemotherapie, angiogeneseremmers, radiotherapie van het hoofd-halsgebied.
• slechte mondhygiëne, parodontitis, verkeerd geplaatste gebitsprothesen, reeds bestaande tandheelkundige aandoeningen, invasieve tandheelkundige ingrepen (bijv. tandextracties).
Alle patiënten moeten worden aangemoedigd om een goede mondhygiëne te behouden, periodieke tandheelkundige controles te ondergaan en onmiddellijk alle orale symptomen te melden, zoals tandmobiliteit, pijn of zwelling of niet-genezende zweertjes in de mond of de aanwezigheid van afscheidingen tijdens de behandeling. . Tijdens de behandeling mogen invasieve tandheelkundige ingrepen alleen worden uitgevoerd na zorgvuldige overweging en moeten worden vermeden in de nabijheid van de toediening van XGEVA.
De behandeling van patiënten die ONJ ontwikkelen, moet gebeuren in nauwe samenwerking tussen de behandelend arts en een tandarts of kaakchirurg die ervaring heeft met de behandeling van ONJ. Tijdelijke onderbreking van de behandeling met XGEVA moet worden overwogen totdat de aandoening is verdwenen en, waar mogelijk, om de risicofactoren die hebben bijgedragen aan het ontstaan ervan te verminderen.
Atypische fracturen van het dijbeen
Gevallen van atypische femurfracturen zijn gemeld bij patiënten die werden behandeld met XGEVA (zie rubriek 4.8). Atypische femurfracturen kunnen optreden met minimaal of geen trauma in de subtrochantere en diafysaire gebieden van het dijbeen. Deze gebeurtenissen worden gekenmerkt door specifieke radiografische bevindingen. Atypische femurfracturen zijn ook gemeld bij patiënten met een aantal comorbide aandoeningen (bijv. vitamine D-tekort, reumatoïde artritis, hypofosfatasie) en bij het gebruik van bepaalde medicijnen (bijv. bisfosfonaten, glucocorticoïden, protonpompremmers). Deze voorvallen traden ook op in afwezigheid van antiresorptieve therapie. Vergelijkbare fracturen, gemeld in verband met het gebruik van bisfosfonaten, zijn vaak bilateraal; daarom moet het contralaterale dijbeen worden geëvalueerd bij met denosumab behandelde patiënten die een femurschachtfractuur hebben opgelopen. Bij patiënten met een vermoedelijke atypische femurfractuur moet worden overwogen de behandeling met XGEVA, in afwachting van evaluatie van de patiënt op basis van een individuele baten/risico-analyse Tijdens de behandeling met XGEVA moeten patiënten worden geadviseerd nieuwe of ongebruikelijke pijn in de dij, heup of lies te melden. Patiënten die dergelijke symptomen vertonen, moeten worden onderzocht op een onvolledige femurfractuur.
Patiënten met een groeiend skelet
XGEVA wordt niet aanbevolen bij patiënten met groeiende skeletsystemen (zie rubriek 4.2). Klinisch significante hypercalciëmie is gemeld bij patiënten met groeiende skeletsystemen die werden behandeld met XGEVA na weken tot maanden stopzetting van de behandeling.
anderen
Patiënten die worden behandeld met XGEVA mogen niet gelijktijdig worden behandeld met andere denosumab-bevattende geneesmiddelen (voor indicaties van osteoporose).
Patiënten die met XGEVA worden behandeld, mogen niet gelijktijdig met bisfosfonaten worden behandeld.
Reusceltumordegeneratie van bot tot kwaadaardige ziekte of gemetastaseerde progressie van de ziekte zijn zeldzame gebeurtenissen en vormen een bekend risico bij patiënten met reusceltumor van het bot. Patiënten moeten worden gecontroleerd op radiologische tekenen van maligniteit, nieuwe radiolucentie of osteolyse. Beschikbare klinische gegevens duiden niet op een verhoogd risico op maligniteit bij patiënten met een reusceltumor van het bot die met XGEVA worden behandeld.
Waarschuwingen voor hulpstoffen
XGEVA bevat sorbitol. Patiënten met zeldzame erfelijke aandoeningen van fructose-intolerantie mogen XGEVA niet gebruiken.
Dit geneesmiddel bevat minder dan 1 mmol natrium (23 mg) per 120 mg, dat wil zeggen dat het in wezen "natriumvrij" is.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie -
Er zijn geen interactiestudies uitgevoerd.
In klinische onderzoeken werd XGEVA toegediend in combinatie met standaard antitumorbehandelingen en bij patiënten die eerder waren behandeld met bisfosfonaten. Er waren geen klinisch relevante veranderingen in de dalserumconcentratie en farmacodynamiek van denosumab (urinair creatinine-aangepast N-telopeptide, uNTx/Cr) als gevolg van hormoontherapie en/of gelijktijdige chemotherapie of eerdere intraveneuze toediening van bisfosfonaten.
04.6 Zwangerschap en borstvoeding -
Zwangerschap
Er zijn geen adequate gegevens beschikbaar over het gebruik van XGEVA bij zwangere vrouwen Reproductietoxiciteit werd aangetoond in een onderzoek bij cynomolgus-apen met toediening van denosumab tijdens de zwangerschap met een AUC van 12 maal de dosis voor de mens (zie rubriek 5.3. ).
Het gebruik van XGEVA wordt niet aanbevolen bij zwangere vrouwen en bij vrouwen in de vruchtbare leeftijd die geen zeer effectieve anticonceptiva gebruiken. Vrouwen moeten worden geadviseerd niet zwanger te worden tijdens de behandeling met XGEVA en gedurende ten minste 5 maanden na de behandeling. Behandeling. Eventuele effecten van XGEVA is waarschijnlijk het grootst tijdens het tweede en derde trimester van de zwangerschap, aangezien monoklonale antilichamen lineair door de placenta worden getransporteerd naarmate de zwangerschap vordert, waarbij de grootste hoeveelheid wordt overgedragen tijdens het derde trimester van de zwangerschap.
Voedertijd
Het is niet bekend of denosumab wordt uitgescheiden in de moedermelk. Studies bij knock-out muizen suggereren dat de afwezigheid van RANKL tijdens de zwangerschap de rijping van de borstklier zou kunnen verstoren, wat kan leiden tot verminderde lactatie na de partus (zie rubriek 5.3). Er moet worden besloten om af te zien van borstvoeding of van behandeling met XGEVA, waarbij het voordeel van borstvoeding voor de pasgeborene/zuigeling en het voordeel van behandeling met XGEVA voor de vrouw in overweging moeten worden genomen.
Vruchtbaarheid
Er zijn geen gegevens over de effecten van denosumab op de vruchtbaarheid bij de mens. Dierstudies wijzen niet op directe of indirecte schadelijke effecten op de vruchtbaarheid (zie rubriek 5.3).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen -
XGEVA heeft geen of een verwaarloosbare invloed op de rijvaardigheid en op het vermogen om machines te bedienen.
04.8 Bijwerkingen -
Samenvatting van het veiligheidsprofiel
Het algemene veiligheidsprofiel is consistent voor alle goedgekeurde indicaties.
Hypocalciëmie werd vaak gemeld na toediening van XGEVA, meestal binnen de eerste 2 weken Hypocalciëmie kan ernstig en symptomatisch zijn (zie rubriek 4.8 - Beschrijving van geselecteerde bijwerkingen). Verlagingen van de serumcalciumconcentraties worden gewoonlijk adequaat behandeld met calcium- en vitamine D-suppletie. De meest voorkomende bijwerkingen van XGEVA zijn musculoskeletale pijn.
De veiligheid van XGEVA is beoordeeld op:
• 5.931 patiënten met gevorderde kanker waarbij bot betrokken is in actief gecontroleerde klinische onderzoeken ter evaluatie van de werkzaamheid en veiligheid van XGEVA versus zoledroninezuur bij de preventie van skeletgerelateerde voorvallen.
• 523 patiënten met een reusceltumor van het bot in een klinisch onderzoek met één arm om de werkzaamheid en veiligheid van XGEVA te evalueren.
Bijwerkingen die in deze klinische onderzoeken en in de postmarketingsetting zijn vastgesteld, worden weergegeven in tabel 1.
Tabel met bijwerkingen
Voor de classificatie van bijwerkingen op basis van incidentiepercentages in drie fase III en twee fase II klinische onderzoeken, werd de volgende conventie gebruikt (zie tabel 1): zeer vaak (≥ 1/10), vaak (≥ 1/100,
Tabel 1: Bijwerkingen gemeld bij patiënten met gevorderde kankers waarbij bot- of reuscelkanker van het bot is betrokken
¹ Zie rubriek Beschrijving van geselecteerde bijwerkingen
² Zie rubriek Andere bijzondere populaties
Beschrijving van geselecteerde bijwerkingen
Hypocalciëmie
In drie actief gecontroleerde klinische fase III-onderzoeken bij patiënten met gevorderde kankers waarbij bot betrokken was, werd hypocalciëmie gemeld bij 9,6% van de patiënten die werden behandeld met XGEVA en bij 5,0% van de patiënten die werden behandeld met zoledroninezuur.
Bij 2,5% van de met XGEVA behandelde patiënten en bij 1,2% van de met zoledroninezuur behandelde patiënten werd een graad 3 daling van de serumcalciumspiegels vastgesteld. Bij 0,6% van de met XGEVA behandelde patiënten en bij 0,2% werd een graad 4 daling van de serumcalciumspiegels vastgesteld. van patiënten behandeld met zoledroninezuur (zie rubriek 4.4).
In twee klinische fase II-onderzoeken met één arm bij patiënten met een reusceltumor van het bot, werd hypocalciëmie gemeld bij 5,7% van de patiënten. Geen van de bijwerkingen werd als ernstig beschouwd.
Tijdens postmarketinggebruik is ernstige symptomatische hypocalciëmie (waaronder gevallen met fatale afloop) gemeld, waarbij de meeste gevallen binnen de eerste paar weken na aanvang van de therapie optraden. Voorbeelden van klinische manifestaties van ernstige symptomatische hypocalciëmie waren verlenging van het QT-interval, tetanie, toevallen en veranderde mentale toestand (inclusief coma) (zie rubriek 4.4) Symptomen van hypocalciëmie in klinische onderzoeken waren paresthesie of spierstijfheid, spiertrekkingen, spierspasmen en krampen.
Osteonecrose van de kaak (ONJ)
In klinische onderzoeken was de incidentie van ONJ hoger bij een langere blootstellingsduur; ONJ werd ook gediagnosticeerd na het einde van de behandeling met XGEVA, waarbij de meeste gevallen binnen 5 maanden na de laatste dosis optraden. Patiënten met een voorgeschiedenis van ONJ of osteomyelitis van de onderkaak/maxilla, met actieve tandheelkundige of mandibulaire/maxillaire ontsteking die een operatie vereist, een resultaat van onopgeloste tandheelkundige/kaakchirurgie, of patiënten voor wie invasieve tandheelkundige ingrepen waren gepland, werden uitgesloten van klinische onderzoeken.
In de primaire behandelingsfasen van drie fase III actief-gecontroleerde klinische onderzoeken bij patiënten met gevorderde kankers waarbij bot betrokken was, werd ONJ bevestigd bij 1,8% van de patiënten behandeld met XGEVA (mediane blootstelling van 12, 0 maanden; bereik 0,1 - 40,5) en bij 1,3 % van de patiënten behandeld met zoledroninezuur. De klinische kenmerken van deze gevallen waren vergelijkbaar tussen de behandelingsgroepen. Van de patiënten met bevestigde ONJ hadden de meeste (81% in beide behandelingsgroepen) een voorgeschiedenis van tandextracties, slechte mondhygiëne en/of gebruik van beugels De meeste proefpersonen kregen of hadden chemotherapie gekregen.
Klinische onderzoeken bij patiënten met borst- of prostaatkanker omvatten een verlengingsfase van de behandeling met XGEVA (mediane totale blootstelling van 14,9 maanden; bereik 0,1 - 67,2). ONJ werd bevestigd bij 6,9% van de patiënten met borstkanker en prostaatkanker tijdens de verlengingsfase van de behandeling.
De totale bevestigde incidentie van ONJ, gecorrigeerd voor patiëntjaar, was 1,1% tijdens het eerste jaar van de behandeling, 3,7% tijdens het tweede jaar en 4,6% in de daaropvolgende jaren. De mediane tijd tot "ONJ-begin was 20,6 maanden (bereik: 4 - 53).
In twee klinische fase II-onderzoeken met één arm bij patiënten met een reusceltumor van het bot, trad ONJ op bij 2,3% (12 van de 523) van de patiënten die werden behandeld met XGEVA (mediane totale blootstelling van 20,3 maanden; bereik: 0-83,4). De incidentie van ONJ, gecorrigeerd voor patiëntjaar, was 0,2% tijdens het eerste jaar van de behandeling en 1,7% tijdens het tweede jaar. De mediane tijd tot het optreden van ONJ was 19,4 maanden (spreiding: 11-40).Gebaseerd op de blootstellingsduur zijn er onvoldoende gegevens voor patiënten met GCTB om het risico op ONJ na 2 jaar te beoordelen.
In een klinische fase III-studie bij patiënten met niet-gemetastaseerde prostaatkanker (een patiëntenpopulatie waarvoor XGEVA niet is geïndiceerd), met een "langere behandelingsblootstelling (tot 7 jaar), werd de incidentie van ONJ bevestigd, gecorrigeerd per patiënt- jaar was 1,1% in het eerste behandeljaar, 3,0% in het tweede jaar en 7,1% in de daaropvolgende jaren.
Overgevoeligheidsreacties op het medicijn
Voorvallen van overgevoeligheid, waaronder zeldzame anafylactische reacties, zijn gemeld bij patiënten die XGEVA kregen tijdens postmarketinggebruik.
Atypische fracturen van het dijbeen
In het klinische ontwikkelingsprogramma zijn zelden atypische femurfracturen gemeld bij patiënten die werden behandeld met denosumab (zie rubriek 4.4).
Musculoskeletale pijn
In de postmarketingsetting werd skeletspierstelselpijn, waaronder ernstige gevallen, gemeld bij patiënten die werden behandeld met XGEVA. In klinische onderzoeken kwam skeletspierstelselpijn zeer vaak voor in zowel de denosumab- als zoledroninezuurbehandelingsgroepen. Skeletspierstelselpijn die leidde tot stopzetting van de behandeling kwam soms voor.
Pediatrische populatie
XGEVA werd onderzocht in een open-label klinische studie bij 18 adolescenten met een volgroeid skelet met een reusceltumor van het bot. Op basis van deze beperkte gegevens lijkt het bijwerkingenprofiel vergelijkbaar te zijn met dat bij volwassenen.
Andere speciale populaties
Nierfunctiestoornis
In een klinische studie bij patiënten met ernstige nierfunctiestoornis (creatinineklaring calciumsuppletie. Het risico op het ontwikkelen van hypocalciëmie tijdens behandeling met XGEVA is groter naarmate de mate van nierfunctiestoornis toeneemt. In een klinische studie bij niet-kankerpatiënten. in vergevorderd stadium, 19 % patiënten met ernstige nierfunctiestoornis (creatinineklaring
Daaropvolgende verhogingen van de parathyroïdhormoonspiegels zijn ook waargenomen bij patiënten met een ernstige nierfunctiestoornis of die dialyse ondergaan die met XGEVA worden behandeld. Controle van de calciumspiegels en adequate calcium- en vitamine D-suppletie zijn met name belangrijk bij patiënten met een nierfunctiestoornis (zie rubriek 4.4).
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt.Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem (Italiaans Geneesmiddelenbureau - Website: http // www.agenziafarmaco.gov.it / it / managers).
04.9 Overdosering -
In klinische onderzoeken zijn geen gevallen van overdosering gemeld. In klinische onderzoeken werd XGEVA toegediend in doses tot 180 mg elke 4 weken en 120 mg per week gedurende 3 weken.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN -
05.1 "Farmacodynamische eigenschappen -
Farmacotherapeutische categorie: Geneesmiddelen voor de behandeling van botziekten - Andere geneesmiddelen die de botstructuur en -mineralisatie beïnvloeden, ATC-code: M05BX04
Werkingsmechanisme
RANKL is een eiwit en komt in transmembraan of oplosbare vorm. RANKL is essentieel voor de vorming, functie en overleving van osteoclasten, het enige celtype dat verantwoordelijk is voor botresorptie. Verhoogde osteoclastische activiteit, gestimuleerd door RANKL, is een belangrijke mediator van botvernietiging bij gemetastaseerde botziekte en bij multipel myeloom. Denosumab is een humaan monoklonaal antilichaam (IgG2) dat zich richt op en bindt aan RANKL met hoge affiniteit en specificiteit, waardoor het optreden van de RANKL / RANK-interactie wordt voorkomen, waardoor het aantal en de functie van osteoclasten wordt verminderd, wat resulteert in verminderde botresorptie en door kanker geïnduceerde botvernietiging .
Reusceltumoren van bot worden gekenmerkt door neoplastische stromale cellen die het RANK-ligand tot expressie brengen en osteoclastachtige reuzencellen die RANK tot expressie brengen.Bij patiënten met reuzencelbotkanker bindt denosumab aan het RANK-ligand, waardoor de osteoclast-achtige gigantische cellen. Dientengevolge wordt osteolyse verminderd en wordt het proliferatieve stroma van de tumor vervangen door nieuw bot met een dichte, niet-proliferatieve, gedifferentieerde structuur.
Farmacodynamische effecten
In klinische fase II-onderzoeken bij patiënten met kanker in een gevorderd stadium waarbij bot betrokken was, resulteerde subcutane (sc) toediening van XGEVA elke 4 weken of elke 12 weken in een snelle verlaging van de botresorptiemarkers (uNTx/Cr, Serum CTx), met mediane verlagingen van ongeveer 80% voor uNTx / Cr binnen een week, ongeacht eerdere bisfosfonaattherapie of baseline uNTx / Cr-niveau. In klinische fase III-onderzoeken werden mediane verlagingen van ongeveer 80% in uNTx/Cr gehandhaafd na 3 maanden behandeling bij 2.075 patiënten met gevorderde kanker die werden behandeld met XGEVA en die niet eerder waren behandeld met IV-bisfosfonaat.
immunogeniciteit
In klinische onderzoeken werden geen neutraliserende antilichamen tegen XGEVA waargenomen. Op basis van de resultaten van een gevoelige immunoassay testte minder dan 1% van de patiënten die tot 3 jaar met denosumab werden behandeld, positief op niet-neutraliserende antilichamen zonder bewijs van een gewijzigd farmacokinetisch, toxicologisch of klinisch responsprofiel.
Klinische werkzaamheid bij patiënten met botmetastasen van solide tumoren
Werkzaamheid en veiligheid van XGEVA 120 mg s.c., elke 4 weken gegeven of van zoledroninezuur 4 mg i.v. (met dosisaanpassing voor verminderde nierfunctie), elke 4 weken toegediend, werden vergeleken in drie gerandomiseerde, dubbelblinde, actief-gecontroleerde onderzoeken bij patiënten die nog niet eerder waren behandeld met IV-bisfosfonaat en met gevorderde kankers met botaantasting: volwassen patiënten met borstkanker ( onderzoek 1), andere solide tumoren of multipel myeloom (onderzoek 2) en castratieresistente prostaatkanker (onderzoek 3) actieve tandheelkundige of mandibulaire / maxillaire kaakchirurgie, een onopgeloste tandheelkundige / mondaandoening na een operatie, of patiënten die zijn ingepland voor invasieve tandheelkundige procedures kwamen niet in aanmerking voor deelname aan deze onderzoeken. De primaire en secundaire eindpunten beoordeelden het optreden van een of meer skeletgerelateerde voorvallen (SRE) In onderzoeken die de superioriteit van XGEVA boven zoledroninezuur aantoonden, werd patiënten een verlengingsfase aangeboden van een vooraf gespecificeerde behandeling, open label met XGEVA gedurende 2 jaar .
XGEVA verminderde het risico op het ontwikkelen van SRE's en op het ontwikkelen van meerdere (eerste en volgende) SRE's bij patiënten met botmetastasen van solide tumoren (zie tabel 2).
Tabel 2: Werkzaamheidsresultaten bij patiënten met gevorderde kankers waarbij bot is betrokken
NR = niet bereikt; NVT = niet beschikbaar; HCM = maligne hypercalciëmie; SMR = skelet morbiditeit; HR = risicoverhouding; RRR = relatieve risicoreductie † Voor studies 1, 2 en 3 worden aangepaste p-waarden gepresenteerd (eindpunten: eerste SRE, en eerste en volgende SRE's); * Omvat alle skeletgebeurtenissen in de loop van de tijd; alleen gebeurtenissen die ≥ 21 dagen na de vorige gebeurtenis hebben plaatsgevonden, worden in aanmerking genomen.
** Inclusief NSCLC, nierkanker, colorectale kanker, kleincellige longkanker, blaaskanker, hoofd- en nekkanker, maag-darmkanker/urogenitale kanker en andere vormen van kanker behalve borst- en prostaatkanker
Ziekteprogressie en algehele overleving
De ziekteprogressie was vergelijkbaar tussen XGEVA en zoledroninezuur in alle drie de onderzoeken en in de gecombineerde vooraf gespecificeerde analyse van alle drie de onderzoeken.
In alle drie de onderzoeken was de totale overleving tussen XGEVA en zoledroninezuur in evenwicht bij patiënten met gevorderde kankers waarbij bot betrokken was: borstkankerpatiënten (hazard ratio en 95% BI: 0,95 [0,81-1,11]), patiënten met prostaatkanker (hazard ratio en 95 % BI: 1,03 [0,91-1,17]) en patiënten met andere solide tumoren of multipel myeloom (hazard ratio en 95% BI: 0,95 [0,83-1,08]). In een post-hocanalyse van onderzoek 2 (patiënten met andere solide tumoren of multipel myeloom) werd de totale overleving onderzocht voor de drie tumortypes die werden gebruikt voor stratificatie (niet-kleincellige longkanker, multipel myeloom en meer). voor XGEVA bij niet-kleincellige longkanker (hazard ratio [95% BI] van 0,79 [0,65-0,95]; n = 702), hoger voor zoledroninezuur bij multipel myeloom (hazard ratio [95% BI] van 2,26 [1,13- 4,50]; n = 180) en vergelijkbaar voor XGEVA en zoledroninezuur bij andere tumortypen (hazard ratio [95% BI] van 1,08 [0,90-1,30]; n = 894). Prognostische factoren en antineoplastische behandelingen werden niet geverifieerd in deze studie. In een gecombineerde, vooraf gespecificeerde analyse van onderzoeken 1, 2 en 3 was de totale overleving vergelijkbaar tussen XGEVA en zoledroninezuur (hazard ratio en 95% BI: 0,99 [0,91-1,07]).
Effecten op pijn
De tijd tot verbetering van de pijn (d.w.z. 2-punts reductie ten opzichte van baseline, in BPI-SF-score voor ergste pijn) was vergelijkbaar voor denosumab en zoledroninezuur in elk onderzoek en geïntegreerde analyses. In een "post-hocanalyse van de gecombineerde dataset was de mediane tijd tot verergering van de pijn (> 4 punten in pijnscore van de slechtste intensiteit) bij patiënten met milde of geen pijn bij aanvang vertraagd voor XGEVA vergeleken met" zoledroninezuur (198 vs. .143 dagen) (p = 0,0002).
Klinische werkzaamheid bij volwassenen en adolescenten met een volgroeid skelet met een reusceltumor van het bot
De veiligheid en werkzaamheid van XGEVA zijn onderzocht in twee open-label, eenarmige klinische fase II-onderzoeken (onderzoeken 4 en 5) waarbij 529 patiënten met ofwel niet-reseceerbare of niet-reseceerbare reusceltumor van het bot werden geïncludeerd. ziektecijfers.
Aan onderzoek 4 deden 37 volwassen patiënten mee met histologisch bevestigde inoperabele reusceltumor van het bot of recidiverende reusceltumor van het bot. Responscriteria omvatten eliminatie van reuzencellen op histopathologische basis of afwezigheid van progressie op radiografische basis.
Van de 35 patiënten die in de werkzaamheidsanalyse waren opgenomen, reageerde 85,7% (95% BI: 69,7-95,2) op behandeling met XGEVA. Alle 20 patiënten (100%) die een histologische evaluatie ondergingen, reageerden op de behandeling. Bij de overige 15 patiënten lieten 10 (67%) radiologische rapporten geen progressie van de doellaesie zien.
Aan onderzoek 5 namen 507 volwassenen of adolescenten met een volgroeid skelet deel met een reusceltumor van het bot en tekenen van meetbare actieve ziekte.
In cohort 1 (patiënten met inoperabele ziekte) werd de mediane tijd tot ziekteprogressie niet bereikt, 21 van de 258 behandelde patiënten hadden ziekteprogressie. In cohort 2 (patiënten met een reseceerbare ziekte, maar voor wie geplande chirurgie gepaard ging met ernstige morbiditeit), ondergingen 209 van de 228 evalueerbare patiënten die werden behandeld met XGEVA geen operatie in maand 6. In totaal werden van 225 patiënten voor wie het reusceltumorbot was chirurgie was gepland (exclusief longmetastasen), 109 ondergingen geen operatie en 84 ondergingen minder invasieve procedures dan gepland bij baseline. De mediane tijd tot chirurgie was 261 dagen.
Een onafhankelijke retrospectieve beoordeling van radiologische beeldvormingsgegevens werd uitgevoerd bij de inschrijving van 305 patiënten in onderzoeken 4 en 5. Honderdnegentig hadden ten minste één keer een evalueerbare respons en werden in de analyse opgenomen (tabel 3). Over het algemeen bereikte XGEVA objectieve responsen bij 71,6% van de patiënten (95% BI: 64,6-77,9) (Tabel 3) beoordeeld met behulp van verschillende methodologieën, waarbij de meeste responsen werden gedefinieerd als vermindering van de activiteit van de fluorodeoxyglucose-PET of dichtheidstoename gemeten in CT /HU, had slechts 25,1% van de patiënten een respons volgens RECIST De mediane tijd tot respons was 3,1 maanden (95% BI: 2,89-3, 65) De mediane duur van de respons was niet evalueerbaar (vier patiënten vertoonden ziekteprogressie na objectieve respons. ) Bij 190 proefpersonen die evalueerbaar waren voor objectieve tumorrespons, ondergingen 55 proefpersonen met GCTB een operatie, waarvan 40 een volledige resectie hebben ondergaan.
Tabel 3: Objectieve respons op behandeling bij patiënten met reuzencelkanker van het bot
¹ BI = Exact betrouwbaarheidsinterval
² RECIST 1.1: aangepaste criteria voor het evalueren van de respons in solide tumoren om de tumormassa te evalueren door middel van computergestuurde axiale tomografie (CT) of magnetische resonantiebeeldvorming (MRI).
³ EORTC: aangepaste criteria van de Europese Organisatie voor Onderzoek en Behandeling van Kanker om de metabole respons te evalueren door het gebruik van Positron Emissie Tomografie met Fluoridesoxyglucose (FDG-PET).
4 Dichtheid/omvang: gewijzigde Choi Inverse-criteria om tumorgrootte en dichtheid te beoordelen met behulp van Hounsfield-eenheden op basis van CT/MRI.
Effect op pijn
Bij deelname van 282 patiënten, in studie 5 gecombineerde cohorten 1 en 2, werd een klinisch significante vermindering van de ergste pijn (bijv. ≥ 2 punten afname vanaf baseline) gemeld bij 31,4% van de risicopatiënten (bijv. degenen die de ergste pijn hadden score ≥ 2 bij baseline) binnen één week behandeling en ≥ 50% in week 5. Deze pijnverbeteringen bleven ongewijzigd in daaropvolgende evaluaties.Het baselinegebruik van analgetica vóór de behandeling in cohort 1 en cohort 2 werd beoordeeld met behulp van een zevenpuntsschaal, waarbij 74,8% van de patiënten matige of niet-gebruik van analgetica meldde (bijv. analgetische score ≤ 2) en 25,2% van de patiënten sterke opioïden gebruikt (bijv. analgetische score 3 tot 7).
Pediatrische populatie
Het Europees Geneesmiddelenbureau heeft besloten af te zien van de verplichting om de resultaten in te dienen van onderzoek met XGEVA in alle subgroepen van pediatrische patiënten voor de preventie van skeletgerelateerde voorvallen bij patiënten met botmetastasen en in subgroepen van pediatrische patiënten jonger dan 12 jaar voor de behandeling van reus celkanker van het bot (zie rubriek 4.2 voor informatie over pediatrisch gebruik).
In onderzoek 5 werd XGEVA geëvalueerd bij een subgroep van 18 adolescente patiënten (13 tot 17 jaar oud) met een reusceltumor van het bot die de volwassenheid van het skelet had bereikt, gedefinieerd als ten minste één volgroeid lang bot (bijv. plaat van de humerus) en lichaamsgewicht ≥ 45 kg Een objectieve respons werd waargenomen bij vier van de zes evalueerbare adolescenten in een "tussentijdse analyse van onderzoek 5. Een evaluatie van de onderzoeker meldde dat alle 18 adolescente patiënten de beste stabiele of superieure ziekte hadden respons (volledige respons bij 2 patiënten, gedeeltelijke respons bij 8 patiënten en ziektestabiliteit bij 8 patiënten). Het Europees Geneesmiddelenbureau heeft de verplichting om de definitieve resultaten van dit onderzoek in te dienen, uitgesteld.
05.2 "Farmacokinetische eigenschappen -
Absorptie
Na subcutane toediening was de biologische beschikbaarheid 62%.
Biotransformatie
Denosumab bestaat uitsluitend uit aminozuren en koolhydraten zoals natieve immunoglobulinen en wordt waarschijnlijk niet geëlimineerd door hepatische metabole mechanismen. Het metabolisme en de eliminatie van het geneesmiddel zullen naar verwachting de routes van immunoglobulineklaring volgen, dwz afbraak tot kleine peptiden en afzonderlijke aminozuren.
Eliminatie
Bij proefpersonen met gevorderde kanker, die om de 4 weken meerdere doses van 120 mg kregen, werd een ongeveer 2-voudige accumulatie in serumconcentraties van denosumab waargenomen en werd binnen 6 maanden een steady-state bereikt; dit is consistent met tijdonafhankelijke farmacokinetiek. Bij proefpersonen met een reusceltumor van het bot die om de 4 weken 120 mg kregen met een oplaaddosis op dag 8 en 15, werden steady-state spiegels bereikt binnen de eerste maand van de behandeling. Tussen week 9 en 49 varieerden de mediane spiegels met minder dan Bij proefpersonen die stopten met het innemen van 120 mg elke 4 weken, was de gemiddelde halfwaardetijd 28 dagen (bereik: 14-55 dagen).
Een farmacokinetische populatieanalyse bracht geen klinisch significante veranderingen aan het licht in de systemische blootstelling aan denosumab bij steady-state voor leeftijd (18-87 jaar), ras/etnische groep (zwarte, Spaanse, Aziatische en blanke proefpersonen werden onderzocht.), geslacht of type solide tumor . Gewichtstoename ging gepaard met een afname van de systemische blootstelling en vice versa. De veranderingen werden niet als klinisch relevant beschouwd, aangezien de farmacodynamische effecten op basis van markers van botturnover constant waren over een breed bereik van lichaamsgewichten.
Lineariteit / niet-lineariteit
Denosumab vertoonde niet-lineaire farmacokinetiek bij verschillende dosisniveaus, maar voor doses van 60 mg (of 1 mg/kg) en daarboven vertoonde het een ongeveer dosisproportionele toename van de blootstelling. Niet-lineariteit is waarschijnlijk te wijten aan een eliminatiemechanisme. verzadigbaar gemedieerd doelwit, belangrijk bij lage concentraties.
Nierfunctiestoornis
In onderzoeken met denosumab (60 mg, n = 55 en 120 mg, n = 32) bij patiënten zonder gevorderde kanker maar met een verschillende mate van nierfunctie, inclusief patiënten die dialyse ondergaan, had de mate van nierfunctiestoornis geen effect op de farmacokinetiek van denosumab; daarom is er geen dosisaanpassing nodig in geval van nierinsufficiëntie. Niercontrole is niet vereist wanneer u XGEVA krijgt.
leverfunctiestoornis
Er zijn geen specifieke onderzoeken uitgevoerd bij patiënten met een verminderde leverfunctie. In het algemeen worden monoklonale antilichamen niet geëlimineerd door levermetabolisme. De farmacokinetiek van denosumab wordt naar verwachting niet beïnvloed door een verminderde leverfunctie.
Bejaarden
Over het algemeen werden geen verschillen in veiligheid en werkzaamheid waargenomen tussen geriatrische patiënten en jongere patiënten Gecontroleerde klinische onderzoeken met XGEVA bij patiënten ouder dan 65 jaar met gevorderde maligniteiten met botaantasting hebben vergelijkbare werkzaamheid en veiligheid aangetoond bij oudere en jongere proefpersonen Geen dosisaanpassing is vereist bij oudere patiënten.
Pediatrische populatie
Het farmacokinetische profiel bij pediatrische patiënten is niet geëvalueerd.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek -
Aangezien de biologische activiteit van denosumab bij dieren specifiek is voor niet-menselijke primaten, werden evaluaties van genetisch gemodificeerde (knock-out) muizen of het gebruik van andere biologische remmers van de route gebruikt om de farmacodynamische eigenschappen van denosumab in knaagdiermodellen te evalueren. , zoals OPG-Fc en RANK-Fc.
In muismodellen van botmetastase van menselijke borstkanker, oestrogeenreceptor positief en negatief, prostaatkanker en niet-kleincellige longkanker, verminderde OPG-Fc osteolytische, osteoblastische en osteolytische/osteoblastische laesies, vertraagde de vorming van botmetastasen de nieuwe en verminderde tumorgroei van het skelet. In deze modellen werd, wanneer OPG-Fc werd gecombineerd met hormonale therapie (tamoxifen) of chemotherapie (docetaxel), een "verdere remming van tumorgroei van het skelet" gevonden. , respectievelijk, in borst kanker en bij prostaat- of longkanker. In een muismodel van borstkanker-inductie verminderde RANK-Fc de door hormonen geïnduceerde proliferatie in het borstepitheel en vertraagde de tumorvorming.
Er zijn geen standaardtests uitgevoerd om de mogelijke genotoxiciteit van denosumab te onderzoeken, aangezien deze tests niet relevant zijn voor dit molecuul. Gezien zijn kenmerken is het echter onwaarschijnlijk dat denosumab genotoxisch potentieel heeft.
Het carcinogene potentieel van denosumab is niet onderzocht in langdurige dierstudies.
In toxiciteitsonderzoeken met enkelvoudige en herhaalde doses uitgevoerd bij cynomolgus-apen, hadden doses denosumab die resulteerden in "systemische blootstelling van 2,7 tot 15 keer de aanbevolen dosis voor de mens" geen invloed op de cardiovasculaire fysiologie, mannelijke vruchtbaarheid of vrouwelijke, of specifieke orgaantoxiciteitsproducten.
In een onderzoek bij cynomolgus-apen met meervoudige doses denosumab tijdens de periode gelijk aan het eerste trimester van de zwangerschap, veroorzaakten doses denosumab die resulteerden in een 9-voudige systemische blootstelling van de aanbevolen dosis voor de mens geen maternale toxiciteit of schade aan de foetus bij een periode gelijk aan het eerste trimester; de foetale lymfeklieren werden echter niet onderzocht.
In een andere studie van cynomolgus-apen die tijdens de zwangerschap denosumab kregen, bij een systemische blootstelling die 12 keer de dosis voor mensen was, was er een toename van doodgeboorte en postnatale mortaliteit, abnormale botgroei, resulterend in verminderde botsterkte, verminderde hematopoëse en slechte tanduitlijning; afwezigheid van perifere lymfeklieren; en verminderde neonatale groei. Er is geen dosisniveau vastgesteld dat negatief kan zijn voor reproductieve effecten. Daarna, 6 maanden na de geboorte, vertoonden de botveranderingen herstel en was er geen effect op tanddoorbraak. De effecten op lymfeklieren en tandafwijkingen hielden echter aan, en het werd waargenomen bij een minimale tot matige mineralisatie in meerdere weefsels (behandeling correlatie onzeker) Er was geen bewijs van maternale schade voorafgaand aan de bevalling. Maternale bijwerkingen kwamen niet vaak voor tijdens de bevalling. De ontwikkeling van de moederborstklier was normaal.
In preklinische onderzoeken naar de botkwaliteit die werden uitgevoerd bij apen die langdurig met denosumab werden behandeld, ging een verminderde botturnover gepaard met verbeterde botsterkte en normale histologie.
Bij mannelijke muizen die genetisch gemanipuleerd waren om menselijke RANKL (knock-in muizen) tot expressie te brengen en onderworpen waren aan een transcorticale fractuur, vertraagde denosumab de verwijdering van kraakbeen en de hermodellering van callus in vergelijking met de controlegroep, maar de biomechanische kracht werd niet nadelig beïnvloed.
Afwezigheid van borstvoeding als gevolg van remming van de rijping van de borstklier (ontwikkeling van de lobulo-alveolaire structuren van de borstklier tijdens de zwangerschap) werd waargenomen bij knock-out muizen die geen RANK of RANKL tot expressie brachten, evenals een gestoorde vorming RANK / RANKL knock-out pasgeboren muizen vertoonden gewichtsverlies, verminderde botgroei, veranderde groeischijven en gebrek aan tanduitbarsting Verminderde botgroei, veranderde groeischijven en verminderde tanduitbarsting werden ook waargenomen in onderzoeken bij neonatale ratten die RANKL-remmers kregen; deze veranderingen waren gedeeltelijk reversibel na stopzetting van de RANKL-remmer Adolescente primaten die werden behandeld met 2,7- en 15-voudige doses denosumab (doses van 10 en 50 mg/kg) vertoonden afwijkingen van de ca. groei staven. Daarom kan behandeling met denosumab de botgroei bij kinderen met open groeischijven belemmeren en tanddoorbraak remmen.
06.0 FARMACEUTISCHE INFORMATIE -
06.1 Hulpstoffen -
Ijsazijn *
Natriumhydroxide (voor pH-aanpassing) *
Sorbitol (E420)
Water voor injecties
* Acetaatbuffer wordt verkregen door azijnzuur en natriumhydroxide te mengen
06.2 Incompatibiliteit "-
Bij gebrek aan onderzoek naar onverenigbaarheden, mag dit geneesmiddel niet worden gemengd met andere geneesmiddelen.
06.3 Geldigheidsduur "-
3 jaar.
XGEVA is in de originele verpakking maximaal 30 dagen houdbaar bij kamertemperatuur (tot 25°C). Eenmaal uit de koelkast gehaald, moet XGEVA binnen deze periode van 30 dagen worden gebruikt.
06.4 Speciale voorzorgsmaatregelen bij bewaren -
Bewaren in de koelkast (2 ° C - 8 ° C).
Niet bevriezen.
Bewaar de injectieflacon in de buitenverpakking om het geneesmiddel tegen licht te beschermen.
06.5 Aard van de primaire verpakking en inhoud van de verpakking -
1,7 ml oplossing in een injectieflacon voor eenmalig gebruik (type I-glas) met een stop (omhuld met elastomeer fluorpolymeer) en een verzegeling (aluminium) met een flip-off-dop.
Verpakkingsgrootte van één, drie of vier injectieflacons.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking -
Voorafgaand aan toediening moet de XGEVA-oplossing visueel worden geïnspecteerd. De oplossing kan sporen van doorschijnende tot witte eiwitachtige deeltjes bevatten. Injecteer de oplossing niet als deze troebel of verkleurd is. Niet te veel schudden. Om problemen op de injectieplaats te voorkomen, laat u de injectieflacon vóór injectie op kamertemperatuur (tot 25 ° C) komen en injecteert u langzaam. Injecteer de volledige inhoud van de injectieflacon. Een stalen naald van 27 gauge wordt aanbevolen voor toediening van denosumab. Gebruik de injectieflacon niet opnieuw.
Ongebruikte medicijnen en afval afkomstig van dit medicijn moeten worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE "VERGUNNING VOOR HET IN DE HANDEL BRENGEN" -
Amgen Europe B.V.
Minervum 7061
NL-4817 ZK Breda
Nederland
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN -
EU / 1/11/703/001
EU / 1/11/703/002
EU / 1/11/703/003
041300017
041300029
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING -
Datum eerste vergunning: 13 juli 2011
Datum van laatste verlenging: 4 april 2016
10.0 DATUM VAN HERZIENING VAN DE TEKST -
december 2016