Actieve ingrediënten: Methylprednisolon
URBASON 4 mg tabletten
Urbason-bijsluiters zijn beschikbaar voor verpakkingen:- URBASON 4 mg tabletten
- URBASON 8 mg tabletten met verlengde afgifte, URBASON 4 mg tabletten met verlengde afgifte
Waarom wordt Urbason gebruikt? Waar is het voor?
FARMACOTHERAPEUTISCHE CATEGORIE
Systemische corticosteroïden, glucocorticoïden.
THERAPEUTISCHE INDICATIES
De belangrijkste toepassingsgebieden zijn: reumatische aandoeningen, bronchiale astma, hooikoorts, serumziekte, overgevoeligheid voor medicijnen en andere allergische reacties. Urticaria, gegeneraliseerd eczeem, dermatitis, gedissemineerde erythematoden, dermatomyositis, pemphigus, exfoliatieve dermatitis. Agranulocytose, trombopenie, verworven hemolytische anemie, myeloblastose, lymfadenose, lymfogranulomatose. Hepatitis, colitis ulcerosa, adrenogenitaal syndroom, nefrotisch syndroom (ook in combinatie met het salureticum Lasix).Contra-indicaties Wanneer Urbason niet mag worden gebruikt
Het mag niet worden gebruikt bij patiënten met overgevoeligheid voor methylprednisolon of voor andere glucocorticoïden of voor één van de hulpstoffen (zie "Samenstelling").
Behalve bij vervangings- of spoedbehandelingen, mag Urbason niet worden toegediend bij:
- patiënten met maag- of darmzweren;
- patiënten met botdemineralisatie (osteoporose);
- patiënten met psychische stoornissen;
- patiënten met open en gesloten hoekglaucoom;
- patiënten met herpetische keratitis;
- patiënten met sommige virale ziekten zoals: waterpokken, herpes simplex en tijdens de virale fase van herpes zoster;
- patiënten met latente of manifeste tuberculose en zelfs als deze slechts wordt vermoed (risico op het ontstaan van de ziekte tot dan latent of verergering van de reeds lopende ziekte);
- patiënten met lymfadenopathie na BCG-vaccinaties;
- patiënten die lijden aan amoebiasis;
- patiënten met systemische mycose;
- patiënten met poliomyelitis (met uitzondering van de encefalitische bulbaire vorm);
- gedurende ongeveer 8 weken voor en 2 weken na de vaccinaties.
Het wordt aanbevolen dat patiënten die worden behandeld met therapeutische doses glucocorticoïden (anders dan vervangingstherapie) niet worden gevaccineerd omdat de antilichaamrespons onvoldoende kan zijn of omdat ze neurologische complicaties kunnen ontwikkelen. Bij ernstige infecties kan Urbason alleen worden gebruikt in combinatie met een specifieke therapie.
Vanwege het risico op groeiachterstand mag Urbason alleen aan kinderen worden gegeven als dit duidelijk nodig is.
Voorzorgen bij gebruik Wat u moet weten voordat u Urbason inneemt
Vanwege het risico op darmperforatie met peritonitis mag Urbason alleen worden gebruikt wanneer dit duidelijk nodig is en met adequate monitoring van patiënten met:
- ernstige colitis ulcerosa met risico op perforatie, abces of purulente ontsteking;
- diverticulitis;
- recente darmanastomosen.
Tenzij ze al waterpokken hebben gehad, moeten kinderen en volwassenen contact vermijden met mensen met waterpokken of gordelroos.
Als ze worden blootgesteld aan dergelijke infecties tijdens het gebruik van Urbason, moeten ze onmiddellijk contact opnemen met een arts, zelfs als er geen symptomen zijn.
Patiënten met tuberculinereactiviteit moeten worden gecontroleerd vanwege het risico op reactivering.
Bij deze patiënten wordt chemoprofylaxe aanbevolen tijdens langdurige behandeling met glucocorticoïden. Bij patiënten met myasthenia gravis, vooral als ze hoge doses glucocorticoïden krijgen, bestaat het risico dat de ziekte verergert, meestal binnen de eerste twee weken na aanvang van de behandeling met glucocorticoïden. Het wordt daarom aanbevolen om de dosis Urbason laag te houden aan het begin van de behandeling en geleidelijk te verhogen.
De metabole toestand van diabetespatiënten moet worden gecontroleerd en de antidiabetische therapie moet indien nodig worden aangepast.
In het bijzonder moet na langdurige therapieën met hoge doses van het geneesmiddel rekening worden gehouden met een mogelijke water- en natriumretentie. In dit geval is het noodzakelijk om te zorgen voor een voldoende toevoer van kalium, waarvan het niveau in het bloed moet worden gecontroleerd, en voor een verminderde inname van natrium.
Er moet rekening worden gehouden met een mogelijke verergering van hypertensie en hartaandoeningen, daarom is passende monitoring van patiënten vereist.
Bij langdurige behandeling met glucocorticoïden omvatten medische controles oogheelkundige controles.
Bij patiënten met hypothyreoïdie of patiënten met levercirrose kan de respons op corticosteroïden verhoogd zijn en daarom zijn dosisverlaging en monitoring van de patiënt vereist.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Urbason veranderen
- Digitalisglucosiden: de werking van glucosiden kan worden versterkt door hypokaliëmie.
- Diuretica: verhoogde kaliumuitscheiding.
- Antidiabetica: het hypoglykemische effect kan verminderd zijn.
- Coumarinederivaten: antistollingseffecten kunnen verminderd zijn.
- Rifampicine, fenytoïne en barbituraten: het effect van corticosteroïden kan verminderd zijn (zie "Bijwerkingen").
- Niet-depolariserende spierverslappers: Spierontspanning kan worden verlengd.
- Oestrogeen (anticonceptiemiddelen): Gelijktijdig gebruik van oestrogeen kan het metabolisme van corticosteroïden, waaronder methylprednisolon, verminderen.
- Niet-steroïde ontstekingsremmers verhogen het risico op gastro-intestinale bloedingen.
- Ciclosporine: remming van het metabolisme; verhoogd risico op epileptische aanvallen.
- Allergietesten: Huidreacties op allergietesten kunnen onderdrukt worden.
- Diltiazem: remming van het metabolisme van methylprednisolon (CYP3A4) en remming van P-glycoproteïne. De patiënt moet worden gecontroleerd bij het starten van de behandeling met methylprednisolon. Aanpassing van de dosering van methylprednisolon kan nodig zijn.
Vertel het uw arts of apotheker als u onlangs andere geneesmiddelen heeft gebruikt, ook zonder voorschrift.
Waarschuwingen Het is belangrijk om te weten dat:
Het gebruik van glucocorticoïden kan het immuunsysteem verzwakken waardoor infecties kunnen ontstaan, sommige micro-organismen kunnen worden geactiveerd met als gevolg de manifestatie van latente infecties.
Glucocorticoïden kunnen de tekenen van een infectie verbergen, waardoor de diagnose van het bestaan of de ontwikkeling ervan moeilijker wordt.
Bij patiënten die systemische glucocorticoïden krijgen, kunnen bepaalde virale ziekten zoals waterpokken, herpes simplex en tijdens de virale fase van herpes zoster ook ernstig worden bij vervangende therapieën.
Systemische behandeling met glucocorticoïden kan chorioretinopathie veroorzaken, wat kan leiden tot visuele stoornissen, waaronder verlies van gezichtsvermogen. Langdurig gebruik van systemische behandeling met glucocorticoïden, zelfs bij lage doses, kan chorioretinopathie veroorzaken (zie rubriek "Bijwerkingen").
Zwangerschap en borstvoeding
Vraag uw arts of apotheker om advies voordat u een geneesmiddel inneemt.
Methylprednisolon passeert de placenta en gaat over in de moedermelk.
Aangezien er zeer beperkte ervaring is met het gebruik van methylprednisolon tijdens de zwangerschap, mag Urbason alleen worden toegediend als dit duidelijk nodig is, onder direct medisch toezicht. Als hoge doses van het geneesmiddel worden toegediend, moet om klinische redenen de borstvoeding worden gestaakt om te voorkomen dat de zuigeling methylprednisolon inneemt met de moedermelk.
Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Sommige bijwerkingen (verminderd gezichtsvermogen, vertroebeling van de lens, verhoogde oogdruk, duizeligheid en migraine) kunnen het concentratie- en reactievermogen van patiënten verminderen, wat een risico vormt in al die situaties waarin deze vaardigheden van bijzonder belang zijn (autorijden of machines gebruiken).
Belangrijke informatie over enkele bestanddelen van URBASON
URBASON bevat lactose.Als uw arts een intolerantie voor bepaalde suikers heeft vastgesteld, neem dan contact met hem op voordat u dit geneesmiddel inneemt.
Voor degenen die sporten:
Het gebruik van het middel zonder therapeutische noodzaak is doping en kan in ieder geval leiden tot positieve dopingtests.
Dosis, wijze en tijdstip van toediening Hoe Urbason te gebruiken: Dosering
Over het algemeen begint de behandeling met relatief hoge doses die in de loop van de behandeling worden verlaagd. Na een succesvolle initiële behandeling wordt de dagelijkse dosis geleidelijk verlaagd (met tussenpozen van één tot meerdere dagen) tot de minimumdosis die nodig is om een bevredigend resultaat te bereiken (onderhoudsdosis).
Bij bronchiale astma en allergische aandoeningen worden startdoses tussen 16-40 mg per dag aanbevolen, terwijl de onderhoudsdosering meestal 4-16 mg per dag is. Bij milde gevallen van chronische polyartritis kan 8-16 mg voldoende zijn om de therapie te starten, bij ernstige gevallen zijn echter 16-40 mg vereist en een dagelijkse dosis van 4-16 mg is gewoonlijk voldoende om therapeutisch succes te behouden.
Volgens de meest recente ervaring zijn hoge doses steroïden vereist bij acute reumatische koorts. Om deze reden moet de dagelijkse dosis van 40-80-120 mg (bij kinderen jonger dan 14 jaar 1,2-1,6 mg/kg lichaamsgewicht) worden toegediend totdat de bezinkingssnelheid van erytrocyten minimaal een week normaal is gebleven; daarna wordt de dosering geleidelijk afgebouwd.
Bij acute erythematodes, pemphigus vulgaris en bij verschillende hemopathieën is soms een aanzienlijk hogere dosering nodig, tot dagelijkse doses van 100 mg en meer.
Bij patiënten die worden behandeld met prednison of prednisolon, is de onderhoudsdosis bij het overschakelen op Urbason gewoonlijk 80% van de eerder toegediende dosis, d.w.z. de Urbason-tablet van 4 mg komt overeen met één prednison- of prednisolontablet vanaf 5 mg.
De tabletten mogen niet op een lege maag worden ingenomen; de verdeling van de dosis gedurende de dag en de duur van de therapie worden overgelaten aan het oordeel van de arts die, zoals bij elke therapie met glucocorticoïden, zal beslissen op basis van de ernst van de ziekte en de verschillende reacties van patiënten op de behandeling.
Overdosering Wat moet u doen als u te veel Urbason heeft ingenomen?
Er zijn geen gevallen bekend van acute intoxicatie. Indien nodig moet echter een maagspoeling worden uitgevoerd en moeten eventuele symptomen worden gecontroleerd.
In geval van accidentele inname/inname van een overmatige dosis URBASON, waarschuw dan onmiddellijk uw arts of ga naar het dichtstbijzijnde ziekenhuis.
Als u vragen heeft over het gebruik van URBASON, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Urbason
Zoals alle geneesmiddelen kan URBASON bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Tijdens behandeling met corticosteroïden, vooral bij intensieve en langdurige behandelingen, kunnen enkele van de volgende effecten optreden:
- abnormale verdeling van lichaamsvet zoals in het geval van maanfacies, zwaarlijvigheid en zeer zelden ook een verdeling van vet in het wervelkanaal (epiduraal) of in de borstholte (epicardiaal, mediastinum); gewichtstoename.
- natriumretentie en ophoping van water in de weefsels, verhoogde kaliumuitscheiding met mogelijke hypokaliëmie, verhoogde pulmonale congestie bij patiënten met een hartaanval, hypertensie.
- verandering in de afscheiding van geslachtshormonen (mogelijke amenorroe, toegenomen haargroei, verminderde seksuele potentie); inactivatie of atrofie van corticoadrenale activiteit, groeiachterstand bij kinderen.
- verhoogde bloedsuikerspiegel, steroïde diabetes, veranderingen in de serumlipidenfractie.
- peesruptuur (achillespees), vooral bij patiënten met stofwisselingsstoornissen zoals: uremie of diabetes mellitus.
- spier zwakte. Verzwakking van spierzwakte en ernstige myasthenische crises kunnen optreden bij patiënten met myasthenia gravis Acute myopathieën kunnen verergeren door het gebruik van niet-depolariserende relaxantia.
- ontwikkeling van maag- en darmzweren; maag- en duodenumperforaties, met peritonitis.
- bloedziekten, vertragingen in genezingsprocessen, toename van het eiwitmetabolisme vergezeld van de "toename van ureum".
- huidveranderingen (atrofie, striae, acne en bloeding).
- in zeldzame gevallen kunnen overgevoeligheidsreacties en huiduitslag optreden. Overgevoeligheidsreacties omvatten shock die kan optreden na parenterale toediening en in het bijzonder bij patiënten met bronchiale astma of die een niertransplantatie hebben ondergaan.
- verminderde immuunrespons en verhoogd risico op infecties. Sommige virale ziekten zoals: waterpokken, herpes simplex en gordelroos kunnen ernstig worden.
- hersenconvulsies, verhoogde intracraniale druk met papiloedeem (pseudotumor cerebri), ontwikkeling of verergering van psychische stoornissen zoals: euforie, stemmingswisselingen, persoonlijkheidsverandering, ernstige depressie, psychose, duizeligheid, hoofdpijn en slaapstoornissen.
- leukocytose (aanvankelijk weer normaal tijdens de behandeling), neiging tot trombocytose, verhoogd risico op trombose.
- troebeling van de lens, verhoogde intraoculaire druk, chorioretinopathie (zie rubriek "Speciale waarschuwingen").
Naleving van de instructies in de bijsluiter verkleint de kans op bijwerkingen.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem van het Italiaanse Geneesmiddelenbureau, website: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse voor meer informatie over de veiligheid van dit geneesmiddel. .
Vervaldatum en retentie
Vervaldatum: zie de vervaldatum die op de verpakking staat vermeld.
De aangegeven houdbaarheidsdatum verwijst naar het product in intacte en correct bewaarde verpakking.
WAARSCHUWING: gebruik het geneesmiddel niet meer na de vervaldatum die staat vermeld op de verpakking.
Niet bewaren boven 30°C.
Buiten het bereik en zicht van kinderen houden.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
SAMENSTELLING
1 tablet bevat:
Actief bestanddeel: methylprednisolon 4 mg.
Hulpstoffen: lactose, maïszetmeel, talk, colloïdaal siliciumdioxide en magnesiumstearaat.
FARMACEUTISCHE VORM EN INHOUD
Tabletten
Doos met 10 tabletten van 4 mg.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
URBASON
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
URBASON 4 mg tabletten
1 tablet bevat: methylprednisolon 4 mg.
URBASON 8 mg tabletten met verlengde afgifte
1 tablet bevat: methylprednisolon 8 mg.
URBASON 4 mg tabletten met verlengde afgifte
1 tablet bevat: methylprednisolon 4 mg.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
URBASON 4 mg tabletten
Ronde tabletten met aan de ene kant "IVD" en aan de andere kant het Hoechst-logo.
URBASON 8 mg tabletten met verlengde afgifte
Ronde tabletten met verlengde afgifte met een maagsapresistente kern en gemarkeerd met "IVR".
URBASON 4 mg tabletten met verlengde afgifte
Ronde tabletten met verlengde afgifte met een maagsapresistente kern en gemarkeerd met "IVM".
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Acute gewrichtsreuma (reumatische koorts) en chronische polyartritis, reumatische en reumatoïde manifestaties van inwendige organen, bloedvaten, ogen, huid en sereus; urine artritis; psoriatische artropathie; bronchiale astma, hooikoorts, serumziekte, overgevoeligheid voor medicijnen en andere allergische en toxisch-allergische reacties; urticaria, gegeneraliseerd eczeem, dermatitis; erytrodermie, gedissemineerde erythematoden, dermatomyositis, pemphigus, exfoliatieve dermatitis; agranulocytose, trombocytopenie, verworven hemolytische anemie, myeloblastose, lymfadenose, lymfogranulomatose; hepatitis, colitis ulcerosa, adrenogenitaal syndroom; nefrotisch syndroom (ook in combinatie met het salureticum Lasix).
04.2 Dosering en wijze van toediening
Over het algemeen begint de behandeling met relatief hoge doses die in de loop van de behandeling worden verlaagd. Na een succesvolle initiële behandeling wordt de dagelijkse dosis geleidelijk verlaagd (met tussenpozen van één tot meerdere dagen) tot de minimumdosis die nodig is om een bevredigend resultaat te bereiken (onderhoudsdosis).
Dosering:
URBASON 4 mg tabletten
Bij bronchiale astma en allergische aandoeningen worden startdoses tussen 16-40 mg per dag aanbevolen, terwijl de onderhoudsdosering meestal 4-16 mg per dag is.
In milde gevallen van chronische polyartritis kan 8-16 mg voldoende zijn om de therapie te starten, terwijl in ernstige gevallen 16-40 mg nodig is. Een dagelijkse dosis van 4-16 mg is meestal voldoende om therapeutisch succes te behouden.
Volgens de meest recente ervaring zijn hoge doses steroïden vereist bij acute reumatische koorts. Daarom moet de dagelijkse dosis van 40-80-120 mg (bij kinderen onder de 14 jaar 1,2-1,6 mg/kg) worden toegediend zolang de bezinkingssnelheid van erytrocyten gedurende ten minste één week normaal is gebleven; daarna wordt de dosering geleidelijk afgebouwd.
Aanzienlijk hogere doseringen, tot dagelijkse doses van 100 mg en meer, zijn soms nodig bij acute erythematoden, pemphigus vulgaris en verschillende hemopathieën.
Bij patiënten die worden behandeld met prednison of prednisolon, is de onderhoudsdosis bij overschakeling op Urbason gewoonlijk 80% van de eerder toegediende dosis, d.w.z. één Urbason 4 mg tablet komt overeen met één prednison 5 mg tablet of prednisolon.
URBASON 8 mg tabletten met verlengde afgifte en URBASON 4 mg tabletten met verlengde afgifte.
Het is zeker mogelijk om direct te beginnen met orale corticosteroïdtherapie met Urbason 8 mg tabletten met verlengde afgifte of Urbason 4 mg tabletten met verlengde afgifte; meestal beginnend met een dagelijkse dosis tussen 20 en 40 mg en dan eventueel zo snel mogelijk overgaan. en naar het oordeel van de arts, bij een lagere dosis.
De onderhoudsdosering moet altijd het minimum zijn waarmee de symptomen onder controle kunnen worden gebracht; de dosisverlaging moet altijd geleidelijk gebeuren.
Wijze van toediening
De tabletten mogen niet op een lege maag worden doorgeslikt.
De tabletten met verlengde afgifte moeten heel worden doorgeslikt, zonder te kauwen.
De verdeling van de dosis gedurende de dag en de duur van de therapie worden overgelaten aan het oordeel van de arts die, zoals bij elke therapie met glucocorticoïden, zal beslissen op basis van de ernst van de ziekte en de verschillende respons van de patiënten op de behandeling .
Het wordt aanbevolen om de eenmaal daagse dosis vroeg in de ochtend in te nemen. Zodra de onderhoudsdosis is vastgesteld, wordt aanbevolen dat de patiënt om de dag een dubbele dagelijkse dosis in één keer in de ochtend inneemt. De duur van de behandeling hangt af van patiënt tot patiënt.
04.3 Contra-indicaties
Het mag niet worden gebruikt bij patiënten met overgevoeligheid voor methylprednisolon of voor andere glucocorticoïden of voor één van de hulpstoffen (zie "6.1 Lijst van hulpstoffen").
Behalve bij vervangings- of spoedbehandelingen, mag Urbason niet worden toegediend bij:
- patiënten met maag- of darmzweren;
- patiënten met botdemineralisatie (osteoporose);
- patiënten met psychische stoornissen;
- patiënten met open en gesloten kamerhoekglaucoom;
- patiënten met herpetische keratitis;
- patiënten met een aantal virale ziekten zoals: waterpokken, herpes simplex en tijdens de virale fase van herpes zoster;
- patiënten met latente of manifeste tuberculose en zelfs als deze slechts wordt vermoed (risico op het ontstaan van de ziekte tot dan latent of verergering van de ziekte die al aan de gang is);
- patiënten met lymfadenopathie na BCG-vaccinaties;
- patiënten die lijden aan amoebiasis;
- patiënten met systemische mycose;
- patiënten met poliomyelitis (met uitzondering van de encefalitische bulbaire vorm);
- gedurende ongeveer 8 weken voor en 2 weken na vaccinaties.
Het wordt aanbevolen dat patiënten die worden behandeld met therapeutische doses glucocorticoïden (anders dan vervangingstherapie) niet worden gevaccineerd omdat de antilichaamrespons onvoldoende kan zijn of omdat ze neurologische complicaties kunnen ontwikkelen. Bij ernstige infecties kan Urbason alleen worden gebruikt in combinatie met een specifieke therapie.
Vanwege het risico op groeiachterstand mag Urbason alleen aan kinderen worden gegeven als dit duidelijk nodig is.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Het gebruik van glucocorticoïden kan het immuunsysteem verzwakken waardoor infecties kunnen ontstaan, sommige micro-organismen kunnen worden geactiveerd met als gevolg de manifestatie van latente infecties.
Glucocorticoïden kunnen de tekenen van een infectie verbergen, waardoor de diagnose van het bestaan of de ontwikkeling ervan moeilijker wordt.
Bij patiënten die systemische glucocorticoïden krijgen, kunnen bepaalde virale ziekten zoals waterpokken, herpes simplex en tijdens de virale fase van herpes zoster ook ernstig worden bij vervangende therapieën.
Systemische behandeling met glucocorticoïden kan chorioretinopathie veroorzaken, wat kan leiden tot visuele stoornissen, waaronder verlies van gezichtsvermogen. Langdurig gebruik van systemische behandeling met glucocorticoïden, zelfs bij lage doses, kan chorioretinopathie veroorzaken (zie rubriek 4.8).
Vanwege het risico op darmperforatie met peritonitis mag Urbason alleen worden gebruikt wanneer dit duidelijk nodig is en met adequate monitoring van patiënten met:
- ernstige colitis ulcerosa met risico op perforatie, abces of purulente ontsteking;
- diverticulitis;
- recente darmanastomosen.
Tenzij ze al waterpokken hebben gehad, moeten kinderen en volwassenen contact vermijden met mensen met waterpokken of gordelroos. Als ze worden blootgesteld aan dergelijke infecties tijdens het gebruik van Urbason, moeten ze onmiddellijk contact opnemen met een arts, zelfs als er geen symptomen zijn.
Patiënten met tuberculinereactiviteit moeten worden gecontroleerd vanwege het risico op reactivering. Bij deze patiënten wordt chemoprofylaxe aanbevolen tijdens langdurige behandeling met glucocorticoïden.
Bij patiënten met myasthenia gravis, vooral als ze hoge doses glucocorticoïden krijgen, bestaat het risico dat de ziekte verergert, meestal binnen de eerste twee weken na aanvang van de behandeling met glucocorticoïden. Het wordt daarom aanbevolen om de dosis Urbason laag te houden aan het begin van de behandeling en geleidelijk te verhogen.
De metabole toestand van diabetespatiënten moet worden gecontroleerd en de antidiabetische therapie moet indien nodig worden aangepast.
In het bijzonder moet na langdurige therapieën met hoge doses van het geneesmiddel rekening worden gehouden met een mogelijke water- en natriumretentie. In dit geval is het noodzakelijk om te zorgen voor een voldoende toevoer van kalium, waarvan het niveau in het bloed moet worden gecontroleerd, en voor een verminderde inname van natrium.
Er moet rekening worden gehouden met een mogelijke verergering van hypertensie en hartaandoeningen, daarom is passende monitoring van patiënten vereist.
Bij langdurige behandeling met glucocorticoïden omvatten medische controles oogheelkundige controles.
Bij patiënten met hypothyreoïdie of patiënten met levercirrose kan de respons op corticosteroïden verhoogd zijn en daarom zijn dosisverlaging en monitoring van de patiënt vereist.
Belangrijke informatie over enkele bestanddelen van URBASON
URBASON bevat lactose.
Patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, Lapp-lactasedeficiëntie of glucose-galactosemalabsorptie dienen dit geneesmiddel niet te gebruiken.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
- Digitalis-glucosiden: de werking van glucosiden kan worden versterkt door hypokaliëmie.
- Diuretica: verhoogde kaliumuitscheiding.
- Antidiabetica: het hypoglykemische effect kan verminderd zijn.
- Cumarinederivaten: antistollingseffecten kunnen worden verminderd.
- Rifampicine, fenytoïne en barbituraten: het effect van corticosteroïden kan verminderd zijn (zie "Bijwerkingen").
- Niet-depolariserende spierverslappers: spierontspanning kan langer duren.
- Oestrogenen (anticonceptiemiddelen): gelijktijdig gebruik van oestrogeen kan het metabolisme van corticosteroïden, waaronder methylprednisolon, verminderen.
- Niet-steroïde ontstekingsremmers verhogen het risico op gastro-intestinale bloedingen.
- Ciclosporine: remming van het metabolisme; verhoogd risico op epileptische aanvallen.
- Allergietesten: huidreacties op allergietesten kunnen onderdrukt worden.
- Diltiazem: remming van het metabolisme van methylprednisolon (CYP3A4) en remming van P-glycoproteïne. De patiënt moet worden gecontroleerd bij het starten van de behandeling met methylprednisolon. Aanpassing van de dosering kan nodig zijn.
04.6 Zwangerschap en borstvoeding
Methylprednisolon passeert de placenta en gaat over in de moedermelk.
Aangezien er zeer beperkte ervaring is met het gebruik van methylprednisolon tijdens de zwangerschap, mag Urbason alleen worden toegediend als dit duidelijk nodig is, onder direct medisch toezicht. Als hoge doses van het geneesmiddel worden toegediend, moet om klinische redenen de borstvoeding worden gestaakt om te voorkomen dat de zuigeling methylprednisolon inneemt met de moedermelk.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Sommige bijwerkingen (verminderd gezichtsvermogen, vertroebeling van de lens, verhoogde oogdruk, duizeligheid en migraine) kunnen het concentratie- en reactievermogen van patiënten verminderen, wat een risico vormt in al die situaties waarin deze vaardigheden van bijzonder belang zijn (autorijden of machines gebruiken).
04.8 Bijwerkingen
Tijdens behandeling met corticosteroïden, vooral bij intensieve en langdurige behandelingen, kunnen enkele van de volgende effecten optreden:
- abnormale verdeling van lichaamsvet zoals in het geval van maanfacies, zwaarlijvigheid en zeer zelden ook een verdeling van vet in het wervelkanaal (epiduraal) of in de borstholte (epicardiaal, mediastinum); gewichtstoename.
- natriumretentie en ophoping van water in de weefsels, verhoogde kaliumuitscheiding met mogelijke hypokaliëmie, verhoogde longcongestie bij patiënten met een hartaanval, hypertensie.
- verandering in de afscheiding van geslachtshormonen (mogelijke amenorroe, toegenomen haargroei, verminderde seksuele potentie); inactivatie of atrofie van corticoadrenale activiteit, groeiachterstand bij kinderen.
- verhoogde bloedsuikerspiegel, steroïde diabetes, veranderingen in de serumfractie van lipiden.
- ruptuur van de pees (Achillespees), vooral bij patiënten met stofwisselingsstoornissen zoals: uremie of diabetes mellitus.
- spier zwakte.
- verergering van spierzwakte en ernstige myasthenische crises kunnen optreden bij patiënten met myasthenia gravis Acute myopathieën kunnen verergeren door het gebruik van niet-depolariserende relaxantia.
- ontwikkeling van maag- en darmzweren; maag- en duodenumperforaties, met peritonitis.
- bloedziekten, vertragingen in het genezingsproces, toename van het eiwitmetabolisme vergezeld van de "toename van" ureum.
- huidveranderingen (atrofie, striae, acne en bloeding).
- in zeldzame gevallen kunnen overgevoeligheidsreacties en huiduitslag optreden. Overgevoeligheidsreacties omvatten shock die kan optreden na parenterale toediening en in het bijzonder bij patiënten met bronchiale astma of die een niertransplantatie hebben ondergaan.
- verminderde immuunrespons en verhoogd risico op infecties. Sommige virale ziekten zoals: waterpokken, herpes simplex en gordelroos kunnen ernstig worden.
- hersenconvulsies, verhoogde intracraniale druk met papiloedeem (pseudotumor cerebri), ontwikkeling of verergering van psychische stoornissen zoals: euforie, stemmingswisselingen, persoonlijkheidsverandering, ernstige depressie, psychose, duizeligheid, hoofdpijn en slaapstoornissen.
- leukocytose (aanvankelijk wordt het weer normaal tijdens de behandeling), neiging tot trombocytose, verhoogd risico op trombose.
- vertroebeling van de lens, verhoogde intraoculaire druk, chorioretinopathie (zie rubriek 4.4).
Melding van vermoedelijke bijwerkingen.
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "Italiaans Geneesmiddelenbureau , website: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Er zijn geen gevallen bekend van acute intoxicatie. Indien nodig moet echter een maagspoeling worden uitgevoerd en moeten eventuele symptomen worden gecontroleerd.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: systemische corticosteroïden, glucocorticoïden.
ATC-code: H02AB04.
Werkingsmechanisme:
Methylprednisolon heeft een dosisafhankelijke invloed op het metabolisme in bijna alle weefsels; in het fysiologische concentratiebereik zijn deze effecten essentieel om de homeostase van het lichaam in rust en onder stressvolle omstandigheden te handhaven en ook om het immuunsysteem te reguleren.
Vervangingstherapie:
Fysiologische doses methylprednisolon vervangen het endogene cortisol in geval van bijnierschorsdisfunctie; bij deze doseringen is er ook een invloed op het metabolisme van koolhydraten, eiwitten en lipiden. 8 mg methylprednisolon komt overeen met 40 mg cortisol. Gezien de bijna totale afwezigheid van mineralocorticoïde effecten van methylprednisolon, moet een mineralocorticoïde gelijktijdig worden toegediend in vervangende therapieën wanneer er een totale blokkering van de adrenocorticotrope functies is.
Wanneer het nodig is om hoge doses Urbason toe te dienen als vervangingstherapie, heeft methylprednisolon een snel ontstekingsremmend effect en een vertraagd immunosuppressief effect.
Het remt chemotaxis en de activiteit van cellen van het immuunsysteem, evenals de afgifte en effecten van mediatoren van immuunreacties, bijvoorbeeld het lysosomale enzym en leukotriënen. Bij bronchiale obstructie worden de effecten van bèta-mimetische luchtwegverwijders versterkt.
Lange en hooggedoseerde therapieën veroorzaken een vermindering van de functie van het immuunsysteem en het corticale deel van de bijnier.
De mineralotrope effecten van methylprednisolon zijn zeer beperkt.
Effecten op obstructieve luchtwegpathologieën:
Het effect van methylprednisolon bij deze pathologieën is volledig toe te schrijven aan zijn vermogen om ontstekingsprocessen te remmen, aan de onderdrukking of preventie van slijmvliesoedeem, aan de remming van bronchoconstrictie, aan de remming of beperking van de slijmproductie en ook aan de vermindering van de viscositeit van de slijm zelf. Deze effecten zijn gebaseerd op het volgende mechanisme: membraanstabilisatie, verbetering van de bronchiale spierrespons op sympathicomimetische b2, vermindering van type I-reacties na één week therapie.
Duur van effecten:
De duur van het effect is langer dan de verblijftijd in het serum; in feite houdt het effect aan voor tussenliggende doses, van 12 tot 36 uur na orale of intraveneuze toediening.
05.2 Farmacokinetische eigenschappen
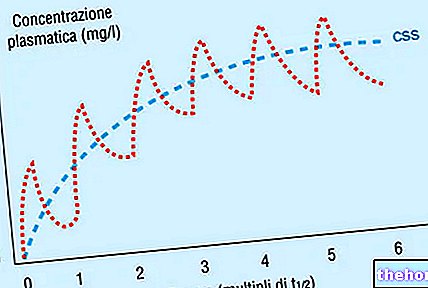
Na orale toediening van Urbason wordt de piekserumconcentratie van methylprednisolon binnen 1,5 uur bereikt en is de t½ ongeveer 2/3 uur. 77% van het medicijn is gebonden aan eiwitten, ongeacht de dosering. De binding vindt plaats met albumine en niet met transcortine.
Methylprednisolon wordt voornamelijk in de lever gemetaboliseerd, de metabolieten (11-keto- en 20-hydroxyderivaten) zijn inactief als hormonen en worden voornamelijk via de nieren uitgescheiden (ongeveer 85% van de toegediende dosis verschijnt binnen 10 uur in de urine en ongeveer 10% in de feces .) Na orale toediening van Urbason wordt minder dan 10% methylprednisolon onveranderd uitgescheiden.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Acute giftigheid:
De LD50 van oraal methylprednisolon is hoger dan 40 mg/kg bij honden, terwijl het bij ratten hoger is dan 4000 mg/kg lichaamsgewicht.
Chronische toxiciteit:
De volgende farmacodynamische effecten zijn waargenomen in dierstudies: polycytemie, lymfopenie, atrofie van de thymus en het corticale deel van de bijnier en verhoogde leveropslag van glycogeen.
Chronische behandelingen met hoge doses (3-10 mg/kg lichaamsgewicht per dag) induceren de vermindering van de immuunrespons, verminderen de activiteit van het beenmerg, veroorzaken atrofie van de skeletspieren, beïnvloeden het gewicht van de testikels en eierstokken (honden: verminderd testisgewicht, rat: verhoogd testis- en ovariumgewicht) en verminderd gewicht van de prostaat (hond) en spermatocyst (rat), polydipsie, diarree en verergering van algemene aandoeningen.
Carcinogenese
Er zijn geen dierstudies op lange termijn met betrekking tot de carcinogene effecten van methylprednisolon.
Mutagenese
De mutageniteit van methylprednisolon is niet volledig onderzocht. De AMES-test is negatief.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
URBASON 4 mg tabletten
lactose, maïszetmeel, talk, colloïdaal siliciumdioxide en magnesiumstearaat.
URBASON 8 mg tabletten met verlengde afgifte
maïszetmeel, lactose, talk, magnesiumstearaat, sucrose, arabische gom, gelatine, vloeibare glucose, calciumcarbonaat, glycerine, methacrylzuurcopolymeer, triethylcitraat, E 127, E 110, polyethyleenglycol 6000.
URBASON 4 mg tabletten met verlengde afgifte
maïszetmeel, lactose, talk, magnesiumstearaat, sucrose, arabische gom, gelatine, vloeibare glucose, calciumcarbonaat, glycerine, methacrylzuurcopolymeer, triethylcitraat, E 104, polyethyleenglycol 6000.
06.2 Incompatibiliteit
Er zijn geen chemisch-fysische onverenigbaarheden bekend.
06.3 Geldigheidsduur
URBASON 4 mg tabletten: 3 jaar.
URBASON 8 mg tabletten met verlengde afgifte en URBASON 4 mg tabletten met verlengde afgifte: 2 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
URBASON 4 mg tabletten
Niet bewaren boven 30°C.
URBASON 8 mg tabletten met verlengde afgifte en 4 mg tabletten met verlengde afgifte
Ze zijn niet voorzien onder normale omgevingsomstandigheden.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
URBASON 4 mg tabletten
Blisterverpakkingen van ondoorzichtig wit PVC en aluminium, hitteverzegeld; 10 tabletten.
URBASON 8 mg tabletten met verlengde afgifte
Blisterverpakkingen van ondoorzichtig wit PVC en aluminium, hitteverzegeld; 10 tabletten met verlengde afgifte.
URBASON 4 mg tabletten met verlengde afgifte
Blisterverpakkingen van ondoorzichtig wit PVC en aluminium, hitteverzegeld; 10 tabletten met verlengde afgifte.
06.6 Instructies voor gebruik en verwerking
Het type primaire en/of secundaire verpakking bevat geen specifieke instructies voor gebruik en gebruik.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Sanofi S.p.A. - Viale L. Bodio, 37 / B - Milaan
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
URBASON 4 mg tabletten A.I.C. nr.:024001012
URBASON 8 mg tabletten met verlengde afgifte A.I.C. nr.:024001036
URBASON 4 mg tabletten met verlengde afgifte A.I.C. nr.:024001051
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
URBASON 4 mg-tabletten: 27.12.1966 / 01.06.2010
URBASON 8 mg tabletten met verlengde afgifte: 10.11.1965 / 01.06.2010
URBASON 4 mg tabletten met verlengde afgifte: 20.4.1979 / 01.06.2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
maart 2015