Wat is CYSTAGON?
CYSTAGON is een geneesmiddel dat cysteamine als het werkzame bestanddeel bevat. Het komt in de vorm van capsules (50 en 150 mg).
Waar wordt CYSTAGON voor gebruikt?
CYSTAGON wordt gebruikt voor de behandeling van patiënten met nefropathische (nier)cystinose. Cystinose is een zeldzame erfelijke ziekte die wordt veroorzaakt doordat cystine zich in sommige cellen ophoopt, waardoor ze niet normaal kunnen functioneren. Deze opbouw veroorzaakt nierproblemen en verspreidt zich naar andere delen van het lichaam, waaronder de ogen, sommige klieren (schildklier, pancreas, geslachtsklieren), het centrale zenuwstelsel, spieren en lever. De ziekte manifesteert zich door groeimoeilijkheden.
Het geneesmiddel is alleen op recept verkrijgbaar.
Hoe wordt CYSTAGON gebruikt?
CYSTAGON moet worden gestart onder toezicht van een arts die ervaring heeft met de behandeling van cystinose.
De leukocytenspiegels van cystine moeten worden gemeten om de dosering van het geneesmiddel aan te passen.
Voor kinderen tot 12 jaar is de aanbevolen dosis 1,30 g/m2/dag verdeeld over vier doses
elke dag.
Voor patiënten ouder dan 12 jaar en met een gewicht van meer dan 50 kilogram wordt een dosis van 2 g/dag aanbevolen, verdeeld over vier dagelijkse doses. De aanvangsdoses moeten overeenkomen met 1/4 - 1/6 van de beoogde einddoses. De aanvangsdoses moeten geleidelijk worden verhoogd in de loop van 4-6 weken.
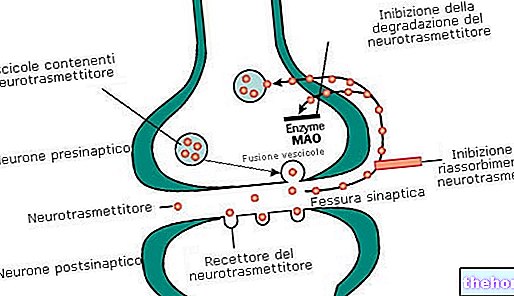
Hoe werkt CYSTAGON?
CYSTAGON reageert met cystine om cysteïne en een gemengd disulfide van cysteamine en cystine te vormen.
Dit gemengde disulfide wordt vervolgens uit de cellen geëxtraheerd door het transportsysteem van een ander aminozuur (lysine). De hoeveelheid cystine in de organen wordt verminderd, waardoor de schade wordt beperkt.
Hoe is CYSTAGON onderzocht?
CYSTAGON is getest in drie klinische onderzoeken met 234 patiënten over een periode van twaalf jaar. Bij de onderzoeken waren kinderen betrokken en recentelijk nieuwe patiënten geworven, waarbij twee verschillende doseringen werden getest. Aangezien dit een zeer ernstige aandoening is, was het om ethische redenen niet mogelijk om CYSTAGON rechtstreeks te vergelijken met een placebo. In plaats daarvan werd de vergelijking uitgevoerd op een groep patiënten die werd behandeld met een placebo, als onderdeel van een ander niet-gerelateerd onderzoek. De onderzoeken waren gericht op de nierfunctie en de overlevings- en groeipercentages van de patiënt.
Welk voordeel heeft CYSTAGON aangetoond tijdens de onderzoeken?
Uit de drie onderzoeken bleek dat CYSTAGON nierziekte en de noodzaak van dialyse of niertransplantatie vertraagt als de behandeling op jonge leeftijd wordt gestart door mensen met een goede nierfunctie. Het medicijn verbetert ook de overlevings- en groeisnelheid bij kinderen die het gebruiken.
Welk risico is verbonden aan CYSTAGON?
De meest voorkomende bijwerkingen van CYSTAGON zijn voornamelijk gerelateerd aan het spijsverteringsstelsel.
De meest gemelde bijwerkingen (die optreden bij meer dan één op de 10 patiënten) zijn: anorexia (verlies van eetlust), misselijkheid, braken, diarree, lethargie en pyrexie (koorts). Zie de bijsluiter voor de volledige lijst van alle gemelde bijwerkingen van CYSTAGON.
CYSTAGON mag niet worden gebruikt bij mensen die mogelijk overgevoelig (allergisch) zijn voor cysteamine, voor de andere bestanddelen van het geneesmiddel of voor penicillamine. CYSTAGON mag niet worden gegeven aan vrouwen die borstvoeding geven, zwanger zijn of een vermoeden hebben van zwangerschap (vooral tijdens de eerste drie maanden), tenzij dit absoluut noodzakelijk is.
Waarom is CYSTAGON goedgekeurd?
Cystinose is een zeldzame en dodelijke ziekte, en CYSTAGON wordt beschouwd als een nuttig geneesmiddel dat
het heeft geen alternatief. Het Comité voor geneesmiddelen voor menselijk gebruik (CHMP) was van oordeel dat de voordelen van CYSTAGON groter zijn dan de risico's en adviseerde om een vergunning voor het in de handel brengen van het geneesmiddel te verlenen.
CYSTAGON is in uitzonderlijke omstandigheden goedgekeurd, aangezien het, zoals het wordt gebruikt voor:
om een zeldzame ziekte te behandelen, kon op het moment van goedkeuring geen nadere informatie over het geneesmiddel worden verkregen.Aangezien de fabrikant de gevraagde aanvullende informatie heeft verstrekt, zijn de uitzonderlijke omstandigheden op 17 april 2007 geëindigd.
Meer informatie over CYSTAGON
Op 23 juni 1997 verleende de Europese Commissie aan Orphan Europe een in de hele Europese Unie geldige "vergunning voor het in de handel brengen" van CYSTAGON, die op 23 juni 2002 en op 23 juni 2007 werd verlengd.
De volledige versie van de evaluatie (EPAR) vindt u hier.
Laatste update van dit overzicht: 06-2007
De informatie over CYSTAGON - cysteamine die op deze pagina wordt gepubliceerd, kan verouderd of onvolledig zijn. Zie voor een correct gebruik van deze informatie de pagina Disclaimer en nuttige informatie.