Actieve ingrediënten: Febuxostat
ADENURIC 80 mg filmomhulde tabletten
ADENURIC 120 mg filmomhulde tabletten
Waarom wordt Adenuric gebruikt? Waar is het voor?
ADENURIC-tabletten bevatten de werkzame stof febuxostat en worden gebruikt voor de behandeling van jicht, een ziekte die gepaard gaat met te veel urinezuur (uraat) in het lichaam. Bij sommige mensen kan de hoeveelheid urinezuur die zich ophoopt in het bloed te hoog worden. in oplossing blijven.In dit geval kunnen zich uraatkristallen vormen in en rond de gewrichten en nieren.Deze kristallen kunnen plotselinge, hevige pijn, roodheid, warmte en zwelling in een gewricht veroorzaken (jichtaanval). Indien onbehandeld, kunnen zich grotere afzettingen, tophi genaamd, vormen in en rond de gewrichten. Tophi kan gewrichten en botten beschadigen.
ADENURIC werkt door het urinezuurgehalte te verlagen. Het handhaven van lage urinezuurspiegels door ADENURIC eenmaal per dag in te nemen, voorkomt de ophoping van kristallen en vermindert na verloop van tijd de symptomen. Als de urinezuurspiegels lang genoeg laag worden gehouden, kan de tophi ook worden geresorbeerd.
ADENURIC 120 mg tabletten worden ook gebruikt voor de behandeling en preventie van hoge urinezuurspiegels in het bloed, die kunnen optreden bij chemotherapie voor bloedkanker. Kankercellen worden vernietigd tijdens chemotherapiebehandeling en het urinezuurgehalte in het bloed neemt toe, tenzij de vorming van dit zuur kan worden voorkomen.
ADENURIC is voor volwassenen.
Contra-indicaties Wanneer Adenuric niet mag worden gebruikt
Gebruik ADENURIC niet:
- Als u allergisch bent voor febuxostat of voor één van de andere bestanddelen van dit geneesmiddel
Voorzorgsmaatregelen bij gebruik Wat u moet weten voordat u Adenuric inneemt
Praat met uw arts voordat u ADENURIC inneemt:
- Als u hartfalen of andere hartproblemen heeft of heeft gehad
- Als u een nieraandoening heeft of heeft gehad en/of ernstige allergische reacties op allopurinol (een geneesmiddel tegen jicht)
- Als u een leverziekte of leverfunctietestafwijkingen heeft of heeft gehad
- Als u verhoogde urinezuurspiegels heeft als gevolg van het syndroom van Lesch-Nyhan (een zeldzame erfelijke aandoening waarbij er te veel urinezuur in het bloed zit)
- Als u schildklierproblemen heeft.
Als allergische reacties op ADENURIC optreden, stop dan met het innemen van het geneesmiddel. Mogelijke symptomen van allergische reacties kunnen zijn:
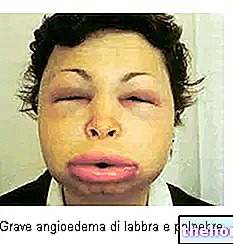
- huiduitslag, waaronder ernstige vormen (bijv. blaren, bulten, jeukende uitslag, exfoliatieve uitslag), jeuk
- zwelling van de ledematen of het gezicht
- moeite met ademhalen
- koorts met gezwollen lymfeklieren
- maar ook ernstige, levensbedreigende allergische aandoeningen met hart- en bloedsomloopstilstand.
Uw arts kan besluiten uw behandeling met Adenuric definitief te stoppen.
Zeldzame, levensbedreigende huiduitslag (Stevens-Johnson-syndroom) is gemeld bij het gebruik van ADENURIC en verscheen aanvankelijk op de romp als roodachtige vlekken of ronde vlekken, vaak met blaren in het midden. Ze kunnen ook zweren in de mond, keel, neus, geslachtsorganen en conjunctivitis (rode en gezwollen ogen) De uitslag kan evolueren tot wijdverbreide blaarvorming of vervelling van de huid.
Als u het syndroom van Stevens-Johnson heeft ontwikkeld bij het gebruik van febuxostat, mag de behandeling met ADENURIC niet meer worden hervat.Als u huiduitslag of deze huidsymptomen heeft gekregen, raadpleeg dan onmiddellijk uw arts en vertel hem dat u met dit geneesmiddel wordt behandeld. .
Als u momenteel een jichtaanval heeft (plotseling begin van ernstige pijn, gevoeligheid, roodheid, warmte en zwelling van één gewricht), wacht dan tot de jichtaanval stopt voordat u met de behandeling met ADENURIC begint.
Bij sommige mensen kunnen jichtaanvallen oplaaien aan het begin van bepaalde therapieën die worden gebruikt om de urinezuurspiegels onder controle te houden. Niet alle mensen ervaren exacerbaties, maar u kunt ook een exacerbatie ervaren wanneer u ADENURIC gebruikt, vooral tijdens de eerste paar weken of maanden van de behandeling. Het is belangrijk dat u ADENURIC blijft gebruiken, zelfs als u een opflakkering krijgt, aangezien ADENURIC blijft werken om uw urinezuurspiegel te verlagen. Als u doorgaat met het dagelijks innemen van ADENURIC, zullen de opflakkeringen na verloop van tijd minder vaak voorkomen en steeds minder pijnlijk zijn.
Uw arts zal, indien nodig, vaak andere geneesmiddelen voorschrijven om de symptomen van opflakkeringen (zoals pijn en zwelling in een 'gewricht') te helpen voorkomen of behandelen.
Bij patiënten met zeer hoge urinezuurspiegels (bijv. patiënten die chemotherapie krijgen), kan behandeling met geneesmiddelen die de urinezuurspiegels verlagen ertoe leiden dat xanthine zich ophoopt in de urinewegen met mogelijke steenvorming, hoewel dit niet is waargenomen bij patiënten die worden behandeld met ADENURIC voor tumoren. Lysis syndroom.
Uw arts kan bloedonderzoeken laten uitvoeren om te controleren of uw lever normaal functioneert.
Kinderen en adolescenten
Geef dit geneesmiddel niet aan kinderen jonger dan 18 jaar omdat de veiligheid en werkzaamheid niet zijn vastgesteld.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Adenuric veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken, ook als u geneesmiddelen gebruikt die u zonder voorschrift kunt krijgen.
Het is erg belangrijk dat u uw arts of apotheker vertelt als u een geneesmiddel gebruikt dat een van de volgende stoffen bevat, aangezien deze een wisselwerking kunnen hebben met ADENURIC en uw arts mogelijk passende maatregelen wil overwegen:
- Mercaptopurine (gebruikt om kanker te behandelen)
- Azathioprine (gebruikt om de immuunrespons te verminderen)
- Theofylline (gebruikt om astma te behandelen)
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
Het is niet bekend of ADENURIC schadelijk kan zijn voor een ongeboren baby. ADENURIC mag niet worden gebruikt tijdens de zwangerschap. Het is niet bekend of ADENURIC in de moedermelk terechtkomt. U mag ADENURIC niet gebruiken als u borstvoeding geeft of van plan bent dit te doen.
Als u zwanger bent of borstvoeding geeft, denkt zwanger te zijn of zwanger wilt worden, vraag dan uw arts of apotheker om advies voordat u dit geneesmiddel inneemt.
Rijvaardigheid en het gebruik van machines
Houd er rekening mee dat u zich duizelig, slaperig, wazig zien, gevoelloosheid of tintelingen kunt voelen tijdens de behandeling, en als deze symptomen optreden, mag u niet autorijden of machines bedienen.
ADENURIC bevat lactose
ADENURIC-tabletten bevatten lactose (een soort suiker). Als u weet dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt.
Dosis, wijze en tijdstip van toediening Hoe Adenuric te gebruiken: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
- De gebruikelijke dosering is één tablet per dag. Op de achterkant van de strip staan de dagen van de week, zodat u kunt controleren of u uw dosis elke dag heeft ingenomen.
- De tabletten moeten via de mond worden ingenomen. Je kunt ze in de buurt van of weg van maaltijden nemen.
Chronische hyperurikemie met uraatafzetting ADENURIC is verkrijgbaar als tablet van 80 mg of 120 mg. Uw arts heeft u de meest geschikte dosering voorgeschreven.
Blijf ADENURIC elke dag innemen, ook als u geen opflakkering of jichtaanval heeft.
Preventie en behandeling van verhoogde urinezuurspiegels bij patiënten die chemotherapie ondergaan ADENURIC is verkrijgbaar als tabletten van 120 mg.
Begin twee dagen voor de chemotherapie met het innemen van ADENURIC en blijf het innemen volgens het advies van uw arts. Het gebruik is meestal van korte duur.
Overdosering Wat moet u doen als u te veel Adenuric heeft ingenomen?
Wat u moet doen als u meer van ADENURIC heeft ingenomen dan u zou mogen
In geval van accidentele overdosering, vraag uw arts wat u moet doen of neem contact op met de dichtstbijzijnde eerste hulpafdeling.
Wat u moet doen wanneer u bent vergeten ADENURIC . in te nemen
Als u bent vergeten een dosis ADENURIC in te nemen, neem deze dan in zodra u het zich realiseert, tenzij het bijna tijd is voor uw volgende dosis. Sla in dit geval de gemiste dosis over en neem de volgende dosis op het geplande tijdstip. Neem geen dubbele dosis om een vergeten dosis in te halen.
Als u stopt met het innemen van ADENURIC
Stop niet met het innemen van ADENURIC zonder toestemming van uw arts, ook niet als u zich beter voelt. Als u stopt met het innemen van ADENURIC, kunnen uw urinezuurspiegels stijgen en kunnen uw symptomen verergeren door de vorming van nieuwe uraatkristallen in en rond uw gewrichten en nieren.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Adenuric
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Stop met het innemen van het geneesmiddel en neem onmiddellijk contact op met uw arts of ga naar de dichtstbijzijnde spoedeisende hulp als u de volgende zeldzame bijwerkingen krijgt (kunnen optreden bij maximaal 1 op de 1.000 mensen), aangezien er een ernstige allergische reactie kan volgen:
- anafylactische reacties, overgevoeligheid voor geneesmiddelen (zie ook rubriek "Waarschuwingen en voorzorgsmaatregelen")
- Levensbedreigende huiduitslag die wordt gekenmerkt door blaarvorming en vervelling van de huid en inwendige oppervlakken van de lichaamsholte, bijv. mond en geslachtsdelen, pijnlijke zweren in de mond en/of genitale gebieden, vergezeld van koorts, keelpijn en vermoeidheid (Stevens-Johnson-syndroom / toxische epidermale necrolyse), of vergrote lymfeklieren, vergrote lever, hepatitis (tot leverfalen), verhoogd aantal witte bloedcellen (geneesmiddelreactie met eosinofilie en systemische symptomen - DRESS).
- gegeneraliseerde uitslag
Vaak voorkomende bijwerkingen (komen voor bij minder dan 1 op de 10 gebruikers) zijn:
- afwijkingen in leverfunctietestresultaten
- diarree
- hoofdpijn
- uitslag (inclusief verschillende soorten huiduitslag, zie hieronder onder "soms" en "zelden")
- misselijkheid
- verhoogde symptomen van jicht
- plaatselijke zwelling door vochtophoping in de weefsels (oedeem)
Andere bijwerkingen die hierboven niet zijn genoemd, worden hieronder vermeld.
Soms voorkomende bijwerkingen (komen voor bij minder dan 1 op de 100 gebruikers) zijn:
- verminderde eetlust, veranderingen in de bloedsuikerspiegel (diabetes) een symptoom hiervan kan zijn overmatige dorst, verhoogde bloedvetspiegels, gewichtstoename
- verlies van libido (seksueel verlangen)
- slaapproblemen, slaperigheid
- duizeligheid, gevoelloosheid, tintelingen, verminderd of veranderd tastgevoel (hypo-esthesie, hemiparese of paresthesie), veranderde smaak (dysgeusie), verminderd reukvermogen (hyposmie)
- afwijkingen in ECG-sporen, onregelmatige of snelle hartslag, perceptie van hartslag (hartkloppingen)
- blozen of roodheid (bijv. roodheid van het gezicht of de nek), verhoogde bloeddruk, bloeding (bloeding, alleen waargenomen bij patiënten die chemotherapie ondergaan voor bloedaandoeningen)
- hoesten, kortademigheid, pijn op de borst, ontsteking van de neus en/of keel (luchtweginfectie), bronchitis
- droge mond, buikpijn of ongemak, overmatig gas, brandend maagzuur / indigestie, constipatie, frequentere stoelgang, braken, maagklachten
- jeuk, netelroos, ontsteking van de huid, verkleuring van de huid, kleine rode of paarse vlekken op de huid, kleine platte rode vlekken op de huid, rood gebied op de huid bedekt met kleine samenvloeiende bultjes, huiduitslag, roodheid en vlekken op de huid, andere huidaandoeningen
- spierkrampen, spierzwakte, spier- of gewrichtspijn, bursitis of artritis (gewrichtsontsteking die gewoonlijk gepaard gaat met pijn, zwelling en/of stijfheid), pijn in extremiteit, rugpijn, spierspasmen
- bloed in de urine, vaker plassen, afwijkende urinetestresultaten (verhoogd eiwitgehalte in de urine) verminderd vermogen van de nieren om goed te functioneren
- vermoeidheid, pijn op de borst, ongemak op de borst
- stenen in de galblaas of galwegen (cholelithiasis)
- verhoogde bloedspiegels van thyroïdstimulerend hormoon (TSH)
- veranderingen in bloed biochemische tests of aantal rode bloedcellen of bloedplaatjes (veranderingen in resultaten van bloedonderzoek)
- nierstenen
- moeite met het krijgen van een erectie
Zeldzame bijwerkingen (kunnen voorkomen bij maximaal 1 op de 1000 mensen) zijn:
- spierbeschadiging, een aandoening die in zeldzame gevallen ernstig kan zijn. Er kunnen zich spierproblemen ontwikkelen en vooral als u zich onwel voelt of tegelijkertijd hoge koorts heeft, kan dit het gevolg zijn van een abnormale afbraak van spiercellen. Neem onmiddellijk contact op met uw arts als u spierpijn, gevoeligheid of zwakte ervaart
- duidelijke zwelling van de diepere huidlagen, vooral rond de lippen, ogen, geslachtsdelen, handen, voeten of tong, met mogelijk plotselinge ademhalingsmoeilijkheden
- hoge koorts geassocieerd met mazelenachtige huiduitslag, vergrote lymfeklieren, vergrote lever, hepatitis (tot leverfalen), verhoogd aantal witte bloedcellen (leukocytose, al dan niet geassocieerd met eosinofilie)
- roodheid van de huid (erytheem), huiduitslag in verschillende soorten (bijvoorbeeld jeukende, witte vlekken, blaren, pus bevattende blaren, vervellen van de huid, mazelenachtige uitslag), diffuus erytheem, necrose en blaarvorming van de opperhuid en slijmvliezen , resulterend in afschilfering en mogelijke sepsis (Stevens-Johnson-syndroom / toxische epidermale necrolyse)
- nervositeit
- dorst
- oorsuizen
- wazig zien, verandering in het gezichtsvermogen
- haaruitval
- buccale ulceratie
- ontsteking van de alvleesklier: veel voorkomende symptomen zijn buikpijn, misselijkheid en braken
- toegenomen zweten
- verminderd gewicht, toegenomen eetlust, ongecontroleerd verlies van eetlust (anorexia)
- spier- en/of gewrichtsstijfheid
- abnormaal laag aantal bloedcellen (witte bloedcellen of rode bloedcellen of bloedplaatjes)
- aandrang om te plassen
- veranderingen of verminderde hoeveelheden in de urine als gevolg van ontsteking in de nieren (tubulo-interstitiële nefritis)
- ontsteking van de lever (hepatitis)
- geel worden van de huid (geelzucht)
- lever schade
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
- Gebruik het geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos en op de folie van de blisterverpakking na "EXP". De vervaldatum verwijst naar de laatste dag van de maand.
- Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Wat bevat ADENURIC
Het werkzame bestanddeel is febuxostat.
Elke tablet bevat 80 mg of 120 mg febuxostat.
De hulpstoffen zijn:
Tabletkern: lactosemonohydraat, microkristallijne cellulose, magnesiumstearaat, hydroxypropylcellulose, croscarmellosenatrium, colloïdaal silicahydraat.
Tabletcoating: Opadry II geel, 85F42129 bevattende: polyvinylalcohol, titaandioxide (E171), macrogol type 3350, talk, geel ijzeroxide (E172).
Hoe ziet ADENURIC eruit en hoeveel zit er in een verpakking?
ADENURIC filmomhulde tabletten zijn lichtgeel/geel en capsulevormig.De filmomhulde tabletten van 80 mg hebben aan één kant de inscriptie '80'. De 120 mg filmomhulde tabletten hebben aan één kant de inscriptie "120".
ADENURIC 80 mg en 120 mg zijn verpakt in doorzichtige blisterverpakkingen (Aclar/PVC/Aluminium) met 14 tabletten.
ADENURIC 80 mg en 120 mg is verkrijgbaar in verpakkingen van 14, 28, 42, 56, 84 en 98 filmomhulde tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
ADENURIC 80 MG TABLETTEN BEDEKT MET FILM
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet bevat 80 mg febuxostat.
Hulpstof(fen) met bekende effecten:
Elke tablet bevat 76,50 mg lactose (als monohydraat)
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Filmomhulde tablet (tablet).
Lichtgele/gele, filmomhulde, capsulevormige tabletten met aan één kant "80".
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Behandeling van chronische hyperurikemie met uraatafzetting (inclusief een voorgeschiedenis van of aanwezigheid van tophi en/of jichtartritis).
ADENURIC is geïndiceerd bij volwassenen.
04.2 Dosering en wijze van toediening
Dosering
De aanbevolen orale dosering van ADENURIC is 80 mg eenmaal daags en kan zowel bij als buiten de maaltijd worden ingenomen. Bij serumurinezuurwaarden > 6 mg/dl (357 mol/l) na 2-4 weken, kan ADENURIC 120 mg eenmaal daags beschouwd worden.
ADENURIC werkt snel genoeg om een nieuwe bepaling van serumurinezuur na 2 weken mogelijk te maken.Het therapeutische doel is om de serumurinezuurspiegel te verlagen en te handhaven onder 6 mg/dL (357 μmol/L).
Voor de profylaxe van exacerbaties van jicht wordt een behandelingsperiode van ten minste 6 maanden aanbevolen (zie rubriek 4.4).
Ouderen
Bij ouderen is geen dosisaanpassing nodig (zie rubriek 5.2).
Nierfunctiestoornis
De werkzaamheid en veiligheid van het geneesmiddel zijn niet volledig vastgesteld bij patiënten met een ernstige nierfunctiestoornis (creatinineklaring
Er is geen dosisaanpassing nodig bij patiënten met een lichte of matige nierfunctiestoornis.
leverfunctiestoornis
De werkzaamheid en veiligheid van febuxostat zijn niet onderzocht bij patiënten met een ernstige leverfunctiestoornis (Child-Pugh-klasse C).
De aanbevolen dosis voor patiënten met een lichte leverfunctiestoornis is 80 mg. Er is beperkte informatie over het gebruik van het geneesmiddel bij patiënten met een matige leverfunctiestoornis.
Pediatrische populatie
De veiligheid en werkzaamheid van ADENURIC bij kinderen jonger dan 18 jaar zijn niet vastgesteld.Er zijn geen gegevens beschikbaar.
Wijze van toediening
oraal gebruik
ADENURIC moet oraal worden toegediend en kan met of zonder voedsel worden ingenomen.
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen (zie ook rubriek 4.8).
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Cardiovasculaire aandoeningen
Behandeling met febuxostat wordt niet aanbevolen bij patiënten met ischemische hartziekte of congestief hartfalen.
Er was een numeriek hogere incidentie van door de onderzoeker gerapporteerde cardiovasculaire APTC-voorvallen (eindpunten gedefinieerd door de Anti-Platelet Trialists "Collaboration) (inclusief cardiovasculaire sterfte, niet-fataal myocardinfarct, niet-fatale beroerte) in de febuxostat-groep vergeleken met die behandeld met allopurinol in de APEX- en FACT-onderzoeken (1,3 versus 0,3 voorvallen per 100 patiëntjaren), maar niet in de CONFIRMS-studie (zie rubriek 5.1 voor gedetailleerde onderzoekskenmerken). De incidentie van door de onderzoeker gerapporteerde cardiovasculaire APTC-voorvallen in de gepoolde fase 3-onderzoeken (APEX, FACT en CONFIRMS) was 0,7 versus 0,6 voorvallen per 100 patiëntjaren.
In de langetermijnextensieonderzoeken waren de incidenties van door de onderzoeker gerapporteerde APTC-voorvallen respectievelijk 1,2 en 0,6 voorvallen per 100 patiëntjaren voor febuxostat en allopurinol. Er werden geen statistisch significante verschillen waargenomen en er werd geen causaal verband met febuxostat vastgesteld. Risicofactoren die voor deze patiënten werden geïdentificeerd, waren een klinische voorgeschiedenis van atherosclerotische ziekte en/of myocardinfarct, of congestief hartfalen.
Allergie / overgevoeligheid voor het medicijn
Zeldzame meldingen van ernstige allergische/overgevoeligheidsreacties waaronder levensbedreigend Stevens-Johnson-syndroom, toxische epidermale necrolyse en acute anafylactische reacties/shock zijn verzameld in de postmarketingperiode. In de meeste gevallen traden deze reacties op tijdens de eerste maand van de behandeling met febuxostat. Sommige, maar niet alle, van deze patiënten hebben een nierfunctiestoornis en/of eerdere overgevoeligheid voor allopurinol gemeld In sommige gevallen zijn ernstige overgevoeligheidsreacties, waaronder geneesmiddelreacties met eosinofilie en systemische symptomen (DRESS), in verband gebracht met koorts, hematologische, renale of lever.Patiënten moeten worden geïnformeerd over de tekenen en symptomen en nauwlettend worden gecontroleerd op symptomen van allergische/overgevoeligheidsreacties (zie rubriek 4.8).De behandeling met febuxostat moet onmiddellijk worden gestaakt als er ernstige allergische/overgevoeligheidsreacties optreden, waaronder Stevens-Johnson-syndroom, zoals preventief staken van de behandeling is geassocieerd met een betere prognose. Als de patiënt een allergische/overgevoeligheidsreactie heeft ontwikkeld, waaronder Stevens-Johnson-syndroom en acute anafylactische reactie/shock, mag febuxostat niet meer worden toegediend.
Acute aanvallen van jicht (flare-up)
Behandeling met febuxostat dient niet te worden gestart totdat de acute jichtaanval volledig is verdwenen Bij het begin van de behandeling kunnen jichtaanvallen optreden als gevolg van een verandering in de serumurinezuurspiegels, die optreedt na een mobilisatie van uraten uit weefselafzettingen. (zie rubrieken 4.8 en 5.1). Bij de start van de behandeling met febuxostat wordt profylaxe tegen opflakkeringen van jicht gedurende ten minste 6 maanden aanbevolen met een NSAID of colchicine (zie rubriek 4.2).
Als tijdens de behandeling met febuxostat een opflakkering van jicht optreedt, mag deze niet worden gestaakt. De exacerbatie moet gelijktijdig worden behandeld, afhankelijk van de behoeften van de individuele patiënt. Voortgezette behandeling met febuxostat vermindert de frequentie en intensiteit van jichtaanvallen.
Afzetting van xanthine
Bij patiënten bij wie de snelheid waarmee uraten worden gevormd is verhoogd (bijvoorbeeld bij maligne neoplasmata en tijdens hun behandeling of bij het syndroom van Lesch-Nyhan), kan de absolute concentratie van xanthine in de urine, in zeldzame gevallen, in mate toenemen om zijn afzetting in de urinewegen. Aangezien er geen ervaring is met febuxostat, wordt het gebruik ervan bij deze categorie patiënten niet aanbevolen.
Mercaptopurine / azathioprine
Het gebruik van febuxostat wordt niet aanbevolen bij patiënten die gelijktijdig met mercaptopurine/azathioprine worden behandeld.Als gelijktijdig gebruik niet kan worden vermeden, dienen patiënten zorgvuldig te worden gecontroleerd. Een verlaging van de dosis mercaptopurine of azathioprine wordt aanbevolen om mogelijke hematologische effecten te voorkomen (zie rubriek 4.5).
Onderwerpen die een orgaantransplantatie hebben ondergaan
Aangezien er geen ervaring is met het gebruik van ADENURIC bij ontvangers van een orgaantransplantatie, wordt het gebruik van febuxostat bij deze patiënten niet aanbevolen (zie rubriek 5.1).
theofylline
Gelijktijdige toediening van febuxostat 80 mg en theofylline 400 mg als een enkele dosis bij gezonde proefpersonen toonde de afwezigheid van een farmacokinetische interactie aan (zie rubriek 4.5).Febuxostat 80 mg kan worden gebruikt bij patiënten die gelijktijdig met theofylline worden behandeld zonder het risico op verhoogde plasmaspiegels van theofylline Er zijn geen gegevens beschikbaar voor febuxostat 120 mg.
Leverziekten
Tijdens de gecombineerde klinische fase 3-onderzoeken werden milde afwijkingen in de leverfunctietest (5,0%) waargenomen bij patiënten die werden behandeld met febuxostat. Leverfunctietesten worden aanbevolen vóór aanvang van de behandeling met febuxostat en daarna met periodieke tussenpozen, zoals beoordeeld door de arts (zie rubriek 5.1).
Ziekten van de schildklier
In langdurige open-label extensieonderzoeken werden verhoogde TSH-waarden (> 5,5 mcIU/ml) waargenomen bij langdurig met febuxostat behandelde patiënten (5,5%). Voorzichtigheid is geboden met febuxostat bij patiënten met een gestoorde schildklierfunctie (zie rubriek 5.1).
Lactose
Febuxostat-tabletten bevatten lactose. Patiënten met zeldzame erfelijke vormen van galactose-intolerantie, Lapp's lactasedeficiëntie of glucose-galactose malabsorptiesyndroom dienen dit geneesmiddel niet te gebruiken.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Mercaptopurine / azathioprine
Op basis van het werkingsmechanisme van febuxostat op de remming van xanthine-oxidase (XO), wordt gelijktijdig gebruik van ADENURIC met mercaptopurine/azathioprine niet aanbevolen. Remming van XO door febuxostat kan verhoogde plasmaconcentraties van deze geneesmiddelen veroorzaken, wat kan leiden tot toxiciteit (zie rubriek 4.4). ). Er zijn geen interactiestudies uitgevoerd van febuxostat met door XO gemetaboliseerde geneesmiddelen.
Er zijn geen interactiestudies uitgevoerd tussen febuxostat en cytotoxische chemotherapie.Er zijn geen gegevens over de veiligheid van febuxostat bij gelijktijdig gebruik met cytotoxische therapie.
Rosiglitazon / CYP2C8-substraten
Van febuxostat is aangetoond dat het in vitro een zwakke remmer van CYP2C8 is. In een onderzoek bij gezonde proefpersonen had gelijktijdige toediening van febuxostat 120 mg eenmaal daags met een enkelvoudige orale dosis rosiglitazon van 4 mg geen effect op de farmacokinetiek van rosiglitazon en zijn metaboliet N-desmethylrosiglitazon, wat aangeeft dat febuxostat geen enzymremmer is van CYP2C8 in vivo. Daarom wordt bij gelijktijdige toediening van febuxostat en rosiglitazon of andere CYP2C8-substraten geen dosisaanpassing voor deze verbindingen verwacht.
theofylline
Er is een interactieonderzoek met febuxostat uitgevoerd bij gezonde proefpersonen om te beoordelen of remming van XO zou kunnen leiden tot een verhoging van de circulerende theofyllinespiegels, zoals gerapporteerd voor andere XO-remmers. De resultaten van de studie tonen aan dat gelijktijdige toediening van febuxostat, 80 mg eenmaal daags, en theofylline, 400 mg enkelvoudige dosis, geen effect heeft op de farmacokinetiek en veiligheid van theofylline. Daarom is er geen bijzondere voorzichtigheid vereist wanneer febuxostat 80 mg en theofylline gelijktijdig worden toegediend. Er zijn geen gegevens beschikbaar voor febuxostat 120 mg.
Naproxen en andere glucuronideringremmers
Het metabolisme van febuxostat is afhankelijk van uridineglucuronosyltransferase (UGT)-enzymen. Geneesmiddelen die glucuronidering remmen, zoals NSAID's en probenecide, kunnen in theorie de eliminatie van febuxostat beïnvloeden. Bij gezonde proefpersonen ging het gelijktijdige gebruik van febuxostat en naproxen 250 mg tweemaal daags gepaard met een verhoogde blootstelling aan febuxostat (Cmax 28%, AUC 41% en t1 / 2 26%). In klinische onderzoeken was het gebruik van naproxen of andere NSAID's / Cox-2-remmers niet gerelateerd aan enige klinisch significante toename van bijwerkingen. Febuxostat kan gelijktijdig met naproxen worden toegediend, zonder dat de dosis van febuxostat of naproxen hoeft te worden aangepast.
Inductoren van glucuronidering
Krachtige inductoren van UGT-enzymen kunnen leiden tot een verhoogd metabolisme en een verminderde werkzaamheid van febuxostat. Een controle van serumurinezuur wordt daarom aanbevolen 1-2 weken na aanvang van de behandeling met een krachtige glucuronidering-inductor. Omgekeerd kan stopzetting van de behandeling met een glucuronidering-inductor resulteren bij verhoogde plasmaspiegels van febuxostat.
Colchicine / indomethacine / hydrochloorthiazide / warfarine
Febuxostat kan gelijktijdig met colchicine of indomethacine worden toegediend zonder dat de dosis febuxostat of de andere gelijktijdig toegediende werkzame stof hoeft te worden aangepast.
Er is geen dosisaanpassing van febuxostat nodig bij gelijktijdige toediening met hydrochloorthiazide.
Bij gelijktijdige toediening met febuxostat is geen dosisaanpassing van warfarine nodig. Toediening van febuxostat (80 mg of 120 mg eenmaal daags) met warfarine had geen effect op de farmacokinetiek van warfarine bij gezonde patiënten. Bovendien worden de INR en geactiveerde factor VII niet beïnvloed door de toediening van febuxostat.
Desipramine / CYP2D6-substraten
Van febuxostat is aangetoond dat het een zwakke remmer is van CYP2D6 in vitro. In een onderzoek bij gezonde proefpersonen resulteerde 120 mg ADENURIC eenmaal daags in een gemiddelde toename van 22% van de AUC van desipramine, een CYP2D6-substraat, wat wijst op een mogelijk zwakke remmende werking van febuxostat op het CYP2D6-enzym. in vivo. In het geval van gelijktijdige toediening van febuxostat en andere CYP2D6-substraten is het daarom niet denkbaar dat de dosis voor een van deze verbindingen moet worden aangepast.
Antacida
Er is aangetoond dat de gelijktijdige inname van een antacidum dat magnesiumhydroxide en aluminiumhydroxide bevat de absorptie van febuxostat vertraagt (met ongeveer 1 uur) en een verlaging van de Cmax met 32% veroorzaakt, terwijl er geen significante verandering is waargenomen met betrekking tot de "AUC". . Het is daarom mogelijk om febuxostat in te nemen zonder rekening te houden met het gebruik van maagzuurremmers.
04.6 Zwangerschap en borstvoeding
Zwangerschap
Gegevens over een zeer beperkt aantal blootgestelde zwangerschappen wijzen niet op bijwerkingen van febuxostat op de zwangerschap of op de gezondheid van de foetus/pasgeborene. Dierstudies wijzen niet op directe of indirecte schadelijke effecten met betrekking tot zwangerschap, embryonale/foetale ontwikkeling of bevalling (zie rubriek 5.3). Het potentiële risico voor mensen is niet bekend. Febuxostat mag niet worden gebruikt tijdens de zwangerschap.
Voedertijd
Het is niet bekend of febuxostat wordt uitgescheiden in de moedermelk. Uit dieronderzoek is gebleken dat de uitscheiding van deze werkzame stof in de moedermelk gepaard gaat met een ontwikkelingsachterstand bij pasgeborenen tijdens de borstvoeding. Een risico voor de zuigeling die borstvoeding krijgt kan niet worden uitgesloten. Febuxostat mag niet worden gebruikt tijdens de borstvoeding. "Borstvoeding.
Vruchtbaarheid
In reproductiestudies bij dieren vertoonden doses tot 48 mg/kg/dag geen dosisafhankelijke bijwerkingen op de vruchtbaarheid (zie rubriek 5.3). Het effect van ADENURIC op de vruchtbaarheid bij de mens is niet bekend.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Slaperigheid, duizeligheid, paresthesie en wazig zien zijn gemeld bij het gebruik van febuxostat.Patiënten moeten grote voorzichtigheid betrachten voordat ze gaan autorijden, machines bedienen of gevaarlijke activiteiten uitvoeren totdat ze er redelijk zeker van zijn dat het gebruik van ADENURIC hun prestaties niet schaadt.
04.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest gemelde bijwerkingen in klinische onderzoeken (4072 proefpersonen behandeld met een dosis van ten minste 10 mg tot 300 mg) en postmarketingervaring zijn acute jichtaanvallen, leverfunctiestoornissen, diarree, misselijkheid, hoofdpijn, huiduitslag en oedeem. bijwerkingen waren meestal licht of matig van ernst Zeldzame ernstige overgevoeligheidsreacties op febuxostat, waarvan sommige geassocieerd waren met systemische symptomen, traden op tijdens postmarketingervaring.
Lijst van bijwerkingen in tabelvorm
Vaak voorkomende bijwerkingen (≥1 / 100 -
Tabel 1: Bijwerkingen gemeld in langdurige gecombineerde fase III-onderzoeken en postmarketingervaring
* Bijwerkingen verzameld tijdens postmarketingervaring
** Opkomende behandeling van niet-infectieuze diarree en abnormale leverfunctietesten in de gecombineerde fase 3-onderzoeken komen vaker voor bij patiënten die gelijktijdig met colchicine worden behandeld.
*** Zie rubriek 5.1 voor de incidentie van jichtaanvallen in de afzonderlijke fase 3 gerandomiseerde gecontroleerde onderzoeken.
Beschrijving van geselecteerde bijwerkingen
Zeldzame gevallen van ernstige overgevoeligheidsreacties op febuxostat, waaronder Stevens-Johnson-syndroom, toxische epidermale necrolyse en anafylactische/shockreacties, zijn opgetreden tijdens postmarketingervaring Stevens-Johnson-syndroom en toxische epidermale necrolyse worden gekenmerkt door erupties progressieve huid geassocieerd met blaren of mucosale laesies en oogirritatie.
Overgevoeligheidsreacties op febuxostat kunnen gepaard gaan met de volgende symptomen: huidreacties die worden gekenmerkt door geïnfiltreerde maculopapulaire uitslag, gegeneraliseerde of exfoliatieve uitslag, maar ook huidlaesies, gezichtsoedeem, koorts, hematologische veranderingen zoals trombocytopenie en eosinofilie, en betrokkenheid van één of meerdere organen ( lever en nieren, inclusief tubulo-interstitiële nefritis) (zie rubriek 4.4).
Acute aanvallen van jicht werden vaak gezien kort na het begin van de behandeling en gedurende de eerste paar maanden.Daarna neemt de frequentie van jichtaanvallen tijdsafhankelijk af. Profylaxe van acute jichtaanvallen wordt aanbevolen (zie rubrieken 4.2 en 4.4).
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue monitoring van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
In het geval van een overdosis moeten patiënten worden behandeld met symptomatische en ondersteunende zorg.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: preparaten tegen jicht, preparaten die de productie van urinezuur remmen.
ATC-code: M04AA03
Werkingsmechanisme
Urinezuur is het eindproduct van het purinemetabolisme en wordt bij mensen geproduceerd volgens de volgorde hypoxanthine → xanthine → urinezuur. Beide stappen van de bovenstaande reactie worden gekatalyseerd door xanthine-oxidase (XO). Febuxostat is een derivaat van 2-arylthiazol dat de therapeutisch effect van verlaging van serumurinezuur door selectieve remming van XO Febuxostat is een krachtige, niet-purine, selectieve remmer van XO (NP-SIXO) met een Ki-waarde (constante d "remming) in vitro minder dan 1 nanomolair. Van Febuxostat is aangetoond dat het XO met grote werkzaamheid kan remmen, zowel in de geoxideerde als in de gereduceerde vorm. Bij therapeutische concentraties remt febuxostat niet de andere enzymen die betrokken zijn bij het metabolisme van purines of pyrimidinen, namelijk guaninedeaminase, hypoxanthine-guaninefosforibosyltransferase, orotaatfosforibosyltransferase, orotidinemonofosfaatdecarboxylase of purinenucleosylase.
Klinische werkzaamheid en veiligheid
De werkzaamheid van ADENURIC werd aangetoond in drie fase 3-hoofdonderzoeken (de twee hoofdonderzoeken APEX en FACT, en het aanvullende CONFIRMS-onderzoek dat hieronder wordt beschreven) die werden uitgevoerd bij 4.101 patiënten met hyperurikemie en jicht. bleek een groter vermogen te hebben dan allopurinol om de urinezuurspiegels in serum te verlagen en te handhaven.
APEX-onderzoek: APEX (Allopurinol and Placebo-Controlled Efficiency Study of Febuxostat-Study of the werkzaamheid van febuxostat gecontroleerd tegen allopurinol en placebo) was een fase 3, gerandomiseerde, dubbelblinde, multicenter, 28 weken durende studie met een duur van 1.072 patiënten. die kregen: placebo (n = 134), ADENURIC 80 mg eenmaal daags (n = 267), ADENURIC 120 mg eenmaal daags (n = 269), ADENURIC 240 mg eenmaal daags (n = 134) o allopurinol (in een dosis van 300 mg eenmaal daags [n = 258] voor patiënten met baseline serumcreatinine ≤1,5 mg/dl of in een dosis van 100 mg eenmaal daags [n = 10] voor patiënten met baseline serumcreatinine>1,5 mg/dl en ≤2,0 mg/dl ) De dosis van 240 mg febuxostat (gelijk aan tweemaal de maximaal aanbevolen dosis) werd gebruikt voor de veiligheidsbeoordeling.
De APEX-studie toonde een statistisch significante superioriteit aan van de groepen die werden behandeld met zowel ADENURIC 80 mg eenmaal daags als ADENURIC 120 mg eenmaal daags bij het verlagen van serumurinezuur tot niveaus onder 6 mg/dl (357 μmol/l) in vergelijking met groepen die werden behandeld met conventionele doses allopurinol van 300 mg (n = 258) / 100 mg (n = 10) (zie tabel 2 en figuur 1). FACT-studie: FEIT (Febuxostat Allopurinol Controlled Trial) was een 52 weken durende, gerandomiseerde, dubbelblinde, multicenter, fase 3-studie. 760 patiënten werden gerandomiseerd die kregen: ADENURIC 80 mg eenmaal daags (n = 256), ADENURIC 120 mg eenmaal daags (n = 251) of allopurinol 300 mg eenmaal daags (n = 253).
De FACT-studie toonde een statistisch significante superioriteit aan van zowel de groepen ADENURIC 80 mg als ADENURIC 120 mg eenmaal daags bij het verlagen en handhaven van serumurinezuur onder 6 mg/dl (357 μmol/l) vergeleken met de groep die werd behandeld met de conventionele dosis allopurinol van 300 mg.
Tabel 2 vat de resultaten van het primaire werkzaamheidseindpunt samen:
tafel 2
Percentage patiënten met serumurinezuurspiegels
Laatste drie maandelijkse bezoeken
Het vermogen van ADENURIC om de serumurinezuurspiegels te verlagen was snel en aanhoudend De verlaging van de serumurinezuurspiegels tot waarden
CONFIRMS-studie: De CONFIRMS-studie was een 26 weken durende, gerandomiseerde, gecontroleerde fase 3-studie ter evaluatie van de veiligheid en werkzaamheid van febuxostat 40 mg en 80 mg, in vergelijking met allopurinol 300 mg of 200 mg, bij patiënten met jicht en hyperurikemie. patiënten werden gerandomiseerd: ADENURIC 40 mg eenmaal daags (n = 757), ADENURIC 80 mg eenmaal daags (n = 756) of allopurinol 300/200 mg eenmaal daags (n = 756). 65% van de patiënten had een lichte tot matige nierfunctiestoornis ( met een creatinineklaring van 30-89 ml/min) was profylaxe tegen jicht verplicht na de periode van 26 weken.
Het percentage patiënten met serumuraatspiegels van μmol/L bij het laatste bezoek was respectievelijk 45% voor 40 mg febuxostat, 67% voor 80 mg febuxostat en 42% voor allopurinol 300/200 mg.
Primair eindpunt in de subgroep van patiënten met nierfunctiestoornis
De APEX-studie evalueerde de werkzaamheid van het geneesmiddel bij 40 patiënten met nierinsufficiëntie (baseline serumcreatinine > 1,5 mg/dl en ≤ 2,0 mg/dl) Voor patiënten met nierinsufficiëntie die gerandomiseerd waren om allopurinol te krijgen, was de laatste dosis beperkt tot 100 mg een keer per dag. ADENURIC bereikte het primaire werkzaamheidseindpunt bij respectievelijk 44% (80 mg eenmaal daags), 45% (120 mg eenmaal daags) en 60% (240 mg eenmaal daags) van de patiënten vergeleken met 0% gevonden in de allopurinol 100 mg eenmaal daags en placebo groepen.
Er werden geen klinisch significante verschillen waargenomen in de snelheid van verlaging van de serumurinezuurconcentraties bij gezonde proefpersonen, ongeacht hun nierfunctiestatus (58% in de groep met normale nierfunctie en 55% in de groep met ernstige nierfunctiestoornis).
Een "analyse bij patiënten met jicht en nierinsufficiëntie werd prospectief gedefinieerd in de CONFIRMS-studie en toonde aan dat febuxostat significant effectiever was in het verlagen van de serumuraatspiegels dan
Primair eindpunt in de subgroep van patiënten met een serumurinezuurspiegel 10 mg/dL
Ongeveer 40% van de patiënten (APEX en FACT samen) had een baseline serumurinezuurwaarde van ≥ 10 mg/dL In deze subgroep bereikte ADENURIC het primaire werkzaamheidseindpunt (urinezuurspiegel
In de CONFIRMS-studie was het percentage patiënten dat voldeed aan het primaire werkzaamheidseindpunt (urinezuurspiegel
Klinische resultaten: Percentage patiënten dat behandeling nodig had voor een jichtaanval
APEX-onderzoek: Tijdens de profylaxeperiode van 8 weken had een groter deel (36%) van de patiënten die werden behandeld met febuxostat 120 mg behandeling nodig voor een jichtaanval dan met febuxostat 80 mg (28%), allopurinol 300 mg (23%) en placebo ( Aanvallen namen toe na de profylaxeperiode en namen geleidelijk af in de loop van de tijd Tussen 46% en 55% van de proefpersonen kreeg behandeling voor acute jichtaanvallen van week 8 tot week 28. Jichtaanvallen tijdens de laatste 4 weken van het onderzoek (weken 24 -28) werden waargenomen bij 15% (febuxostat 80, 120 mg), 14% (allopurinol 300 mg) en 20% (placebo) van de patiënten FEIT: Tijdens de profylaxeperiode van 8 weken werd een groter deel (36%) van de met febuxostat 120 mg behandelde patiënten had behandeling nodig voor jichtopflakkering dan beide behandelingen met febuxostat 80 mg (22%) en allopurinol 300 mg (21%).
Na de profylaxeperiode van 8 weken nam de incidentie van acute aanvallen geleidelijk toe en af in de loop van de tijd (64% en 70% van de proefpersonen kregen behandeling voor acute jichtaanvallen van week 8 tot week 52). studie (weken 49-52) werden waargenomen bij 6-8% (febuxostat 80 mg, 120 mg) en 11% (allopurinol 300 mg) van de patiënten.
Het percentage patiënten dat behandeling nodig had voor een jichtaanval (APEX- en FACT-onderzoeken) was numeriek lager in de groepen die een gemiddelde post-baseline serumuraatspiegel bereikten.
Tijdens de CONFIRMS-studie waren de percentages patiënten die behandeling nodig hadden voor jichtaanvallen (dag 1 tot en met maand 6) respectievelijk 31% en 25% voor de febuxostat 80 mg- en allopurinolgroepen. Er was geen verschil in het percentage patiënten dat behandeling nodig had voor jichtaanvallen tussen de febuxostat 80 mg- en 40 mg-groepen.
Langdurige open-label extensieonderzoeken
EXCEL-onderzoek (C02-021): EXCEL was een drie jaar durende, open-label, multicenter, gerandomiseerde, allopurinol-gecontroleerde, veiligheidsverlengingsstudie van drie jaar voor patiënten die de fase 3-hoofdstudies (APEX of FACT) hadden voltooid. In totaal namen 1.086 patiënten deel: ADENURIC 80 mg eenmaal daags (n = 649), ADENURIC 120 mg eenmaal daags (n = 292) en allopurinol 300/100 mg eenmaal daags (n = 145). Ongeveer 69% van de patiënten had geen behandelingsveranderingen nodig om een stabiele uiteindelijke respons te bereiken. Patiënten met drie opeenvolgende urineconcentraties > 6,0 mg/dL werden gestaakt.
Serumuraatspiegels bleven in de loop van de tijd gehandhaafd (bijv. 91% en 93% van de patiënten die aanvankelijk werden behandeld met respectievelijk febuxostat 80 mg en 120 mg hadden urinemie
Gegevens over drie jaar toonden een vermindering van de incidentie van jichtaanvallen aan bij minder dan 4% van de patiënten die behandeling nodig hadden voor een exacerbatie (d.w.z. meer dan 96% van de patiënten die geen behandeling nodig hadden voor een exacerbatie) na 16-24 maanden en 30- 36 maanden 46% en 38% van de patiënten die de laatste stabiele behandeling kregen met respectievelijk febuxostat 80 mg of 120 mg eenmaal daags, verdwenen volledig van palpabele primaire tophus vanaf baseline tot het laatste bezoek.
FOCUS-studie (TMX-01-005): FOCUS was een 5-jarige fase 2, open-label, multicenter, veiligheidsuitbreidingsstudie voor patiënten die 4 weken febuxostat-dosering hadden voltooid in de dubbelblinde TMX-studie -00-004. 116 patiënten werden geïncludeerd en kregen aanvankelijk 80 mg febuxostat eenmaal daags. 62% van de patiënten had geen dosisaanpassing nodig om urinezuur te behouden
Het aandeel patiënten met serumuraatspiegels
Tijdens klinische fase 3-onderzoeken werden lichte veranderingen in de testwaarden van de leverfunctie (5,0%) waargenomen bij patiënten die werden behandeld met febuxostat. Deze waarden waren vergelijkbaar met die gerapporteerd voor allopurinol (4,2%) (zie rubriek 4.4). Verhoogde TSH-waarden (> 5,5 mcIU / ml) werden waargenomen in langdurige open-label extensieonderzoeken bij patiënten. behandeld met febuxostat (5,5%) en bij patiënten behandeld met allopurinol (5,8%) (zie rubriek 4.4).
05.2 Farmacokinetische eigenschappen
Bij gezonde proefpersonen stegen de Cmax (maximale plasmaconcentratie) en AUC (gebied onder de curve) van febuxostat dosisproportioneel na toediening van een enkelvoudige en herhaalde dosis van 10 mg tot 120 mg. Voor febuxostat-doses variërend van 120 mg en 300 mg was een grotere dan dosisproportionele toename van de AUC wordt waargenomen. Er is geen merkbare accumulatie zichtbaar na toediening van doses van 10 mg tot 240 mg om de 24 uur. Febuxostat heeft een schijnbare terminale eliminatiehalfwaardetijd (t1/2) van ongeveer 5-8 uur.
Farmacokinetische/farmacodynamische populatieanalyses werden uitgevoerd bij 211 patiënten met hyperurikemie en jicht die werden behandeld met ADENURIC in een dosis van 40-240 mg eenmaal daags.
Over het algemeen zijn de farmacokinetische parameters van febuxostat, geschat door deze analyses, consistent met die waargenomen bij gezonde proefpersonen, wat aangeeft dat gezonde proefpersonen representatief zijn voor farmacokinetische/farmacodynamische evaluatie bij de populatie van jichtpatiënten.
Absorptie
Febuxostat wordt snel geabsorbeerd (Tmax van 1,0-1,5 uur) en bijna volledig (minstens 84%). Na toediening van een enkelvoudige orale dosis of meerdere orale doses van 80 en 120 mg eenmaal daags, is de Cmax respectievelijk ongeveer 2,8-3,2 mcg/ml en 5,0-5,3 mcg/ml. De absolute biologische beschikbaarheid van de febuxostat-tabletformulering is niet onderzocht.
Na toediening van meerdere orale doses van 80 mg eenmaal daags of een enkelvoudige dosis van 120 mg samen met een vetrijke maaltijd, werd een verlaging van de Cmax van respectievelijk 49% en 38% en een verlaging van de Cmax waargenomen. respectievelijk % en 16%.
Er werd echter geen klinisch significante verandering waargenomen in de procentuele verlaging van de serumurinezuurconcentratie bij evaluatie (herhaalde doses van 80 mg).Daarom kan ADENURIC zowel bij als buiten de maaltijden worden ingenomen.
Verdeling
Het schijnbare distributievolume bij stabiele toestand (Vss / F) van febuxostat varieert van 29 tot 75 l na orale doses van 10-300 mg. De plasma-eiwitbinding van febuxostat is ongeveer 99,2% (voornamelijk albumine) en blijft constant boven de concentraties die worden bereikt met doses van 80 tot 120 mg De plasma-eiwitbinding van metabolieten ligt tussen ongeveer 82% en 91%.
Biotransformatie
Febuxostat wordt uitgebreid gemetaboliseerd door conjugatie via het uridinedifosfaatglucuronosyltransferase (UDPGT)-enzymsysteem en door oxidatie via het cytochroom P450 (CYP)-systeem. Er zijn vier farmacologisch actieve hydroxylmetabolieten geïdentificeerd, waarvan er drie kunnen worden waargenomen in humaan plasma. Studies iin vitro met humane levermicrosomen toonde aan dat deze oxidatieve metabolieten voornamelijk bestonden uit CYP1A1, CYP1A2, CYP2C8 of CYP2C9 en febuxostat-glucuronide voornamelijk uit UGT 1A1, 1A8 en 1A9.
Eliminatie
Febuxostat wordt geëlimineerd via zowel de lever als de nieren. Na orale toediening van een dosis van 80 mg 14C-gelabeld febuxostat werd ongeveer 49% van de dosis in de urine teruggevonden als onveranderd febuxostat (3%), werkzame stof acylglucoronide (30%), zijn oxidatieve metabolieten samen met hun conjugaten (13 %), en andere onbekende metabolieten (3%). Naast de eliminatie via de urine werd ongeveer 45% van de dosis teruggevonden in de feces in de vorm van onveranderd febuxostat (12%), acylglucuronide van het werkzame bestanddeel (1%), zijn bekende oxidatieve metabolieten samen met hun conjugaten (25% ), en andere onbekende metabolieten (7%).
Nierfunctiestoornis
Na toediening van herhaalde doses van 80 mg ADENURIC aan patiënten met een lichte, matige of ernstige nierfunctiestoornis, verschilde de Cmax van febuxostat niet van die van proefpersonen met een normale nierfunctie. De totale gemiddelde AUC van febuxostat nam ongeveer 1,8-voudig toe van 7,5 mcg.u/ml in de groep met een normale nierfunctie tot 13,2 mcg.u/ml in de groep met ernstige nierinsufficiëntie. vouwen, respectievelijk. Er is echter geen dosisaanpassing nodig bij personen met een lichte of matige nierfunctiestoornis.
leverfunctiestoornis
Na herhaalde toediening van 80 mg ADENURIC aan patiënten met een lichte (Child-Pugh-klasse A) of matige (Child-Pugh-klasse B) leverfunctiestoornis, veranderden de Cmax en AUC van febuxostat en zijn metabolieten niet significant in vergelijking met proefpersonen met een normale leverfunctie Er zijn geen onderzoeken uitgevoerd bij patiënten met een ernstige leverfunctiestoornis (Child-Pugh-klasse C).
Leeftijd
Er werden geen significante veranderingen in de AUC van febuxostat of zijn metabolieten waargenomen na herhaalde toediening van orale doses ADENURIC bij oudere proefpersonen in vergelijking met jongere gezonde proefpersonen.
Type
Na herhaalde orale doses ADENURIC waren de Cmax en AUC respectievelijk 24% en 12% hoger bij vrouwen dan bij mannen. De voor gewicht gecorrigeerde Cmax en AUC waren echter gelijk voor beide geslachten Er is geen dosisaanpassing vereist op basis van geslacht.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Effecten die optraden in niet-klinische onderzoeken werden over het algemeen waargenomen bij blootstelling aan geneesmiddelen die de maximale blootstelling bij de mens overschreed.
Carcinogenese, mutagenese, verminderde vruchtbaarheid
Bij mannelijke ratten werd een statistisch significante toename van blaastumoren (transitiecel papilloma en carcinoom) alleen waargenomen in de aanwezigheid van xanthinestenen in de groep die werd behandeld met de hoogste dosis, overeenkomend met doses die ongeveer 11 keer hoger waren dan de blootstelling. in een van de andere tumortypes werd waargenomen, noch bij mannelijke muizen of ratten, noch bij vrouwelijke muizen of ratten. Deze waarnemingen worden beschouwd als een gevolg van soortspecifiek metabolisme van purines en urinesamenstelling en zijn niet relevant voor de klinisch gebruik van het geneesmiddel.
Een standaard reeks genotoxiciteitstesten bracht geen relevante genotoxische effecten van febuxostat aan het licht.
Febuxostat bij orale doses tot 48 mg/kg/dag had geen effect op de vruchtbaarheid en reproductieprestaties bij zowel mannelijke als vrouwelijke ratten.
Er waren geen aanwijzingen voor verminderde vruchtbaarheid, teratogene effecten of schadelijke gevolgen voor de foetus door de werking van febuxostat. Bij ratten werd bij hoge doses en met een blootstelling van ongeveer 4,3 maal die van mensen een toxiciteit voor de moeder waargenomen, vergezeld van een verlaging van de speenindex en een vertraging in de ontwikkeling van het nageslacht Teratologische studies uitgevoerd bij drachtige ratten en konijnen met een blootstelling van respectievelijk ongeveer 4,3 en 13 keer zo hoog als die voor mensen, brachten geen teratogene effecten van febuxostat aan het licht.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Kern van de tablet
Lactosemonohydraat
Microkristallijne cellulose
Magnesium stearaat
Hydroxypropylcellulose
Croscarmellosenatrium
Silica, colloïdaal gehydrateerd
Tabletcoating
Opadry II, geel, 85F42129 met daarin:
Polyvinylalcohol
Titaandioxide (E171)
Macrogol-type 3350
Talk
Geel ijzeroxide (E172)
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Transparante blisterverpakking (Aclar / PVC / Aluminium) met 14 tabletten.
ADENURIC 80 mg is verkrijgbaar in verpakkingen van 14, 28, 42, 56, 84 en 98 filmomhulde tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Menarini International Operations Luxembourg S.A.
1, Avenue de la Gare, L-1611 Luxemburg
Luxemburg
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU / 1/08/447/001
EU / 1/08/447/002
EU / 1/08/447/005
EU / 1/08/447/006
EU / 1/08/447/007
EU / 1/08/447/008
039538018
039538020
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste vergunning: 21 april 2008
Datum van de meest recente verlenging: 20 december 2012
10.0 DATUM VAN HERZIENING VAN DE TEKST
april 2015




















.jpg)