Actieve ingrediënten: Finasteride
Finasteride Actavis 5 mg filmomhulde tabletten
Waarom wordt Finasteride gebruikt - Generiek geneesmiddel? Waar is het voor?
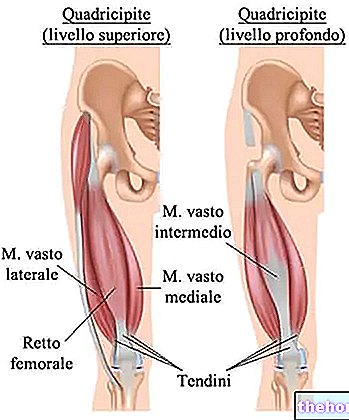
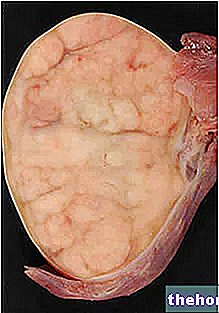
Finasteride Actavis bevat de werkzame stof finasteride die behoort tot een groep geneesmiddelen die 5α-reductaseremmers worden genoemd. Ze werken door de grootte van de prostaatklier bij mannen te verkleinen
Finasteride Actavis wordt gebruikt voor de behandeling en controle van goedaardige (niet-kankerachtige) vergroting van de prostaat.
Contra-indicaties Wanneer Finasteride - Generic Drug niet mag worden gebruikt
Gebruik Finasteride Actavis niet
- als u allergisch bent voor finasteride of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6)
- als u een vrouw of een kind bent (zie ook "Zwangerschap, borstvoeding en vruchtbaarheid" in deze rubriek)
Voorzorgen bij gebruik Wat u moet weten voordat u Finasteride gebruikt - Generiek geneesmiddel
- als u een verminderde leverfunctie heeft;
- als u moeite heeft met het volledig legen van uw blaas of een ernstige vermindering van de urinestroom, moet uw arts u zorgvuldig onderzoeken voordat u met Finasteride Actavis begint om andere urinewegobstructies uit te sluiten;
- Als u veranderingen in het borstweefsel bemerkt, zoals knobbels, pijn, vergroting van het borstweefsel of afscheiding van de tepels, kunnen dit tekenen zijn van een ernstige aandoening zoals borstkanker. Vertel het uw arts onmiddellijk als u een van deze veranderingen opmerkt.
Als uw seksuele partner zwanger is of vermoedt zwanger te zijn, moet u voorkomen dat u haar blootstelt aan uw sperma dat een kleine hoeveelheid van het geneesmiddel kan bevatten (zie ook "Zwangerschap, borstvoeding en vruchtbaarheid" in deze rubriek).
Als u een bloedtest met de naam "PSA" moet ondergaan, moet u dit aan uw arts of verpleegkundige vertellen voordat u de test uitvoert, aangezien finasteride de testresultaten kan veranderen.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Finasteride - Generic Drug veranderen
Finasteride Actavis-tabletten kunnen meestal samen met andere geneesmiddelen worden ingenomen. Vraag uw arts om advies voordat u tegelijkertijd andere geneesmiddelen inneemt.
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Waarop moet u letten met eten en drinken?
Finasteride Actavis kan met of zonder voedsel worden ingenomen.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Finasteride Actavis is alleen bedoeld voor mannen. Als uw seksuele partner zwanger is of vermoedt dat ze zwanger is, moet u voorkomen dat u haar blootstelt aan zijn sperma dat een kleine hoeveelheid van het geneesmiddel kan bevatten.
Vrouwen die zwanger zijn of van plan zijn zwanger te worden, mogen niet in contact komen met gebroken of gebroken tabletten Finasteride Actavis.
Als finasteride door de huid wordt opgenomen of oraal wordt ingenomen door een zwangere vrouw van een mannelijke foetus, kan de baby geboren worden met een misvorming van de geslachtsorganen. De tabletten zijn filmomhuld om contact met finasteride te voorkomen, zolang de tabletten niet gebroken of fijngemaakt worden.
Rijvaardigheid en het gebruik van machines
Er zijn geen aanwijzingen dat Finasteride Actavis de rijvaardigheid of het vermogen om machines te bedienen verandert.
Finasteride Actavis bevat lactose.
Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt.
Dosis, wijze en tijdstip van toediening Hoe wordt Finasteride gebruikt - Generiek geneesmiddel: Dosering
Gebruik dit geneesmiddel precies zoals uw arts of apotheker u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
De aanbevolen dosering is 1 tablet per dag.
De tablet moet heel worden doorgeslikt en mag niet worden gebroken of fijngemaakt. Het kan met of zonder voedsel worden ingenomen.
Overdosering Wat moet u doen als u een overdosis Finasteride heeft ingenomen?
Wat u moet doen als u meer van Finasteride Actavis heeft ingenomen dan u zou mogen
Neem onmiddellijk contact op met een arts, de dichtstbijzijnde spoedeisende hulp of het antigifcentrum voor advies.
Bent u vergeten Finasteride Actavis in te nemen?
Neem geen dubbele dosis om een vergeten tablet in te halen. Neem de volgende zoals gepland voor uw behandeling.
Als u stopt met het innemen van Finasteride Actavis
Hoewel vaak na korte tijd verbetering wordt waargenomen, kan het nodig zijn de behandeling gedurende ten minste 6 maanden voort te zetten. Verander de dosis niet en stop de behandeling niet zonder eerst uw arts te raadplegen.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Finasteride - Generic Drug?
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Als u een van de volgende symptomen (angio-oedeem) krijgt, stop dan onmiddellijk met het innemen van Finasteride Actavis en neem contact op met uw arts: zwelling van het gezicht, de tong of de keel, moeite met slikken, netelroos en ademhalingsmoeilijkheden.
Vaak (komt voor bij 1 tot 10 op de 100 patiënten): onvermogen om een erectie te krijgen, verminderde zin in seks, verminderd ejaculatievolume
Soms (treedt op bij 1 tot 10 op de 1000 patiënten): gevoelige borsten, huiduitslag, borstvergroting, moeilijk klaarkomen
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald): Depressie, pijn in de testikels, geen erectie kunnen krijgen die aanhoudt na het stoppen van de behandeling met Finasteride Actavis, verminderd seksueel verlangen dat aanhoudt na het stoppen van de behandeling, mannelijke onvruchtbaarheid en/of slecht sperma kwaliteit, jeuk, netelroos, onregelmatige, sterke of snelle hartslag, verhoogde leverenzymspiegels.
Meld eventuele veranderingen in het borstweefsel, zoals knobbels, pijn, vergroting van het borstweefsel of tepelafscheiding, onmiddellijk aan uw arts. Dit kunnen tekenen zijn van een ernstige aandoening zoals borstkanker.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de blisterverpakking en de doos na "EXP": De vervaldatum verwijst naar de laatste dag van de maand.
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
Gooi geneesmiddelen niet weg via het afvalwater of met het huisvuil.Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt.Dit helpt het milieu te beschermen.
Welke stoffen zitten er in Finasteride Actavis?
- De werkzame stof (het ingrediënt waardoor het geneesmiddel werkt) is finasteride.Eén filmomhulde tablet bevat 5 mg finasteride.
- De andere stoffen in de tabletkern zijn: lactosemonohydraat, microkristallijne cellulose, gepregelatineerd zetmeel (maïs), laurine-macrogolglyceriden, natriumzetmeelglycolaat, magnesiumstearaat. De tabletomhulling bevat hypromellose, macrogol, titaniumdioxide (E171), indigokarmijn aluminiumlak (E132).
Hoe ziet Finasteride Actavis er uit en wat is de inhoud van de verpakking
Finasteride Actavis is een blauwe, ronde, biconvexe tablet met de aanduiding "F5". De diameter is 7mm.
De blisterverpakking bevat 7, 10, 14, 15, 20, 28, 30, 49, 50, 60, 98, 100 of 300 tabletten.
De plastic fles bevat 10, 30, 50, 100 of 300 tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
FINASTERIDE ACTAVIS 5 MG TABLETTEN OMHOOG MET FILM
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke filmomhulde tablet bevat 5 mg finasteride.
Hulpstof: Elke filmomhulde tablet bevat 90,96 mg lactosemonohydraat.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
03.0 FARMACEUTISCHE VORM
Filmomhulde tabletten.
Blauwe, ronde en biconvexe tablet met de aanduiding "F5". De diameter is 7mm.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Finasteride Actavis is geïndiceerd voor de behandeling en beheersing van goedaardige prostaathyperplasie (BPH) bij patiënten met een vergrote prostaat voor:
- regressie van de vergrote prostaat induceren, de urinestroom verbeteren en symptomen geassocieerd met BPH . verbeteren
- het verminderen van de incidentie van acute urineretentie en de noodzaak van chirurgie, waaronder transurethrale resectie van de prostaat (TURP) en prostatectomie.
Finasteride Actavis 5 mg tabletten mogen alleen worden toegediend aan patiënten met een vergrote prostaat (prostaatvolume groter dan ongeveer 40 ml).
04.2 Dosering en wijze van toediening
Alleen voor oraal gebruik.
De aanbevolen dosering is één tablet van 5 mg per dag, met of zonder voedsel. De tablet moet in zijn geheel worden doorgeslikt en mag niet worden gedeeld of fijngemaakt (zie rubriek 6.6). Zelfs als er in korte tijd verbetering zichtbaar is, kan een behandeling van ten minste 6 maanden nodig zijn om objectief vast te stellen of de respons op de behandeling bevredigend is geweest.
Dosering bij leverinsufficiëntie
Er zijn geen gegevens beschikbaar over patiënten met een leverfunctiestoornis (zie rubriek 4.4).
Dosering bij nierinsufficiëntie
Er zijn geen dosisaanpassingen nodig bij patiënten met nierinsufficiëntie in verschillende mate (met creatinineklaring verminderd tot 9 ml/min), aangezien in farmacokinetische studies nierinsufficiëntie geen effect op de eliminatie van finasteride liet zien. Finasteride is niet onderzocht bij hemodialysepatiënten.
Dosering bij ouderen
Hoewel farmacokinetische onderzoeken hebben aangetoond dat de eliminatiesnelheid van finasteride enigszins is afgenomen bij patiënten ouder dan 70 jaar, zijn dosisaanpassingen niet nodig.
04.3 Contra-indicaties
Finasteride Actavis is niet geïndiceerd voor gebruik bij vrouwen of kinderen.
Finasteride is gecontra-indiceerd in de volgende gevallen:
- Overgevoeligheid voor het werkzame bestanddeel of voor één van de hulpstoffen.
- Zwangerschap: Gebruik bij vrouwen die zwanger zijn of mogelijk zwanger zijn (zie "Zwangerschap en borstvoeding; Blootstelling aan finasteride - risico voor een mannelijke foetus" in rubriek 4.6).
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Algemeen:
• Om obstructieve complicaties te voorkomen, is het belangrijk dat patiënten met een groot resterend urinevolume en/of een ernstig verminderde urinestroom zorgvuldig worden gecontroleerd. De mogelijkheid van een operatie moet als een optie worden beschouwd.
• Voor patiënten die met finasteride worden behandeld, dient overleg met een uroloog te worden overwogen.
• Finasteride Actavis bevat lactosemonohydraat. Patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, Lapp-lactasedeficiëntie of glucose-galactosemalabsorptie dienen dit geneesmiddel niet te gebruiken.
Effecten op prostaatspecifiek antigeen (PSA) en diagnose van prostaatkanker
Er is nog geen klinisch voordeel aangetoond bij patiënten met prostaatkanker die werden behandeld met finasteride 5 mg. Patiënten met verhoogde BPH en verhoogd prostaatspecifiek antigeen (PSA) werden gecontroleerd in gecontroleerde klinische onderzoeken met periodieke PSA-dosering en prostaatbiopten. In deze BPH-onderzoeken veranderde finasteride 5 mg het detectiepercentage van prostaatkanker niet en de totale incidentie van prostaatkanker was niet significant verschillend bij patiënten die werden behandeld met finasteride 5 mg of placebo.
Digitaal rectaal onderzoek en, indien nodig, bepaling van prostaatspecifiek antigeen (PSA) in serum moet bij patiënten worden uitgevoerd voordat de behandeling met finasteride 5 mg wordt gestart en periodiek tijdens de behandeling om prostaatkanker uit te sluiten. In het algemeen geldt dat wanneer PSA-waarden worden bepaald, een baseline PSA-waarde > 10 ng/ml (Hybritech) "nadere evaluatie en het overwegen van een biopsie omvat; voor PSA-waarden tussen 4 en 10 ng/ml is het raadzaam een "nadere evaluatie uit te voeren. Er is een aanzienlijke overlap in PSA-waarden tussen mannen met en zonder prostaatkanker. Bijgevolg sluiten PSA-waarden binnen het normale referentiebereik bij mannen met goedaardige prostaathyperplasie (BPH) prostaatkanker niet uit, ongeacht de behandeling met finasteride 5 mg. Een baseline PSA-waarde
Finasteride 5 mg veroorzaakt een verlaging van de serum-PSA-concentraties met ongeveer 50% bij patiënten met BPH, zelfs in aanwezigheid van prostaatkanker. Deze verlaging van de serum-PSA-spiegels bij BPH-patiënten die met finasteride 5 mg worden behandeld, moet worden overwogen bij de evaluatie van PSA-gegevens en sluit gelijktijdige prostaatkanker niet uit. Deze verlaging is voorspelbaar over het gehele bereik van PSA-waarden, hoewel deze bij individuele patiënten kan variëren.
Een "analyse van PSA-gegevens van een dubbelblind, placebogecontroleerd langetermijnonderzoek naar veiligheid en werkzaamheid (PLESS) bij 3000 patiënten gedurende 4 jaar met finasteride, bevestigde dat bij typische patiënten die gedurende zes maanden of langer met finasteride 5 mg werden behandeld, PSA waarden moeten worden verdubbeld om te vergelijken met normale waarden bij onbehandelde mannen. Deze aanpassing zorgt voor de gevoeligheid en specificiteit van de PSA-test en behoudt het vermogen om prostaatkanker op te sporen.
Elke aanhoudende stijging van de PSA-spiegels bij patiënten die met finasteride 5 mg worden behandeld, moet zorgvuldig worden overwogen, inclusief de mogelijkheid dat de patiënt de behandeling met 5 mg finasteride niet naleeft.
Het percentage vrij PSA (verhouding vrij PSA tot totaal) wordt niet significant verlaagd door finasteride 5 mg en blijft constant, zelfs onder invloed van finasteride 5 mg. Wanneer het percentage vrij PSA wordt gebruikt als hulpmiddel bij het opsporen van kanker bij prostaat, er is geen aanpassing aan de waarde nodig.
Geneesmiddel-/laboratoriumtestinteracties
Effecten op PSA-niveaus
Serum PSA-concentratie correleert met de leeftijd van de patiënt en het prostaatvolume, en het prostaatvolume correleert met de leeftijd van de patiënt. Bij het evalueren van PSA-laboratoriumwaarden moet er rekening mee worden gehouden dat de PSA-spiegels over het algemeen afnemen bij patiënten die worden behandeld met 5 mg finasteride. Bij de meeste patiënten wordt in de eerste maanden van de behandeling een snelle afname van PSA waargenomen; na deze periode stabiliseren de PSA-niveaus zich op een nieuwe basiswaarde. Uitgangswaarden na de behandeling zijn ongeveer de helft van de waarden voor de behandeling. Daarom moeten in het typische geval van patiënten die gedurende zes maanden of langer met 5 mg finasteride worden behandeld, de PSA-waarden worden verdubbeld in vergelijking met de normale waarden van onbehandelde mannen. Voor een "klinische interpretatie, zie" Effecten op "prostaatspecifiek antigeen (PSA) en prostaatkankerdiagnose in deze rubriek". Er werden geen andere verschillen waargenomen bij patiënten die werden behandeld met placebo of finasteride in standaard laboratoriumtests.
Borstkanker bij mensen
Borstkanker is gemeld bij mannen die werden behandeld met finasteride 5 mg tijdens klinische onderzoeken en de postmarketingperiode. Artsen dienen patiënten te informeren over de noodzaak om veranderingen in het borstweefsel, zoals knobbels, pijn, gynaecomastie of afscheiding uit de borst, onmiddellijk te melden.
Pediatrisch gebruik
Finasteride is niet geïndiceerd voor gebruik bij kinderen.
De veiligheid en werkzaamheid bij kinderen zijn niet vastgesteld.
Leverinsufficiëntie
Het effect van leverinsufficiëntie op de farmacokinetiek van finasteride is niet onderzocht. Voorzichtigheid is geboden bij patiënten met een verminderde leverfunctie, aangezien finasteride uitgebreid wordt gemetaboliseerd in de lever en de plasmaspiegels van finasteride bij dergelijke patiënten kunnen toenemen (zie rubriek 4.2).
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Er werden geen significante interacties met andere geneesmiddelen gevonden. Finasteride wordt voornamelijk gemetaboliseerd via het cytochroom P450 3A4-systeem, maar lijkt er geen significante effecten op te hebben. Hoewel het risico dat finasteride de farmacokinetiek van andere geneesmiddelen beïnvloedt laag wordt geschat, is het waarschijnlijk dat remmers en inductoren van cytochroom P450 3A4 de plasmaconcentratie van finasteride beïnvloeden. Op basis van de vastgestelde veiligheidsmarges is het echter onwaarschijnlijk dat een verhoging als gevolg van gelijktijdig gebruik van deze remmers klinisch significant is.
De volgende geneesmiddelen zijn bij mensen onderzocht en er zijn geen klinisch significante interacties vastgesteld: propranol, digoxine, glibenclamide, warfarine, theofylline en fenazon.
04.6 Zwangerschap en borstvoeding
Zwangerschap
Het gebruik van finasteride is gecontra-indiceerd bij vrouwen die zwanger zijn of mogelijk zwanger zijn (zie rubriek 4.3).
Vanwege het vermogen van type II 5α-reductaseremmers om de omzetting van testosteron in dihydrotestosteron te remmen, kunnen deze geneesmiddelen, waaronder finasteride, afwijkingen veroorzaken aan de uitwendige geslachtsorganen van een mannelijke foetus wanneer ze worden toegediend aan een zwangere vrouw (zie rubrieken 5.3 en 6.6).
Blootstelling aan finasteride - risico voor de mannelijke foetus
Zwangere vrouwen en vrouwen die zwanger kunnen worden, mogen geen gebroken of fijngemaakte finasteridetabletten hanteren, aangezien finasteride door de huid kan worden opgenomen, wat een potentieel risico voor een mannelijke foetus met zich meebrengt (zie "Zwangerschap" in deze rubriek).
Finasteride-tabletten zijn omhuld en dit voorkomt contact met de werkzame stof bij normaal gebruik, zolang de tabletten niet worden gebroken of geplet.
Er zijn kleine hoeveelheden finasteride gevonden in het sperma van proefpersonen die finasteride 5 mg/dag kregen.Het is niet bekend of een mannelijke foetus in gevaar kan komen als de moeder wordt blootgesteld aan het sperma van een patiënt die met finasteride wordt behandeld. Wanneer de seksuele partner van de patiënt zwanger is of ervan verdacht wordt zwanger te zijn, wordt de patiënt aangeraden de blootstelling van de partner aan zijn sperma tot een minimum te beperken.
Voedertijd
Het gebruik van Finasteride Actavis 5 mg tabletten is niet geïndiceerd bij vrouwen Het is niet bekend of finasteride wordt uitgescheiden in de moedermelk.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er zijn geen gegevens die erop wijzen dat finasteride de rijvaardigheid of het vermogen om machines te bedienen beïnvloedt.
04.8 Bijwerkingen
De meest voorkomende bijwerkingen zijn impotentie en verminderd libido Deze bijwerkingen treden op bij het begin van de behandeling en verdwijnen bij voortzetting van de therapie bij de meeste patiënten. Bijwerkingen die zijn gemeld tijdens klinische onderzoeken en/of postmarketinggebruik staan vermeld in de onderstaande tabel.
De frequentie van bijwerkingen is als volgt gedefinieerd:
Zeer vaak (≥ 1/10)
Vaak (≥ 1/100 tot
Soms (≥1 / 1.000 tot
Zeldzaam (≥1 / 10.000 tot
Erg zeldzaam (
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald)
De frequentie van bijwerkingen die tijdens postmarketinggebruik zijn ontvangen, kan niet worden bepaald omdat ze zijn afgeleid van spontane meldingen.
Daarnaast is de volgende bijwerking gemeld in klinische onderzoeken en bij gebruik na het in de handel brengen: Borstkanker bij mensen (zie rubriek 4.4)
Medische therapie van prostaatsymptomen (MTOPS)
Een studie naar de behandeling van prostaatsymptomen (MTOPS) vergeleek finasteride 5 mg / dag (n = 768), doxazosine 4 of 8 mg / dag (n = 756), de therapeutische combinatie van finasteride 5 mg / dag en doxasozine 4 of 8 mg / dag (n = 786) en placebo (n = 737) In deze studie was het veiligheids- en verdraagbaarheidsprofiel van de therapeutische combinatie over het algemeen compatibel met de profielen van de afzonderlijke componenten. De incidentie van ejaculatiestoornissen bij patiënten die de combinatietherapie kregen was vergelijkbaar met de som van de incidentie van deze bijwerking voor de twee monotherapieën.
Diagnostische toetsen
Bij het evalueren van PSA-laboratoriumresultaten moet er rekening mee worden gehouden dat de PSA-spiegels over het algemeen afnemen bij patiënten die met finasteride worden behandeld (zie rubriek 4.4). Geneesmiddel / laboratoriumtestinteracties).
Andere langetermijngegevens
In een 7 jaar durend placebogecontroleerd onderzoek met 18.882 gezonde mannen, van wie 9060 prostaatnaaldbiopsiegegevens beschikbaar hadden voor analyse, werd 803 (18,4%) van de prostaatkanker gediagnosticeerd, mannen die 5 mg finasteride gebruikten en 1147 (24,4%) mannen die placebo. In de finasteride 5 mg-groep hadden 280 (6,4%) mannen prostaatkanker met een Gleason-score van 7-10 gediagnosticeerd door naaldbiopsie versus 237 (5,1%) in de placebogroep. Aanvullende analyses suggereren dat de toename van de prevalentie van hooggradige prostaatkanker waargenomen bij mannen die 5 mg finasteride gebruikten, kan worden verklaard door een bias in de detectie als gevolg van het effect van finasteride op het prostaatvolume.Van de totale gevallen van prostaatkanker die in dit onderzoek werden gediagnosticeerd, werd ongeveer 98% geclassificeerd als intracapsulair bij diagnose (klinisch stadium T1 of T2) De betekenis c linische gegevens van de Gleason-score van 7-10 zijn niet bekend.
04.9 Overdosering
Patiënten namen enkele doses finasteride tot 400 mg en meerdere doses tot 80 mg per dag gedurende drie maanden zonder bijwerkingen te ervaren. Er kan geen specifieke behandeling worden aanbevolen met betrekking tot een overdosis finasteride.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: Testosteron-5α-reductaseremmers, ATC-code: G04CB01
Finasteride is een synthetische 4-azasteroïde, een specifieke competitieve remmer van het intracellulaire enzym 5α-reductase, type 2. Het enzym zet testosteron om in het krachtigere androgeen dihydrotestosteron (DHT). De prostaatklier en dus ook het hyperplastische prostaatweefsel zijn voor hun normale werking en groei afhankelijk van de omzetting van testosteron in DHT. Finasteride heeft geen affiniteit voor de androgeenreceptor.
Klinische studies tonen een snelle verlaging van de serum-DHT-spiegels met 70% aan, wat leidt tot een vermindering van het volume van de prostaat. Na 3 maanden is er een afname van ongeveer 20% in het volume van de klier, en de afname zet zich voort en bereikt ongeveer 27% na 3 jaar. In het periurethrale gebied direct rondom de urethra vindt een duidelijke vermindering plaats.Urodynamische metingen bevestigden ook een significante vermindering van de detrusordruk als gevolg van de verminderde obstructie.
Na een paar weken werden significante verbeteringen in de maximale urinestroomindex en symptomen bereikt in vergelijking met het begin van de behandeling. Verschillen met placebo werden gedocumenteerd na respectievelijk 4 en 7 maanden.
Alle werkzaamheidsparameters werden gehandhaafd gedurende een follow-upperiode van drie jaar.
Effecten van een 4-jarige behandeling met finasteride op de incidentie van acute urineretentie, chirurgische noodzaak, symptoomscore en prostaatvolume:
In klinische onderzoeken bij patiënten met matige tot ernstige symptomen van BPH, met een vergrote prostaat bij digitaal rectaal onderzoek en met lage resterende urinevolumes, verminderde finasteride de incidentie van acute urineretentie van 7/100 tot 3/100 in vier jaar en de noodzaak van operatie (TURP of prostatectomie) van 10/100 tot 5/100. Deze verlagingen gingen gepaard met een verbetering van 2 punten in de QUASI-AUA-symptoomclassificatie (bereik 0-34), een aanhoudende regressie van het prostaatvolume van ongeveer 20% en een aanhoudende toename van de urinestroomindex.
05.2 "Farmacokinetische eigenschappen
Absorptie
De biologische beschikbaarheid van finasteride is ongeveer 80% Piekplasmaconcentraties worden ongeveer 2 uur na inname bereikt en de absorptie is voltooid na 6-8 uur.
Verdeling
De plasma-eiwitbinding is ongeveer 93%.
De klaring en het distributievolume zijn respectievelijk ongeveer 165 ml/min (70-279 ml/min) en 76 l (44-96 l). Accumulatie van kleine hoeveelheden finasteride wordt waargenomen na herhaalde toediening.Na een dagelijkse dosis van 5 mg werd de laagste steady-state concentratie van finasteride berekend op 8-10 ng/ml en blijft stabiel in de tijd.
Biotransformatie:
Finasteride wordt gemetaboliseerd in de lever. Finasteride heeft geen significante invloed op het cytochroom P 450-enzymsysteem Er zijn twee metabolieten geïdentificeerd met een laag remmend effect op 5α-reductase.
Eliminatie:
De gemiddelde plasmahalfwaardetijd is 6 uur (4-12 uur) (bij mannen > 70 jaar: 8 uur, bereik 6 - 15 uur).
Na toediening van radioactief gelabeld finasteride werd ongeveer 39% (32 - 46%) van de dosis als metabolieten in de urine uitgescheiden Vrijwel onveranderd finasteride werd in zeer kleine hoeveelheden in de urine teruggevonden. Ongeveer 57% (51 - 64%) van de totale dosis werd uitgescheiden in de feces.
Bij patiënten met nierinsufficiëntie (creatinineklaring hoger dan 9 ml/min) werd geen verandering in de eliminatie van finasteride waargenomen (zie rubriek 4.2).
Finasteride passeert de bloed-hersenbarrière. Kleine hoeveelheden finasteride werden gedetecteerd in het sperma van behandelde patiënten. In 2 onderzoeken bij gezonde proefpersonen (n = 69), waarbij finasteride 5 mg/dag gedurende 6-24 weken werd toegediend, varieerden de finasterideconcentraties in het sperma van niet-detecteerbaar (gevoelig, de finasterideconcentraties in het sperma van 16 proefpersonen werd finasteride 5 mg/dag toegediend variërend van niet-detecteerbaar (
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Niet-klinische gegevens, gebaseerd op conventionele onderzoeken naar toxiciteit bij herhaalde dosering, genotoxiciteit en carcinogeen potentieel, duiden niet op een speciaal risico voor mensen.
Reproductietoxiciteitsonderzoeken bij mannelijke ratten toonden een verminderd gewicht van de prostaat en zaadblaasjes, verminderde secretie uit de accessoire geslachtsklieren en verminderde vruchtbaarheidsindex (veroorzaakt door het primaire farmacologische effect van finasteride). De klinische relevantie van finasteride. Deze resultaten zijn onduidelijk.
Net als bij andere 5α-reductaseremmers werd feminisering van mannelijke rattenfoetussen waargenomen bij toediening van finasteride tijdens de dracht. Bij drachtige resusapen veroorzaakte intraveneuze toediening van finasteride-doses tot 800 ng / dag gedurende de gehele periode van embryonale en foetale ontwikkeling geen afwijkingen bij mannelijke foetussen. Deze dosis is ongeveer 60-120 keer de geschatte hoeveelheid in sperma van een man die 5 mg finasteride hebben ingenomen en waaraan een vrouw via sperma kan worden blootgesteld.Bevestigend de relevantie van het rhesusmodel voor de ontwikkeling van de menselijke foetus, orale toediening van finasteride 2 mg/kg/dag (systemische blootstelling (AUC) van apen, was iets hoger (3x) dan bij mannen die 5 mg finasteride gebruikten, of ongeveer 1-2 miljoen keer de geschatte hoeveelheid finasteride in sperma) bij drachtige apen resulteerde in afwijkingen van de geslachtsorganen uitwendig van mannelijke foetussen. Er werden geen andere afwijkingen waargenomen bij mannelijke foetussen en er werden bij geen enkele dosis finasteride-gerelateerde afwijkingen waargenomen bij vrouwelijke foetussen.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Kern van de tablet:
Lactosemonohydraat
Microkristallijne cellulose
Voorgegelatineerd zetmeel (maïs)
Laurine macrogolglyceriden
Natriumzetmeelglycolaat (Type A)
Magnesium stearaat
Coating:
Hypromellose
Macrogol
Titaandioxide (E171)
Indigokarmijn aluminiumlak (E132)
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar
06.4 Speciale voorzorgsmaatregelen bij bewaren
Voor dit geneesmiddel zijn er geen speciale bewaarcondities
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Aluminium/PVC of Aluminium/Aluminium blisterverpakkingen: 15 tabletten.
06.6 Instructies voor gebruik en verwerking
Zwangere vrouwen of vrouwen die zwanger kunnen worden, mogen geen gebroken of gebroken finasteridetabletten hanteren vanwege de mogelijkheid van absorptie van finasteride en het daaruit voortvloeiende potentiële risico voor een mannelijke foetus (zie rubriek 4.6).
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Actavis Group PTC ehf - Reykjavikurvegi 76-78, 220 Hafnarfjördur (IJsland)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AIC n. 037774231 / M "5 mg filmomhulde tabletten", 15 tabletten in PVC/Al blisterverpakking
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Bepaling nt 573/2007 van 25-07-2007
10.0 DATUM VAN HERZIENING VAN DE TEKST
juli 2012