Algemeenheid
Amyloïdose is de term die wordt gebruikt om een groep ziekten te definiëren die wordt gekenmerkt door de accumulatie, vaak in het extracellulaire gebied, van een fibrillair eiwitmateriaal, gedefinieerd als amyloïde.Onoplosbare amyloïdefibrillen vormen bijzonder stabiele afzettingen in talrijke organen.

Andere foto's Amyloïdose - Gallery 2
Symptomen en ernst van de ziekte hangen af van het orgaan dat voornamelijk wordt aangetast door amyloïdaccumulatie en het type amyloïdose. De meeste gevallen zijn echter systemisch. Met andere woorden, fibrillaire afzettingen zijn wijdverbreid en kunnen mogelijk de functie van veel weefsels en organen van het lichaam aantasten. . De diagnose wordt bepaald door biopsie, door een klein stukje weefsel onder een microscoop te onderzoeken. Potentiële etiologische factoren variëren afhankelijk van de variant van amyloïdose. Beschikbare behandelingen kunnen de symptomen helpen beheersen en de productie van amyloïden beperken.
Kenmerken van amyloïde afzettingen
Amyloïdose komt voort uit aandoeningen van de secundaire structuur van eiwitten (met een β-gevouwen bladconfiguratie) In normale omstandigheden worden eiwitten in feite gesynthetiseerd in een lineaire reeks aminozuren, die, wanneer ze worden gevouwen, een specifieke ruimtelijke conformatie aanneemt (eiwitvouwing). Dankzij zijn structuur, dus door de juiste eiwitvouwing, is het eiwit in staat om de fysiologische functies uit te voeren waarvoor het verantwoordelijk is. De amyloïde-eiwitten zijn afkomstig van een voorloper die verkeerd door de cellen wordt verwerkt (vanwege "misvouwing" "). De eiwitten die fibrillen vormen, worden gediversifieerd volgens grootte, aminozuursequentie en natieve structuur, maar worden onoplosbare aggregaten die qua structuur en eigenschappen vergelijkbaar zijn. De voorlopers van fibrillen worden weergegeven door primaire moleculen (voorbeeld: lichte keten van immunoglobulinen, β2-microglobuline, apolipoproteïne A1, enz.) of van producten die een verandering in de s weerspiegelen aminozuur volgorde. De afwijkende secundaire structuur predisponeert voor de vorming van fibrillen, die lokaal in weefsels en organen kunnen worden afgezet en leiden tot de verslechtering van hun normale fysiologische functie.Er zijn meer dan 20 verschillende eiwitprecursoren geïdentificeerd die een amyloïde conformatie kunnen aannemen, die waarom ze veel verschillende soorten amyloïdose hebben.
Op basis van de locatie van de amyloïde afzettingen kan de ziekte worden onderverdeeld in:
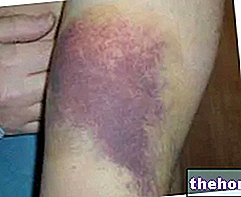
- Gelokaliseerde vorm: beperkt tot een bepaald orgaan of weefsel (hart, nieren, maagdarmkanaal, zenuwstelsel en dermis) en is meestal minder ernstig dan systemische (diffuse) vormen. Amyloïdose kan bijvoorbeeld alleen de huid aantasten, waardoor verkleuring en/of jeuk ontstaat. Een bepaald type amyloïd-eiwit is ook gevonden in de hersenen van patiënten met de ziekte van Alzheimer. Gelokaliseerde amyloïdose is typerend voor senescentie en getroffen patiënten. vanaf diabetes type 2 (waar eiwit zich ophoopt in de pancreas).
- Systemische vorm: amyloïde afzettingen zijn aanwezig in verschillende organen en herkennen in het algemeen neoplastische, inflammatoire, genetische of iatrogene oorsprong Systemische amyloïdose is vaak zeer ernstig: het beschadigt gewoonlijk het hart, de nieren, de darmen en de zenuwen, waardoor progressieve insufficiëntie van het orgaan ontstaat.
Classificatie
Er zijn veel vormen van amyloïdose, ingedeeld naar de aard van de eiwitten waaruit de fibrillaire afzettingen bestaan.
De meest voorkomende varianten zijn:
- Primaire amyloïdose (ook wel lichte keten amyloïdose, AL genoemd);
- Secundaire amyloïdose (ook wel verworven amyloïdose, AA genoemd);
- Erfelijke amyloïdose;
- Met veroudering geassocieerde amyloïdose (of seniele systemische amyloïdose).