Actieve ingrediënten: Totale triterpeenfractie van Centella asiatica
Centellase 30 mg tabletten
Waarom wordt centellase gebruikt? Waar is het voor?
Centellase is een geneesmiddel op basis van Centella asiatica, een geneesmiddel dat wordt gebruikt om de aderen te beschermen.
Centellase is geïndiceerd bij de behandeling van:
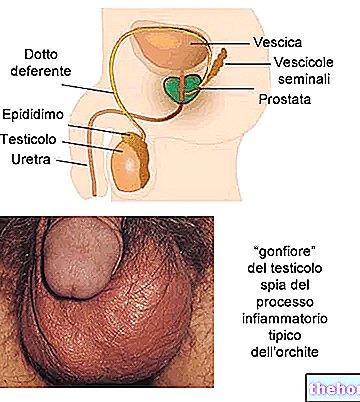
- zwelling in de enkels en benen door veneuze insufficiëntie, zwaar gevoel in de benen, tintelingen en jeuk in de benen, nachtelijke krampen in de benen en zichtbare haarvaten;
- kwetsbaarheid van haarvaten.
Neem contact op met uw arts als u zich niet beter voelt of als u zich slechter voelt.
Contra-indicaties Wanneer Centellase niet mag worden gebruikt
Gebruik Centellase niet
- als u allergisch bent voor de werkzame stof of voor één van de andere bestanddelen van dit geneesmiddel
Voorzorgsmaatregelen bij gebruik Wat u moet weten voordat u Centellase inneemt
Er zijn geen speciale voorzorgsmaatregelen voor het gebruik van dit geneesmiddel.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Centellase veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Gebruik dit geneesmiddel niet tijdens zwangerschap en borstvoeding omdat de effecten niet bekend zijn.
als u zwanger bent of borstvoeding geeft, denkt zwanger te zijn of zwanger wilt worden, vraag dan uw arts of apotheker om advies voordat u dit geneesmiddel inneemt.
Rijvaardigheid en het gebruik van machines
Centellase heeft geen invloed op de rijvaardigheid of het vermogen om machines te bedienen.
Dosis, wijze en tijdstip van toediening Hoe Centellase te gebruiken: Dosering
Gebruik dit geneesmiddel altijd precies zoals beschreven in deze bijsluiter of zoals voorgeschreven door uw arts of apotheker. Raadpleeg bij twijfel uw arts of apotheker.
De aanbevolen dosering is 1 tot 2 tabletten per dag, bij voorkeur tijdens de maaltijd.
Hoe te gebruiken: de tabletten moeten heel worden doorgeslikt met water
Duur van de behandeling: Gebruik dit geneesmiddel alleen voor korte behandelingsperioden. Raadpleeg uw arts als de aandoening herhaaldelijk voorkomt of als u recente veranderingen in de kenmerken ervan heeft opgemerkt.
Bijwerkingen Wat zijn de bijwerkingen van Centellase
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Het gebruik van het geneesmiddel kan jeuk veroorzaken of aanleiding geven tot verschijnselen van gevoeligheid voor de zon en UV-stralen (fotosensibilisatie) met het verschijnen van roodheid en rode en/of gezwollen vlekken (huiduitslag).
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via de website: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos na "EXP". De vervaldatum verwijst naar de laatste dag van die maand.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Welke stoffen zitten er in Centellase?
- Het actieve ingrediënt is: totale triterpeenfractie van Centella asiatica
- De andere stoffen in dit middel zijn: dibasisch calciumfosfaatdihydraat, docusaatnatrium, povidon, croscarmellose-natrium, carmellose-natrium, magnesiumstearaat.
Hoe ziet Centellase eruit en wat is de inhoud van de verpakking
Centellase wordt geleverd in een kartonnen doos met 30 tabletten verpakt in blisterverpakkingen.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
CENTELLASE TABLETTEN
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1 tablet bevat: totale triterpeenfractie van gotuola (asiaticoside 40% - asiatic acid + madecassic acid 60%) 30 mg.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Tabletten.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Symptomen toe te schrijven aan veneuze insufficiëntie; staten van capillaire fragiliteit.
04.2 Dosering en wijze van toediening
Dosering
1 tot 2 tabletten per dag, bij voorkeur bij de maaltijd.
Het geneesmiddel mag slechts gedurende een korte behandelingsperiode worden gebruikt.
Wijze van toediening: oraal gebruik.
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Geen bijzondere voorzorgsmaatregelen voor het gebruik van het product.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Er zijn geen interacties met andere geneesmiddelen bekend.
04.6 Zwangerschap en borstvoeding
Uit dieronderzoek is geen reproductietoxiciteit gebleken. Er zijn geen adequate gegevens over het gebruik van het geneesmiddel bij zwangere vrouwen of vrouwen die borstvoeding geven. Centellase mag niet worden gebruikt tijdens zwangerschap en borstvoeding.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Centellase heeft geen invloed op de rijvaardigheid of het vermogen om machines te bedienen.
04.8 Bijwerkingen
Gevallen van jeuk en fotosensitiviteitsreacties met het verschijnen van roodheid en huiduitslag zijn gemeld na orale toediening van het geneesmiddel.
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres: http ://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Er zijn geen gevallen van overdosering gemeld.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: vasoprotectors.
ATC-code: C05CX.
Werkingsmechanisme
De triterpeenfractie van Centella asiatica (FTTCA) heeft modulerende eigenschappen op de ontwikkeling van bindweefsel, wat resulteert in een verbetering van de tonus en elasticiteit van de veneuze wand, waardoor de endotheelpermeabiliteit (afname van stasis en diapedese bij het capillaire niveau), om in de loop van de tijd het hemodynamisch evenwicht te herstellen op het niveau van het microvasculaire systeem van weefsel, waarvan de verandering de oorzaak is van de symptomatologie die gepaard gaat met het spatadersyndroom.
05.2 Farmacokinetische eigenschappen
Absorptie
De FTTCA wordt na orale toediening snel geabsorbeerd en bereikt de maximale plasmaspiegel rond 4 uur. Na epicutane toediening vertoont het product een bloedpiek tussen het 6e en 12e uur.
Biotransformatie en eliminatie
De actieve ingrediënten worden niet door het lichaam gemetaboliseerd en worden als zodanig via de fecale route geëlimineerd.
Er is een entero-hepatische circulatie aangetoond.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Er is geen informatie, afgeleid van preklinische gegevens, die van significant belang is voor de arts die niet al is vermeld in de andere rubrieken van de Samenvatting van de Productkenmerken.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Dibasisch calciumfosfaatdihydraat, docusaatnatrium, povidon, croscarmellose-natrium, carmellosenatrium, magnesiumstearaat.
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
5 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
De tabletten zijn ingesloten in plastic materiaal, hitteverzegeld met aluminium (blisterverpakking) en samen met de bijsluiter in een kartonnen doos geplaatst.
Doos met 30 tabletten.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies voor verwijdering.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Farmaceutisch laboratorium SIT S.r.l. - Via Cavour, 70 - 27035 Mede (PV)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AIC: 016222073
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste vergunning: november 1982.
Datum van de meest recente verlenging: mei 2010.
10.0 DATUM VAN HERZIENING VAN DE TEKST
AIFA-beschikking van 21 juli 2014.