Actieve ingrediënten: Pioglitazon
Actos 15 mg tabletten
Actos-bijsluiters zijn beschikbaar voor verpakkingsgrootten:- Actos 15 mg tabletten
- Actos 30 mg tabletten
- Actos 45 mg tabletten
Waarom wordt Actos gebruikt? Waar is het voor?
Actos bevat pioglitazon. Het is een middel tegen diabetes dat wordt gebruikt voor de behandeling van type 2 (niet-insulineafhankelijke) diabetes mellitus, wanneer metformine niet geschikt is of niet goed heeft gewerkt. Dit type diabetes komt meestal voor bij volwassenen.
Actos helpt de bloedsuikerspiegel onder controle te houden als u diabetes type 2 heeft door uw lichaam te helpen de insuline die het aanmaakt beter te gebruiken. Uw arts zal 3-6 maanden na aanvang van de behandeling controleren of Actos werkt.
Actos kan alleen worden gebruikt bij patiënten die niet in staat zijn om metformine in te nemen en bij wie dieet en oefentherapie niet hebben geleid tot controle van de bloedsuikerspiegel, of het kan worden toegevoegd aan andere therapieën (zoals metformine, een sulfonylureumderivaat of "insuline), die niet voor voldoende controle van de bloedglucose zorgen.
Contra-indicaties Wanneer Actos niet mag worden gebruikt
Gebruik Actos niet
- als u overgevoelig (allergisch) bent voor pioglitazon of voor één van de andere bestanddelen van Actos.
- als u hartfalen heeft of in het verleden aan hartfalen heeft geleden.
- als u lijdt aan leverproblemen.
- als u lijdt aan diabetische ketoacidose (een complicatie van diabetes die snel gewichtsverlies, misselijkheid of braken veroorzaakt).
- als u blaaskanker (blaaskanker) heeft of ooit heeft gehad.
- als u bloed in uw urine heeft dat uw arts nog niet heeft gecontroleerd.
Voorzorgen bij gebruik Wat u moet weten voordat u Actos inneemt
Wees extra voorzichtig met Actos
Vertel het uw arts voordat u dit geneesmiddel gaat gebruiken
- als u vocht tegenhoudt (vochtretentie) of problemen heeft met hartfalen, vooral als u ouder bent dan 75 jaar. Vertel het uw arts ook als u ontstekingsremmende geneesmiddelen gebruikt, die ook vochtretentie en zwelling kunnen veroorzaken,
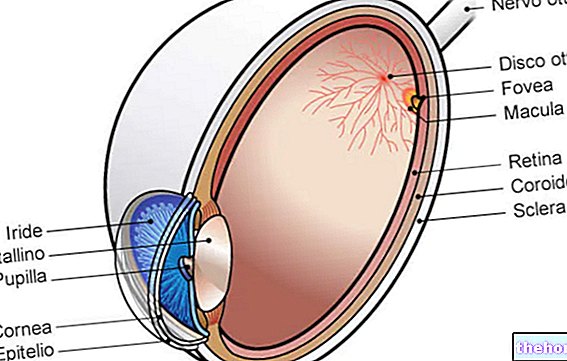
- als u een speciaal type diabetische oogziekte heeft die macula-oedeem wordt genoemd (zwelling van de achterkant van het oog).
- als u ovariumcysten heeft (polycysteus ovariumsyndroom) De kans om zwanger te worden kan toenemen, omdat de eisprong kan hervatten wanneer u Actos gebruikt. Als dit het geval is, gebruik dan adequate anticonceptie om het risico van een ongeplande zwangerschap te voorkomen.
- als u lever- of hartproblemen heeft. Voordat u Actos gaat gebruiken, krijgt u een bloedonderzoek om uw leverfunctie te controleren. Deze test kan periodiek worden herhaald. Sommige patiënten met langdurige diabetes mellitus type 2 en hartaandoeningen of een eerdere beroerte die werden behandeld met Actos en insuline, hebben hartfalen ervaren. Vertel het uw arts zo snel mogelijk als u tekenen van hartfalen ervaart, zoals ongewone kortademigheid of snelle gewichtstoename of plaatselijke zwelling (oedeem).
Als u Actos inneemt met andere geneesmiddelen tegen diabetes, is de kans groter dat uw bloedsuiker tot onder normaal daalt (hypoglykemie). Het kan ook een daling van het aantal bloedcellen hebben (bloedarmoede).
Botbreuken
Er is een groter aantal botbreuken gevonden bij patiënten, vooral bij vrouwen die pioglitazon gebruiken. Uw arts zal hiermee rekening houden bij de behandeling van uw diabetes.
Kinderen
Gebruik bij kinderen onder de 18 jaar wordt niet aanbevolen.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Actos . veranderen?
Actos innemen met andere geneesmiddelen
Vertel uw arts of apotheker als u andere geneesmiddelen gebruikt of kort geleden heeft gebruikt. Dit geldt ook voor geneesmiddelen die u zonder voorschrift kunt krijgen.
U kunt gewoonlijk andere geneesmiddelen blijven gebruiken terwijl u met Actos wordt behandeld.
Het is echter waarschijnlijk dat sommige geneesmiddelen de hoeveelheid suiker in het bloed beïnvloeden:
- gemfibrozil (gebruikt om het cholesterolgehalte te verlagen)
- rifampicine (gebruikt om tuberculose en andere infecties te behandelen)
Vertel het uw arts of apotheker als u een van deze geneesmiddelen gebruikt. Uw bloedsuikerspiegel zal worden gecontroleerd en uw Actos-dosis moet mogelijk worden gewijzigd.
Waarop moet u letten met eten en drinken
U kunt de tabletten met of zonder voedsel innemen. U moet de tabletten met een glas water innemen.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
Vertel het uw arts als:
- zwanger bent, als u denkt zwanger te zijn of van plan bent zwanger te worden.
- u borstvoeding geeft of van plan bent uw baby borstvoeding te geven.
Uw arts zal u adviseren om te stoppen met het gebruik van dit geneesmiddel.
Rijvaardigheid en het gebruik van machines
Pioglitazon heeft geen invloed op de rijvaardigheid of op het vermogen om machines te bedienen, maar wees voorzichtig als u gezichtsstoornissen heeft.
Belangrijke informatie over enkele bestanddelen van Actos
Dit geneesmiddel bevat lactosemonohydraat. Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u Actos inneemt.
Dosis, wijze en tijdstip van toediening Hoe Actos te gebruiken: Dosering
Eén tablet pioglitazon 15 mg dient eenmaal per dag te worden ingenomen. Indien nodig kan uw arts u vertellen een andere dosis in te nemen. Als u de indruk heeft dat het effect van Actos te zwak is, neem dan contact op met uw arts.
Wanneer Actos-tabletten worden ingenomen in combinatie met andere geneesmiddelen die worden gebruikt om diabetes te behandelen (zoals insuline, chloorpropamide, glibenclamide, gliclazide, tolbutamide), zal uw arts u vertellen of u een lagere dosis van de andere geneesmiddelen moet gebruiken.
Uw arts zal u vragen om periodiek bloedonderzoek te laten doen tijdens de behandeling met Actos. Dit is om de normale werking van de lever te controleren.
Als u een diabetesdieet volgt, moet u dit voortzetten terwijl u Actos gebruikt.
Het gewicht moet regelmatig worden gecontroleerd; als uw gewicht toeneemt, vertel dit dan aan uw arts.
Overdosering Wat te doen als u te veel Actos heeft ingenomen
Wat u moet doen als u meer Actos-tabletten heeft ingenomen dan u zou mogen
Als u per ongeluk te veel tabletten heeft ingenomen, of als iemand of een kind uw tabletten heeft ingenomen, neem dan onmiddellijk contact op met uw arts of apotheker. Uw bloedsuikerspiegel kan dalen tot onder het normale niveau en kan stijgen door suikerinname. Het is raadzaam om suikerklontjes, snoepjes, koekjes of suikerhoudende vruchtensappen mee te nemen.
Wat u moet doen wanneer u bent vergeten Actos-tabletten in te nemen
Probeer Actos elke dag in te nemen zoals voorgeschreven. Als u echter een dosis vergeet in te nemen, ga dan gewoon door met de volgende dosis. Neem geen dubbele dosis om een vergeten tablet in te halen.
Als u stopt met het innemen van Actos
Actos moet elke dag worden gebruikt om goed te werken. Als u stopt met het gebruik van Actos, kan uw bloedsuikerspiegel stijgen. Praat met uw arts voordat u stopt met de behandeling.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Actos
Zoals alle geneesmiddelen kan Actos bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Bij sommige patiënten zijn met name de volgende ernstige bijwerkingen opgetreden:
Hartfalen kwam vaak voor (1 tot 10 gebruikers op 100) bij patiënten die Actos in combinatie met insuline gebruikten. Symptomen zijn ongebruikelijke kortademigheid of snelle gewichtstoename of plaatselijke zwelling (oedeem). Als u een van deze symptomen ervaart, vooral als u ouder bent dan 65, zoek dan onmiddellijk medische hulp.
Soms zijn er gevallen van blaaskanker (blaaskanker) opgetreden (1 tot 10 op de 1000 patiënten) bij patiënten die Actos gebruikten. Tekenen en symptomen zijn onder meer bloed in de urine, pijn bij het plassen of de plotselinge behoefte om te plassen. Als u een van deze symptomen krijgt, neem dan zo snel mogelijk contact op met uw arts.
Er zijn zeer vaak gevallen van plaatselijke zwelling (oedeem) geweest bij patiënten die Actos in combinatie met insuline gebruikten. Vertel het uw arts zo snel mogelijk als u deze bijwerking krijgt.
Er zijn vaak meldingen geweest (1 tot 10 gebruikers op 100) van botbreuken bij vrouwen die Actos gebruiken. Als u deze bijwerking ervaart, vertel dit dan zo snel mogelijk aan uw arts.
Wazig zien als gevolg van zwelling (of vocht) van de achterkant van het oog (frequentie niet bekend) is ook gemeld bij patiënten die Actos gebruiken Vertel het uw arts zo snel mogelijk als u deze symptomen voor de eerste keer opmerkt. zo snel mogelijk, zelfs als u al wazig ziet en het symptoom erger wordt.
Allergische reacties zijn gemeld (frequentie niet bekend) bij patiënten die Actos gebruiken. Als u een ernstige allergische reactie heeft, waaronder netelroos en zwelling van het gezicht, de lippen, de tong of de keel, waardoor u moeilijk kunt ademen of slikken, stop dan met het innemen van dit geneesmiddel en neem zo snel mogelijk contact op met uw arts.
De andere bijwerkingen die zijn opgetreden bij sommige patiënten die Actos gebruikten, zijn:
vaak (komt voor bij 1 tot 10 op de 100 patiënten)
- luchtweginfecties
- abnormaal zicht
- gewichtstoename
- doof gevoel
soms (komt voor bij 1 tot 10 op de 1.000 gebruikers)
- ontsteking van de sinussen (sinusitis)
- moeite met slapen (slapeloosheid)
niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald)
- verhoogde leverenzymen.
- allergische reacties
De andere bijwerkingen die bij sommige patiënten zijn opgetreden bij het gebruik van Actos samen met andere antidiabetica zijn:
zeer vaak (komt voor bij meer dan één op de 10 patiënten)
- verlaagde bloedsuikerspiegel (hypoglykemie)
vaak (komt voor bij 1 tot 10 op de 100 patiënten)
- hoofdpijn
- duizeligheid
- gewrichtspijn
- impotentie
- rugpijn
- kortademigheid
- een kleine afname van het aantal rode bloedcellen in het bloed
- winderigheid
soms (komt voor bij 1 tot 10 op de 1.000 gebruikers)
- suiker in de urine, eiwit in de urine
- verhoogde enzymen
- draaierig gevoel (duizeligheid)
- zweten
- vermoeidheid
- verhoogde eetlust
Als een van de bijwerkingen ernstig wordt of als er bij u een bijwerking optreedt die niet in deze bijsluiter is vermeld, raadpleeg dan uw arts of apotheker.
Vervaldatum en retentie
Buiten het bereik en zicht van kinderen houden.
Gebruik Actos niet meer na de vervaldatum die staat vermeld op de doos en op de blisterverpakking na het woord "EXP". De vervaldatum verwijst naar de laatste dag van de maand.
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
Wat bevat Actos
- Het actieve ingrediënt in Actos is pioglitazon. Elke tablet bevat 15 mg pioglitazon (als hydrochloride).
- De andere stoffen in dit middel zijn lactosemonohydraat, hyprolose, carmellosecalcium en magnesiumstearaat.
Hoe ziet Actos eruit en wat is de inhoud van de verpakking
Actos-tabletten zijn wit tot gebroken wit, rond, convex, met de inscriptie "15" aan de ene kant en "ACTOS" aan de andere. De tabletten worden geleverd in blisterverpakkingen, in verpakkingen van 14, 28, 30, 50, 56, 84, 90, 98, 112 of 196 tabletten. Niet alle genoemde verpakkingsgrootten worden in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
ACTOS 15 MG-TABLETTEN
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet bevat 15 mg pioglitazon (als hydrochloride).
Hulpstoffen:
Elke tablet bevat 92,87 mg lactosemonohydraat (zie rubriek 4.4).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Tablet.
De tabletten zijn wit tot gebroken wit, rond, convex en gemarkeerd met "15" aan de ene kant en "ACTOS" aan de andere.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Pioglitazon is geïndiceerd als tweede- of derdelijnsbehandeling voor diabetes mellitus type 2, zoals hieronder beschreven:
in monotherapie
• bij volwassen patiënten (met name patiënten met overgewicht) die onvoldoende onder controle zijn door dieet en lichaamsbeweging voor wie behandeling met metformine niet geschikt is vanwege contra-indicaties of intolerantie.
Bij duale orale therapie in combinatie met:
• metformine, bij volwassen patiënten (met name patiënten met overgewicht) met onvoldoende glykemische controle ondanks de maximaal verdraagbare dosis van metformine als monotherapie
• een sulfonylureumderivaat, alleen bij volwassen patiënten die intolerantie vertonen voor metformine of voor wie metformine gecontra-indiceerd is, met onvoldoende glykemische controle ondanks de maximaal verdraagbare dosis monotherapie met een sulfonylureumderivaat
Bij drievoudige orale therapie in combinatie met:
• metformine en een sulfonylureumderivaat, bij volwassen patiënten (met name patiënten met overgewicht) met onvoldoende glykemische controle ondanks dubbele orale therapie
• Pioglitazon is ook geïndiceerd in combinatie met insuline bij volwassen patiënten met type 2 diabetes mellitus die niet voldoende glykemische controle krijgen met insuline, voor wie het gebruik van metformine niet geschikt is vanwege contra-indicaties of intolerantie (zie rubriek 4.4).
Na het starten van de behandeling met pioglitazon moeten patiënten na 3-6 maanden opnieuw worden geëvalueerd om de adequaatheid van de respons op de behandeling te verifiëren (bijv. verlaging van HbA1c). Bij patiënten die niet adequaat reageren, moet de behandeling met pioglitazon worden stopgezet. In het licht van de mogelijke risico's van langdurige therapie, dienen voorschrijvers bij volgende bezoeken te bevestigen dat de voordelen van behandeling met pioglitazon behouden blijven (zie rubriek 4.4).
04.2 Dosering en wijze van toediening
Dosering
De behandeling met pioglitazon kan worden gestart met een startdosering van 15 mg of 30 mg eenmaal daags.De dosis kan geleidelijk worden verhoogd tot eenmaal daags 45 mg.
In combinatie met insuline kan aan het begin van de behandeling met pioglitazon de huidige insulinedosis worden gehandhaafd.Als patiënten hypoglykemie melden, moet de insulinedosis worden verlaagd.
Speciale populaties
Bejaarden
Bij oudere patiënten is geen dosisaanpassing nodig (zie rubriek 5.2). Artsen moeten de behandeling starten met de laagst beschikbare dosis en deze geleidelijk verhogen, vooral wanneer pioglitazon wordt gebruikt in combinatie met insuline (zie rubriek 4.4 Vochtretentie en hartfalen).
Nierfalen
Er is geen dosisaanpassing nodig bij patiënten met een verminderde nierfunctie (creatinineklaring > 4 ml/min) (zie rubriek 5.2). Er is geen informatie beschikbaar over dialysepatiënten, daarom mag pioglitazon niet bij dergelijke patiënten worden gebruikt.
Leverinsufficiëntie
Pioglitazon mag niet worden gebruikt bij patiënten met leverinsufficiëntie (zie rubrieken 4.3 en 4.4).
Pediatrische populatie
De veiligheid en werkzaamheid van Actos bij kinderen en adolescenten jonger dan 18 jaar zijn nog niet vastgesteld.
Er zijn geen gegevens beschikbaar.
Wijze van toediening
Pioglitazon-tabletten worden eenmaal daags oraal ingenomen, met of zonder voedsel. De tabletten moeten worden doorgeslikt met een glas water.
04.3 Contra-indicaties
Pioglitazon is gecontra-indiceerd bij patiënten met:
• overgevoeligheid voor de werkzame stof of voor één van de hulpstoffen.
• hartfalen of voorgeschiedenis van hartfalen (NYHA-stadia I tot IV)
• Leverfalen
• diabetische ketoacidose
• actieve blaaskanker of geschiedenis van blaaskanker
• grove hematurie van onbepaalde aard
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Waterretentie en hartfalen
Pioglitazon kan vochtretentie veroorzaken, wat hartfalen kan verergeren of versnellen. Bij de behandeling van patiënten met ten minste één risicofactor voor het ontwikkelen van congestief hartfalen (bijv. een eerder myocardinfarct, symptomatische coronaire hartziekte of ouderen), moeten artsen de behandeling starten met de laagst beschikbare dosis en de dosis geleidelijk verhogen. Patiënten moeten worden geobserveerd op tekenen en symptomen van hartfalen, gewichtstoename of oedeem; vooral die met een verminderde hartreserve.
Er zijn postmarketingmeldingen geweest van hartfalen bij gebruik van pioglitazon in combinatie met insuline of bij patiënten met een voorgeschiedenis van hartfalen. Patiënten moeten worden geobserveerd op tekenen en symptomen van hartfalen, gewichtstoename en oedeem wanneer pioglitazon wordt gebruikt in combinatie met insuline. Aangezien zowel insuline als pioglitazon geassocieerd zijn met vochtretentie, kan gelijktijdige toediening het risico op oedeem verhogen. Er zijn ook postmarketingmeldingen geweest van perifeer oedeem en hartfalen bij patiënten met gelijktijdig gebruik van pioglitazon en niet-steroïde anti-inflammatoire geneesmiddelen, waaronder selectieve COX-2-remmers. Pioglitazon moet worden stopgezet als er een verslechtering van de hartstatus optreedt.
Een cardiovasculaire uitkomststudie van pioglitazon werd uitgevoerd bij patiënten jonger dan 75 jaar met type 2 diabetes mellitus en een reeds bestaande ernstige macrovasculaire ziekte. Pioglitazon of placebo werden gedurende maximaal 3,5 jaar toegevoegd aan lopende antidiabetica en cardiovasculaire therapie. Deze studie toonde een toename van hartfalenrapporten, maar dit leidde niet tot een toename van de mortaliteit in deze studie.
Bejaarden
Het gecombineerde gebruik van pioglitazon en insuline moet met voorzichtigheid worden overwogen bij ouderen vanwege het verhoogde risico op ernstig hartfalen.
In het licht van leeftijdgerelateerde risico's (met name blaaskanker, fracturen en hartfalen), moet de afweging van voordelen en risico's bij ouderen zorgvuldig worden afgewogen, zowel voor als tijdens de behandeling met pioglitazon.
Blaaskanker
In een meta-analyse van gecontroleerde klinische onderzoeken werden gevallen van blaaskanker vaker gemeld bij pioglitazon (19 gevallen van 12.506 patiënten, 0,15%) dan in controlegroepen (7 gevallen van 10.212 patiënten, 0,07%) HR = 2,64 (95 % BI; 1,11-6,31; P = 0,029). Na uitsluiting van patiënten bij wie de blootstelling aan het onderzoeksgeneesmiddel minder dan één jaar was op het moment dat de diagnose van blaaskanker werd gesteld, waren er 7 gevallen van pioglitazon (0,06%) terwijl die in de controlegroepen 2 waren (0,02%). risico op blaaskanker bij diabetespatiënten die met pioglitazon worden behandeld, met name bij patiënten die gedurende langere perioden en met de hogere cumulatieve doses worden behandeld.Een mogelijk risico na kortdurende behandelingen is uitgesloten.
Risicofactoren voor blaaskanker moeten worden geëvalueerd voordat de behandeling met pioglitazon wordt gestart (risico's zijn onder meer leeftijd, roken, blootstelling aan bepaalde stoffen die op de werkplek worden gebruikt of chemotherapie zoals cyclofosfamide of eerdere radiotherapie met blootstelling aan het bekkengebied.). Elke grove hematurie moet worden onderzocht voordat de behandeling met pioglitazon wordt gestart.
Patiënten dienen onmiddellijk hun arts te raadplegen als tijdens de behandeling symptomen zoals ernstige hematurie, dysurie of aandrang tot urineren optreden.
Monitoring van de leverfunctie
Hepatocellulaire disfunctie is zelden gemeld tijdens postmarketingervaring (zie rubriek 4.8). Het wordt daarom aanbevolen dat patiënten die met pioglitazon worden behandeld, periodieke controle van de leverenzymen ondergaan. Leverenzymen dienen te worden gecontroleerd voordat de behandeling met pioglitazon wordt gestart bij alle patiënten Pioglitazon de behandeling mag niet worden gestart bij patiënten met verhoogde baseline leverenzymwaarden (ALAT > 2,5 maal ULN) of met enig bewijs van leverziekte.
Na het starten van de behandeling met pioglitazon wordt aanbevolen dat de leverenzymen indien nodig klinisch periodiek worden gecontroleerd.Als de ALT-spiegels tijdens behandeling met pioglitazon driemaal de bovengrens van normaal zijn, moeten de leverenzymspiegels zo snel mogelijk opnieuw worden beoordeeld. De ALAT-spiegels blijven > 3 maal de bovengrens van normaal, de therapie moet worden gestaakt Als een patiënt symptomen ervaart die wijzen op een leverfunctiestoornis, waaronder onverklaarbare misselijkheid, braken, buikpijn, vermoeidheid, anorexia en/of donkere urine, dienen leverenzymen De beslissing om de patiënt al dan niet met pioglitazon te blijven behandelen, moet worden gebaseerd op een klinisch oordeel in afwachting van laboratoriumonderzoeken. Als geelzucht optreedt, moet het geneesmiddel worden stopgezet.
Gewichtstoename
In klinische onderzoeken met pioglitazon zijn aanwijzingen gevonden voor een dosisgerelateerde gewichtstoename, die het gevolg kan zijn van vetophoping en in sommige gevallen gepaard gaat met vochtretentie. In sommige gevallen kan gewichtstoename een symptoom zijn van hartfalen, dus het gewicht moet zorgvuldig worden gecontroleerd. Dieetcontrole maakt deel uit van de diabetesbehandeling. Patiënten moeten erop worden gewezen dat ze strikt een caloriebeperkt dieet moeten volgen.
hematologie
Een lichte afname van de gemiddelde hemoglobine (relatieve afname van 4%) en hematocriet (relatieve afname van 4,1%) werd waargenomen tijdens behandeling met pioglitazon, bestaande uit hemodilutie. Soortgelijke veranderingen werden waargenomen bij patiënten die werden behandeld met metformine (relatieve verlaging van hemoglobine 3-4% en hematocriet 3,6-4,1%) en in mindere mate bij patiënten die werden behandeld met sulfonylureumderivaten en insuline (relatieve verlaging van hemoglobine 1-2% en hematocriet 1 -3,2%) in vergelijkende gecontroleerde onderzoeken met pioglitazon.
Hypoglykemie
Als gevolg van een verhoogde insulinegevoeligheid kunnen patiënten die pioglitazon krijgen in twee- of drievoudige orale therapie met een sulfonylureumderivaat of tweevoudige therapie met insuline een risico lopen op dosisgerelateerde hypoglykemie, en een verlaging van de dosis van het sulfonylureumderivaat kan nodig zijn. .
Visuele stoornissen
Post-marketing gevallen van nieuwe aanvang of verergering van diabetisch macula-oedeem met verminderde gezichtsscherpte zijn gemeld met thiazolidinedionen, waaronder pioglitazon. Veel van deze patiënten kregen gelijktijdig perifeer oedeem. Het is onduidelijk of er al dan niet een direct verband bestaat tussen pioglitazon en macula-oedeem, maar artsen moeten alert zijn op de mogelijkheid van macula-oedeem als patiënten gezichtsscherptestoornissen melden; passend oogheelkundig onderzoek moet worden overwogen.
Ander
In een "cumulatieve analyse van bijwerkingen van botbreuken gemeld uit gerandomiseerde, gecontroleerde, dubbelblinde klinische onderzoeken bij meer dan 8.100 patiënten behandeld met pioglitazon en 7.400 behandeld met comparator gedurende meer dan 3,5 jaar, a" verhoogde incidentie van botbreuken bij vrouwen.
Fracturen werden waargenomen bij 2,6% van de vrouwen die werden behandeld met pioglitazon vergeleken met 1,7% van de vrouwen die werden behandeld met een comparator.Er werd geen toename van de incidentie van fracturen waargenomen bij mannen die werden behandeld met pioglitazon (1,3%) in vergelijking met de vergelijkingsgroep (1,5%).
De berekende incidentie van fracturen was 1,9 fracturen per 100 patiëntjaren bij vrouwen die werden behandeld met pioglitazon en 1,1 fracturen per 100 patiëntjaren bij vrouwen die werden behandeld met een comparator.Het verhoogde risico op fracturen voor vrouwen in deze dataset voor pioglitazon was daarom 0,8 fracturen per 100 patiëntjaren.
In de 3,5 jaar durende cardiovasculaire risicostudie PROactive ondervonden 44/870 (5,1%; 1,0 fracturen per 100 patiëntjaren) van vrouwelijke patiënten die werden behandeld met pioglitazon fracturen in vergelijking met 23 / 905 (2,5%; 0,5 fracturen per 100 patiëntjaren) vrouwelijke patiënten behandeld met comparator. Er was geen toename in de incidentie van fracturen bij mannen behandeld met pioglitazon (1,7%) in vergelijking met mannen behandeld met comparator (2,1%).
Sommige epidemiologische studies hebben een vergelijkbaar verhoogd risico op fracturen gesuggereerd bij zowel mannen als vrouwen.
Bij patiënten die met pioglitazon worden behandeld, moet bij langdurige therapie rekening worden gehouden met het risico op fracturen.
Als gevolg van de verhoogde werking van insuline kan behandeling met pioglitazon bij patiënten met polycysteus ovariumsyndroom ervoor zorgen dat de eisprong wordt hervat. Deze patiënten lopen mogelijk risico op zwangerschap. Patiënten moeten zich bewust zijn van het risico op zwangerschap en als de patiënte zwanger wil worden of als er zwangerschap optreedt, moet de behandeling worden stopgezet (zie rubriek 4.6).
Pioglitazon dient met voorzichtigheid te worden gebruikt bij gelijktijdige toediening van remmers (bijv. gemfibrozil) of inductoren (bijv. rifampicine) van cytochroom P450 2C8. De glycemische controle moet nauwlettend worden gevolgd.Aanpassing van de dosis pioglitazon binnen de aanbevolen dosering of veranderingen in de diabetesbehandeling moeten worden overwogen (zie rubriek 4.5).
Actos-tabletten bevatten lactosemonohydraat en mogen daarom niet worden toegediend aan patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, Lapp-lactasedeficiëntie of glucose-galactosemalabsorptie.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Interactiestudies hebben aangetoond dat pioglitazon geen relevant effect heeft op de farmacokinetiek of de farmacodynamiek van digoxine, warfarine, fenprocoumon en metformine. Gelijktijdige toediening van pioglitazon met sulfonylureumderivaten lijkt de farmacokinetiek van het sulfonylureumderivaat niet te beïnvloeden. Studies bij mensen suggereren dat er geen inductie is van het belangrijkste induceerbare cytochroom P450, 1A, 2C8/9 en 3A4. in vitro vertoonden geen remming van enig cytochroom P450-subtype. Er worden geen interacties verwacht met geneesmiddelen die door deze enzymen worden gemetaboliseerd, bijv. orale anticonceptiva, ciclosporine, calciumkanaalblokkers en HMGCoA-reductaseremmers.
Gelijktijdige toediening van pioglitazon met gemfibrozil (een cytochroom P450 2C8-remmer) resulteerde in een drievoudige verhoging van de AUC van pioglitazon Aangezien een verhoging van dosisgerelateerde bijwerkingen mogelijk is, kan het nodig zijn de dosis pioglitazon te verlagen wanneer gemfibrozil wordt gelijktijdig toegediend.Nauwkeurige controle van de glykemische controle dient te worden overwogen (zie rubriek 4.4) Gelijktijdige toediening van pioglitazon met rifampicine (een cytochroom P450 2C8-inductor) resulteerde in een afname van de pioglitazon-AUC met 54%. De dosis pioglitazon moet mogelijk worden verhoogd wanneer rifampicine gelijktijdig wordt toegediend. Nauwgezette controle van de glykemische controle moet worden overwogen (zie rubriek 4.4).
04.6 Zwangerschap en borstvoeding
Zwangerschap
Er zijn geen adequate gegevens bij mensen om de veiligheid van pioglitazon tijdens de zwangerschap te bepalen. Dierstudies met pioglitazon hebben een vertraagde ontwikkeling van de foetus aangetoond. Deze waarneming is toegeschreven aan de werking van pioglitazon bij het verminderen van maternale hyperinsulinemie en aan de verhoogde insulineresistentie die optreedt tijdens de zwangerschap, waardoor de beschikbaarheid van metabole substraten voor de groei van de foetus wordt verminderd.
Voedertijd
Pioglitazon werd gevonden in de melk van zogende ratten. Het is niet bekend of pioglitazon overgaat in de moedermelk. Daarom mag pioglitazon niet worden gegeven aan vrouwen die borstvoeding geven.
Vruchtbaarheid
In vruchtbaarheidsonderzoeken bij dieren werden geen effecten op copulatie, bevruchting of vruchtbaarheidsindex waargenomen.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Actos heeft geen of een verwaarloosbaar effect op de rijvaardigheid of het vermogen om machines te bedienen. Patiënten met visuele stoornissen moeten echter voorzichtig zijn bij het autorijden of het bedienen van machines
04.8 Bijwerkingen
Bijwerkingen die in grotere mate (> 0,5%) zijn gemeld dan bij placebo en in meer dan één geïsoleerd geval bij patiënten die pioglitazon kregen in dubbelblinde onderzoeken, worden hieronder in MedDRA-terminologie opgesomd per systeem/orgaanklasse en absolute frequentie. Frequenties zijn gedefinieerd als: zeer vaak (≥ 1/10), vaak (≥ 1/100,
1 Overgevoeligheidsreacties zijn gemeld bij patiënten die na het in de handel brengen met pioglitazon werden behandeld, waaronder anafylaxie, angio-oedeem en urticaria.
2 Visuele stoornissen zijn voornamelijk gemeld aan het begin van de behandeling en houden verband met veranderingen in de bloedglucose als gevolg van een tijdelijke verandering in turgiditeit en brekingsindex van de lens, zoals waargenomen bij andere bloedglucoseverlagende middelen.
3 Oedeem werd gemeld bij 6-9% van de patiënten die gedurende één jaar met pioglitazon werden behandeld in gecontroleerde klinische onderzoeken. Het percentage oedeem in de vergelijkingsgroepen (sulfonylureumderivaat, metformine) was 2-5%. Gevallen van oedeem waren over het algemeen licht tot matig en er was gewoonlijk geen stopzetting van de behandeling nodig.
4 In gecontroleerde klinische onderzoeken was de incidentie van hartfalen gemeld bij behandeling met pioglitazon dezelfde als in de placebo-, metformine- en sulfonylureumderivaatgroepen, maar was verhoogd wanneer pioglitazon werd gebruikt in combinatietherapie met insuline. bestaande ernstige macrovasculaire ziekte, was de incidentie van ernstig hartfalen 1,6% hoger met pioglitazon dan met placebo indien toegevoegd aan een behandeling met insuline. Dit resulteerde echter niet in een toename van de mortaliteit in deze studie. In deze studie, bij patiënten die pioglitazon en insuline kregen, werd een hoger percentage patiënten met hartfalen waargenomen bij patiënten ≥ 65 jaar, vergeleken met patiënten jonger dan 65 jaar (9 (7% versus 4,0%). Bij patiënten die insulinetherapie zonder pioglitazon kregen, was de incidentie van hartfalen was 8 , 2% bij patiënten ≥ 65 jaar, vergeleken met 4,0% bij patiënten jonger dan 65 jaar. Hartfalen is gemeld tijdens het op de markt brengen van pioglitazon, en vaker wanneer pioglitazon werd gebruikt in combinatie met insuline of bij patiënten met een voorgeschiedenis van hartfalen.
5 Een "cumulatieve analyse van bijwerkingen van botfracturen gemeld uit gerandomiseerde, comparator-gecontroleerde, dubbelblinde klinische onderzoeken werd uitgevoerd bij meer dan 8.100 patiënten behandeld met pioglitazon en 7.400 behandeld met comparator gedurende een periode van meer dan 3,5 een hogere incidentie van fracturen werd waargenomen bij vrouwen die werden behandeld met pioglitazon (2,6%) dan bij vrouwen die werden behandeld met een comparator (1,7%). Er was geen toename in de incidentie van fracturen bij mannen die werden behandeld met pioglitazon (1,3%) in vergelijking met mannen die werden behandeld met een comparator (1,5%).
In het 3,5 jaar durende PROactive-onderzoek kregen 44/870 (5,1%) vrouwelijke patiënten die met pioglitazon werden behandeld, fracturen in vergelijking met 23/905 (2,5%) vrouwelijke patiënten die werden behandeld met een vergelijkend geneesmiddel. Er was geen toename in de incidentie van fracturen bij mannen behandeld met pioglitazon (1,7%) in vergelijking met mannen behandeld met comparator (2,1%).
6 In actief-gecontroleerde onderzoeken was de gemiddelde gewichtstoename met pioglitazon gegeven als monotherapie 2 tot 3 kg gedurende één jaar Dit resultaat was vergelijkbaar met het resultaat dat werd gezien in de sulfonylureumvergelijkingsgroep De gemiddelde gewichtstoename was 1,5 kg in onderzoeken waarbij pioglitazon werd gecombineerd met metformine en 2,8 kg in onderzoeken waarin pioglitazon langer dan een jaar werd gecombineerd met sulfonylureumderivaat. In de vergelijkingsgroepen resulteerde de toevoeging van sulfonylureumderivaat aan metformine in een gemiddelde gewichtstoename van 1,3 kg en de toevoeging van metformine aan het sulfonylureumderivaat resulteerde in een gemiddeld gewichtsverlies van 1,0 kg.
7 In klinische onderzoeken met pioglitazon was de incidentie van ALT-verhogingen van 3 maal de bovengrens van normaal gelijk aan die van placebo, maar lager dan die waargenomen in de metformine- of sulfonylureumcomparatorgroepen De gemiddelde leverenzymspiegels zijn verlaagd bij behandeling met pioglitazon Zeldzame gevallen van Verhogingen van leverenzymen en hepatocellulaire disfunctie zijn opgetreden tijdens postmarketingervaring. Hoewel in zeer zeldzame gevallen fatale voorvallen zijn gemeld, is het oorzakelijk verband niet vastgesteld.
04.9 Overdosering
In klinische onderzoeken namen patiënten pioglitazon in een hogere dosis dan de maximaal aanbevolen dosis van 45 mg per dag. De maximaal gerapporteerde dosis van 120 mg/dag gedurende vier dagen en vervolgens 180 mg/dag gedurende zeven dagen ging niet gepaard met symptomen.
Hypoglykemie kan optreden in combinatie met sulfonylureumderivaten of insuline. In het geval van een overdosis moeten symptomatische en algemene ondersteunende maatregelen worden genomen.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: geneesmiddelen gebruikt bij diabetes, geneesmiddelen die de bloedglucose verlagen, met uitzondering van insulines; ATC-code: A10BG03.
De effecten van pioglitazon kunnen worden gemedieerd door een verlaging van de insulineresistentie Pioglitazon lijkt te werken door specifieke receptoren in de kern te activeren (geactiveerde gamma-receptor voor peroxisoomproliferatie), wat leidt tot een toename van de insulinegevoeligheid van de lever, het vet en de skeletspiercellen. bij dieren. Het is aangetoond dat behandeling met pioglitazon de glucoseproductie in de lever vermindert en de beschikbaarheid van perifere glucose verhoogt in geval van insulineresistentie.
Nuchtere en postprandiale glykemische controle is verbeterd bij patiënten met diabetes mellitus type 2. Deze verbeterde glykemische controle gaat gepaard met een verlaging van zowel nuchtere als postprandiale plasma-insulineconcentraties.Een klinische studie uitgevoerd met pioglitazon vs monotherapie met gliclazide werd verlengd tot twee jaar om de tijd tot falen van de behandeling te beoordelen (gedefinieerd als HbA1c ≥ 8,0% na de eerste zes maanden van de behandeling). Kaplan-Meier-analyse toonde een kortere tijd tot falen van de behandeling aan bij patiënten die met gliclazide werden behandeld dan bij patiënten die met pioglitazon werden behandeld.Na twee jaar was glykemische controle (gedefinieerd als HbA1c
In een placebogecontroleerd onderzoek werden patiënten met onvoldoende glykemische controle ondanks een periode van 3 maanden van geoptimaliseerde insulinetherapie gerandomiseerd naar pioglitazon of placebo gedurende 12 maanden. Patiënten die met pioglitazon werden behandeld, hadden een gemiddelde verlaging van HbA1c van 0,45% in vergelijking met degenen die alleen insuline bleven gebruiken, en een verlaging van de insulinedosis in de pioglitazongroep.
De HOMA-analyse laat zien dat pioglitazon de bètacelfunctie verbetert en de gevoeligheid voor insuline verhoogt. Klinische studies van twee jaar hebben aangetoond dat dit effect behouden blijft.
In klinische onderzoeken van één jaar veroorzaakte pioglitazon consequent een statistisch significante verlaging van de albumine/creatinine-verhouding vanaf baseline.
Het effect van pioglitazon (monotherapie 45 mg vs placebo) werd geëvalueerd in een kleine 18 weken durende studie bij patiënten met diabetes type 2. Pioglitazon ging gepaard met significante gewichtstoename. Het visceraal vet was significant afgenomen, terwijl de extra-abdominale vetmassa toenam.Deze veranderingen in de lichaamsvetverdeling met pioglitazon gingen gepaard met een toename van de insulinegevoeligheid. In de meeste klinische onderzoeken werden in vergelijking met placebo verlagingen van de totale plasmatriglyceriden en vrije vetzuren en verhogingen van de HDL-cholesterolwaarden waargenomen, met kleine maar niet klinisch significante verhogingen van de LDL-cholesterolwaarden.
In klinische onderzoeken die tot twee jaar duurden, verlaagde pioglitazon de totale plasmatriglyceriden en vrije vetzuren en verhoogde het HDL-cholesterolgehalte in vergelijking met placebo, metformine en gliclazide. Pioglitazon veroorzaakte geen statistisch significante verhogingen van het LDL-cholesterolgehalte in vergelijking met placebo, terwijl verlagingen werden waargenomen met metformine en gliclazide. In een 20 weken durend onderzoek verminderde pioglitazon niet alleen de nuchtere triglyceriden, maar ook postprandiale hypertriglyceridemie met een effect op zowel geabsorbeerde als hepatisch gesynthetiseerde triglyceriden.Deze effecten waren onafhankelijk van de effecten van pioglitazon op de bloedglucose en zijn statistisch significant verschillend van toestanden dan glibenclamide.
In PROactive, een cardiovasculaire uitkomststudie, werden 5238 patiënten met type 2 diabetes mellitus en reeds bestaande ernstige macrovasculaire ziekte gerandomiseerd naar pioglitazon of placebo naast lopende antidiabetica en cardiovasculaire therapie gedurende maximaal 3,5 jaar. De onderzoekspopulatie had een gemiddelde leeftijd van 62 jaar; de gemiddelde duur van diabetes was 9,5 jaar. Ongeveer een derde van de patiënten gebruikte insuline in combinatie met metformine en/of een sulfonylureumderivaat. Om in aanmerking te komen, moesten patiënten een of meer van de volgende aandoeningen: myocardinfarct, beroerte, percutane hartoperatie of coronaire bypass-transplantaat, acuut coronair syndroom, coronaire hartziekte of perifere obstructieve arteriële ziekte Bijna de helft van de patiënten had een eerder myocardinfarct gehad en ongeveer 20% had een Ongeveer de helft van de onderzoekspopulatie had ten minste twee van de inclusiecriteria voor cardiovasculaire voorgeschiedenis. Bijna alle proefpersonen (95%) gebruikten cardiovasculaire geneesmiddelen (bètablokkers, ACE-remmers, angiotensine II-antagonisten, calciumkanaalblokkers, nitraten, diuretica, aspirine, statines, fibraten).
Hoewel de studie niet voldeed aan het primaire eindpunt, dat een samengesteld eindpunt was van mortaliteit door alle oorzaken, niet-fataal myocardinfarct, beroerte, acuut coronair syndroom, ernstige beenamputatie, coronaire en beenrevascularisatie, suggereren de resultaten dat er geen langdurige cardiovasculaire problemen bij het gebruik van pioglitazon. De incidentie van oedeem, gewichtstoename en hartfalen nam echter toe. Er werd geen toename van de mortaliteit door hartfalen waargenomen.
Pediatrische populatie
Het Europees Geneesmiddelenbureau heeft de vergunninghouder ontheven van de verplichting om de resultaten in te dienen van onderzoek met Actos in alle subgroepen van pediatrische patiënten met diabetes mellitus type 2. Zie rubriek 4.2 voor informatie over pediatrisch gebruik.
05.2 Farmacokinetische eigenschappen
Absorptie
Na orale toediening wordt pioglitazon snel geabsorbeerd en piekplasmaconcentraties van onveranderd pioglitazon worden over het algemeen 2 uur na de dosis bereikt. Proportionele verhogingen van de plasmaconcentratie werden waargenomen voor doses variërend van 2 tot 60 mg. Steady state wordt bereikt na 4-7 dagen toediening. Herhaalde dosering resulteert niet in accumulatie van het geneesmiddel of metabolieten. Absorptie wordt niet beïnvloed door voedselinname. De absolute biologische beschikbaarheid is groter dan 80%.
Verdeling
Het geschatte distributievolume bij de mens is 0,25 l/kg.
Pioglitazon en alle actieve metabolieten zijn in hoge mate gebonden aan plasma-eiwitten (> 99%).
Biotransformatie
Pioglitazon wordt uitgebreid gemetaboliseerd door de lever door hydroxylering van alifatische methyleengroepen. Dit gebeurt voornamelijk via cytochroom P450 2C8, hoewel andere isovormen in mindere mate betrokken kunnen zijn. Drie van de zes geïdentificeerde metabolieten zijn actief (M-II, M-III en M-IV). Wanneer activiteit, concentraties en eiwitbinding in aanmerking worden genomen, dragen pioglitazon en de metaboliet M-III in gelijke mate bij aan de werkzaamheid. Op basis hiervan is de bijdrage van M-IV aan de werkzaamheid ongeveer driemaal die van pioglitazon, terwijl de relatieve werkzaamheid van M-II minimaal is.
Opleiding in vitro toonde niet aan dat pioglitazon enig subtype van cytochroom P450 remt. Er is geen inductie van de belangrijkste induceerbare iso-enzymen van P450 bij mensen, 1A, 2C8/9 en 3A4.
Interactiestudies hebben aangetoond dat pioglitazon geen relevant effect heeft op de farmacokinetiek of de farmacodynamiek van digoxine, warfarine, fenprocoumon en metformine. Gelijktijdige toediening van pioglitazon met gemfibrozil (een cytochroom P450 2C8-remmer) of rifampicine (een cytochroom P450 2C8-inductor) veroorzaakte respectievelijk een verhoging of verlaging van de plasmaconcentraties van pioglitazon (zie rubriek 4.5).
Eliminatie
Na orale toediening van radioactief gelabeld pioglitazon bij mensen werd het grootste deel van de gelabelde stof teruggevonden in de feces (55%) en een kleine hoeveelheid in de urine (45%). Bij dieren kan slechts een kleine hoeveelheid onveranderd pioglitazon worden gedetecteerd. in urine of feces De gemiddelde plasma-eliminatiehalfwaardetijd bij de mens is 5-6 uur voor onveranderd pioglitazon en 16-23 uur voor zijn totale actieve metabolieten.
Bejaarden
De steady-state farmacokinetiek is vergelijkbaar bij patiënten van 65 jaar of ouder en bij jonge proefpersonen.
Patiënten met nierinsufficiëntie
Bij patiënten met nierinsufficiëntie zijn de plasmaconcentraties van pioglitazon en zijn metabolieten lager dan die waargenomen bij proefpersonen met een normale nierfunctie, maar met een vergelijkbare orale klaring voor het oorspronkelijke geneesmiddel. De concentratie van vrij (ongebonden) pioglitazon blijft dus ongewijzigd.
Patiënten met leverinsufficiëntie
De totale plasmaconcentratie van pioglitazon is onveranderd maar met een verhoogd distributievolume. Bijgevolg is de intrinsieke klaring verminderd, wat gepaard gaat met een hogere fractie ongebonden pioglitazon.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
In toxicologische onderzoeken trad een toename van het plasmavolume met hemodilutie, anemie en reversibele excentrische cardiale hypertrofie consequent op na herhaalde toediening bij muizen, ratten, honden en apen. Bovendien werd een verhoogde vetafzetting en infiltratie waargenomen. Deze resultaten werden waargenomen bij alle soorten bij plasmaconcentraties ≤ 4 keer de klinische blootstelling. Verminderde foetale groei trad op in dierstudies met pioglitazon. Dit is toe te schrijven aan de werking van pioglitazon bij het verminderen van maternale hyperinsulinemie en aan de verhoogde insulineresistentie die optreedt tijdens de zwangerschap, waardoor de beschikbaarheid van metabole substraten voor foetale groei wordt verminderd.
Pioglitazon had geen genotoxisch potentieel in een uitgebreide reeks uitgevoerde genotoxiciteitstesten in vivo en in vitro. Een verhoogde incidentie van hyperplasie (mannetjes en vrouwtjes) en tumoren (mannetjes) van het urineblaasepitheel werd waargenomen bij ratten die tot 2 jaar met pioglitazon werden behandeld.
De hypothese is dat de vorming en aanwezigheid van urinestenen met daaropvolgende irritatie en hyperplasie de mechanistische basis is van de tumorverwekkende respons die wordt waargenomen bij de mannelijke rat.
Een mechanistische studie van 24 maanden bij mannelijke ratten toonde aan dat toediening van pioglitazon resulteerde in een verhoogde incidentie van hyperplastische veranderingen in de blaas Voedingsverzuring verminderde de incidentie van tumoren significant, maar deed deze niet verdwijnen. aanwezigheid van microkristallen verergerde de hyperplastische respons, maar werd niet beschouwd als de belangrijkste oorzaak van hyperplastische veranderingen De relevantie voor de mens van de tumorverwekkende effecten die zijn waargenomen bij de mannelijke rat kan niet worden uitgesloten.
Er was geen tumorverwekkende respons bij beide geslachten van muizen. Blaashyperplasie werd niet waargenomen bij honden of apen die tot 12 maanden met pioglitazon werden behandeld.
In een diermodel van familiaire adenomateuze polyposis (FAP) verhoogde behandeling met twee andere thiazolidinedionen de multipliciteit van darmkanker. De relevantie van deze bevinding is niet bekend.
Milieurisicobeoordeling: Klinisch gebruik van pioglitazon heeft naar verwachting geen impact op het milieu.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Calcium Carmellose
Hypolose
Lactosemonohydraat
Magnesium stearaat.
06.2 Incompatibiliteit
Niet toepasbaar.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Voor dit geneesmiddel zijn er geen speciale bewaarcondities.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Aluminium/aluminium blisterverpakkingen in verpakkingen van 14, 28, 30, 50, 56, 84, 90, 98, 112 en 196 tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Takeda Pharma A / S
Langebjerg 1
DK-4000 Roskilde
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU / 1/00/150/001
034946018
EU / 1/00/150/002
034946020
EU / 1/00/150/003
034946032
EU / 1/00/150/007
034946071
EU / 1/00/150/009
034946095
EU / 1/00/150/016
034946160
EU / 1/00/150/017
034946172
EU / 1/00/150/018
034946184
EU / 1/00/150/025
EU / 1/00/150/026
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste autorisatie: 13/10/2000
Datum van laatste verlenging: 31/08/2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
D.CCE november 2013