Actieve ingrediënten: Gabesaatmesylaat
FOY 100 mg poeder en oplosmiddel voor oplossing voor infusie
Indicaties Waarom wordt Foy gebruikt? Waar is het voor?
FARMACOTHERAPEUTISCHE CATEGORIE
Gabesatemesilaat behoort tot de categorie van SERPIN, dat wil zeggen serineproteaseremmers, stoffen die in verschillende delen van het lichaam worden geproduceerd.Het is een synthetisch geneesmiddel (niet-eiwitachtig) met een laag moleculair gewicht, met een sterk remmend effect tegen kallikreïne, trypsine, evenals een krachtige ontspannende werking op de sluitspier van Oddi.
Vanwege deze eigenschappen heeft het product een positief effect bij het oplossen van de symptomen en het corrigeren van de pathogenetische mechanismen van acute pancreatitis geassocieerd met de overdreven of ongecontroleerde afgifte van proteolytische enzymen.
THERAPEUTISCHE INDICATIES
Acute ontsteking aan de alvleesklier.
Contra-indicaties Wanneer Foy niet mag worden gebruikt
Overgevoeligheid voor gabesaatmesylaat
Voorzorgen bij gebruik Wat u moet weten voordat u Foy inneemt
Het product kan een antistollingswerking hebben.
In sommige onderzoeken bij honden met hoge doses werd een vermindering van de partiële tromboplastinetijd waargenomen.
Deze gebeurtenis is tot nu toe niet waargenomen tijdens Foy-therapie bij mensen.
Toediening van dit product in hoge doses kan necrotische ulcera veroorzaken op de injectieplaats en langs de bloedvaten waar het de vaatwand kan beschadigen en flebitis en verstijving van het vat zelf kan veroorzaken.
Patiënten moeten zorgvuldig worden gecontroleerd.
Als zich pijn, roodheid of ontsteking op de injectieplaats voordoet, moet de behandeling worden stopgezet of moet de injectieplaats worden gewijzigd en moeten passende maatregelen worden genomen.
Tijdens de toediening moet de patiënt constant worden gecontroleerd.
Shock, anafylactische shock, anafylactoïde reacties kunnen optreden.
In het geval van bloeddrukdaling, precordiale benauwdheid, dyspneu, bewustzijnsverlies, farynx-/larynxoedeem, jeuk of malaise, moet de behandeling onmiddellijk worden stopgezet en moeten passende maatregelen worden genomen.
Patiënten moeten ook nauwlettend worden gecontroleerd op het mogelijke optreden van: agranulocytose, leukopenie, trombocytopenie en hyperkaliëmie.
Als er abnormale waarden worden gevonden, moet de behandeling worden stopgezet en in het geval van hyperkaliëmie moeten passende maatregelen worden genomen.
Als: hoofdpijn, verminderde partiële tromboplastinetijd, bloedingsneiging, hypotensie, misselijkheid, braken, diarree, huiduitslag, jeuk of gezichtscongestie optreden, moet de dosering worden verlaagd. Bij aanhoudende behandeling de behandeling definitief stopzetten.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Foy . veranderen?
Er zijn geen interacties tussen geneesmiddelen bekend.
Vertel het uw arts of apotheker als u kort geleden andere geneesmiddelen heeft gebruikt, ook zonder voorschrift.
Waarschuwingen Het is belangrijk om te weten dat:
Gebruik bij zwangerschap of borstvoeding
. In het geval van een vastgestelde of veronderstelde zwangerschap, is het raadzaam om de dosering van Foy op de minimaal effectieve niveaus te houden en alleen voor indicaties die levensbedreigend zijn voor de zwangere vrouw.
Anderzijds zijn er geen gegevens beschikbaar over de mogelijke uitscheiding in de moedermelk.
Dosering en wijze van gebruik Hoe te gebruiken Foy: Dosering
Start de behandeling met 1-3 injectieflacons per dag (100-300 mg gabesaatmesylaat) via intraveneuze druppelinfusie met een snelheid van niet meer dan 8 ml / minuut en verlaag vervolgens de dosering in functie van de verbetering van het klinische beeld. Indien nodig is het mogelijk om de hierboven aangegeven dosering op dezelfde dag met 1-3 injectieflacons te verhogen.
Breng het speciale oplosmiddel aan in de injectieflacon met Foy-poeder.De aldus verkregen oplossing moet verder worden verdund in 500 ml Ringer-oplossing of 5% glucose.
De aldus bereide oplossing moet onmiddellijk worden gebruikt of worden bewaard in de koelkast (bij 3 ° C), waar het ongeveer 5 dagen stabiel blijft.
Het is raadzaam om de oplossing i.v. langzaam, waarbij de snelheid wordt aangepast om 2,5 mg gabesaatmesylaat per kg lichaamsgewicht en per uur niet te overschrijden.
In geval van gelijktijdige therapie met andere parenterale geneesmiddelen, moet gabesaatmesylaat afzonderlijk worden toegediend.
De dosering moet op passende wijze worden aangepast aan de symptomen van de patiënt.
Gebruik bij ouderen: Na een vermindering van fysiologische functies worden bij ouderen constante controle en voorzorgsmaatregelen zoals dosisverlaging aanbevolen.
Overdosering Wat te doen als u te veel Foy heeft ingenomen
Er zijn geen symptomen van overdosering bekend.
Bijwerkingen Wat zijn de bijwerkingen van Foy
Uit een klinische studie, uitgevoerd bij ongeveer 4000 patiënten die met Foy werden behandeld, kwamen verschillende bijwerkingen naar voren; de belangrijkste worden weergegeven in de onderstaande tabel, onderverdeeld naar systeem en frequentie:
Naleving van de instructies in de bijsluiter verkleint de kans op bijwerkingen.
Het is belangrijk om de arts of apotheker op de hoogte te stellen van elke bijwerking, ook als deze niet in de bijsluiter staat beschreven.
Vervaldatum en retentie
Vervaldatum: zie de vervaldatum die op de verpakking staat vermeld.
De aangegeven houdbaarheidsdatum verwijst naar het product in intacte verpakking, correct bewaard.
WAARSCHUWING: gebruik het geneesmiddel niet meer na de vervaldatum die staat vermeld op de verpakking.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Houd dit geneesmiddel buiten het bereik en zicht van kinderen.
SAMENSTELLING
Eén injectieflacon met poeder bevat: Werkzaam bestanddeel: Gabesatemesylaat 100 mg. Eén ampul oplosmiddel bevat: Water voor injecties.
FARMACEUTISCHE VORM EN INHOUD
Poeder en oplosmiddel voor oplossing voor infusie. "100 mg poeder en oplosmiddel voor oplossing voor infusie" 1 injectieflacon + 1 ampul met oplosmiddel 5 ml
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
FOY 100 MG POEDER EN OPLOSMIDDEL VOOR OPLOSSING VOOR INFUSIE
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Eén injectieflacon met poeder bevat 100 mg gabesaatmesylaat
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Poeder en oplosmiddel voor oplossing voor infusie
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Acute ontsteking aan de alvleesklier.
04.2 Dosering en wijze van toediening
Start de behandeling met 1-3 injectieflacons per dag (100-300 mg gabesaatmesylaat) via intraveneuze druppelinfusie met een snelheid van niet meer dan 8 ml / minuut en verlaag vervolgens de dosering in functie van de verbetering van het klinische beeld. Indien nodig is het mogelijk om de hierboven aangegeven dosering op dezelfde dag met 1-3 injectieflacons te verhogen.
Breng het speciale oplosmiddel aan in de injectieflacon met Foy-poeder.De aldus verkregen oplossing moet verder worden verdund in 500 ml Ringer-oplossing of 5% glucose.
De aldus bereide oplossing moet onmiddellijk worden gebruikt of worden bewaard in de koelkast (bij 3 ° C), waar het ongeveer 5 dagen stabiel blijft.
Het is raadzaam om de oplossing i.v. langzaam, waarbij de snelheid wordt aangepast om 2,5 mg gabesaatmesylaat per kg lichaamsgewicht en per uur niet te overschrijden.
De dosering moet op passende wijze worden aangepast aan de symptomen van de patiënt.
Gebruik bij ouderen:
Na een vermindering van fysiologische functies worden bij ouderen constante controle en voorzorgsmaatregelen zoals dosisverlaging aanbevolen.
04.3 Contra-indicaties
Overgevoeligheid voor gabesaatmesylaat.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Het product kan een antistollingswerking hebben.
In sommige onderzoeken bij honden met hoge doses werd een vermindering van de partiële tromboplastinetijd waargenomen.
Deze gebeurtenis is tot nu toe niet waargenomen tijdens Foy-therapie bij mensen.
Tijdens de toediening van het product (zie ook par. 4.2) is het raadzaam de infusiesnelheid aan te passen zodat deze niet hoger is dan 2,5 mg/kg per uur. In geval van gelijktijdige therapie met andere parenterale geneesmiddelen, is het noodzakelijk gabesaatmesylaat afzonderlijk toe te dienen.
Toediening van dit product in hoge doses kan necrotische ulcera veroorzaken op de injectieplaats en langs de bloedvaten waar het de vaatwand kan beschadigen en flebitis en verstijving van het vat zelf kan veroorzaken.
Patiënten moeten zorgvuldig worden gecontroleerd.
Als zich pijn, roodheid of ontsteking op de injectieplaats voordoet, moet de behandeling worden stopgezet of moet de injectieplaats worden gewijzigd en moeten passende maatregelen worden genomen.
Tijdens de toediening moet de patiënt constant worden gecontroleerd. Shock, anafylactische shock, anafylactoïde reacties kunnen optreden.
In het geval van bloeddrukdaling, precordiale benauwdheid, dyspneu, bewustzijnsverlies, farynx-/larynxoedeem, jeuk of malaise, moet de behandeling onmiddellijk worden stopgezet en moeten passende maatregelen worden genomen.
Patiënten moeten ook nauwlettend worden gecontroleerd op het mogelijke optreden van: agranulocytose, leukopenie, trombocytopenie en hyperkaliëmie.
Als er abnormale waarden worden gevonden, moet de behandeling worden stopgezet en in het geval van hyperkaliëmie moeten passende maatregelen worden genomen.
Als: hoofdpijn, verminderde partiële tromboplastinetijd, bloedingsneiging, hypotensie, misselijkheid, braken, diarree, huiduitslag, jeuk of gezichtscongestie optreden, moet de dosering worden verlaagd. Bij aanhoudende behandeling de behandeling definitief stopzetten.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Niet bekend.
04.6 Zwangerschap en borstvoeding
Zwangerschap
Tijdens een vastgestelde of veronderstelde zwangerschap is het raadzaam om de dosering van Foy op de minimaal effectieve niveaus te houden (een gewichtsverlies van de foetussen werd waargenomen bij muizen met doses van 100 mg / kg / dag) en alleen voor indicaties die levens- de zwangere vrouw bedreigen.
Voedertijd
Er zijn geen gegevens over mogelijke uitscheiding in de moedermelk.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Niet relevant omdat Foy alleen in een ziekenhuisomgeving wordt gegeven.
04.8 Bijwerkingen
Uit een klinische studie, uitgevoerd bij ongeveer 4000 patiënten die met Foy werden behandeld, kwamen verschillende bijwerkingen naar voren; de belangrijkste worden weergegeven in de onderstaande tabel, onderverdeeld naar systeem en frequentie:
Melding van vermoedelijke bijwerkingen.
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue monitoring van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
Er zijn geen symptomen van overdosering bekend.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: antihemorragica, antifibrinolytica, proteaseremmers
- ATC-code: B02AB
Van gabesaatmesylaat (GM) is aangetoond dat het bijzonder actief is als een remmer van trypsine, fosfolipase A, plasmine, kallikreïne en trombine (zelfs in de afwezigheid van AT III), wat gunstig interfereert met pancreashyperproteasemie, fibrinolyse, coagulatie en kinine. antibloedplaatjeseigenschappen, oefent een beschermend effect uit op experimenteel geïnduceerde acute pancreatitis bij ratten en konijnen, een remmend effect op geïnduceerde DIC bij konijnen, ratten en honden, een beschermend effect bij verschillende soorten shock. Bovendien kon bij de hond een duidelijke losmakende werking van de sluitspier van Oddi worden aangetoond.
05.2 "Farmacokinetische eigenschappen
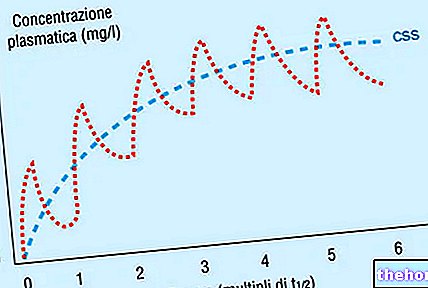
De halfwaardetijd van GM is ongeveer 60 seconden IV toegediend aan gezonde mannelijke proefpersonen met een snelheid van 2 mg / kg / uur bereikt het de maximale concentratie in 5-10 minuten vanaf het begin van de toediening met een bloedspiegel van principe niet-gemetaboliseerd actief gelijk aan 109 ng/ml. Bij een dosis van 4 mg/kg/u is de bloedspiegel van het niet-gemetaboliseerde product gelijk aan 265 ng/ml.
Na intraveneuze toediening wordt het snel gemetaboliseerd tot guanidinocapronzuur en parabenzoaat (beide inactief). Eliminatie vindt plaats gedurende 24 uur, voornamelijk in de urine, met minimale uitscheiding via de gal.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Acute toxiciteitsstudies hebben LD50-waarden (mg/kg) aangetoond variërend van 8000 tot 260 mg/kg en van 7770 tot 81 mg/kg bij respectievelijk muizen en ratten, indien oraal of intraveneus toegediend.
GM wordt bevredigend getolereerd voor herhaalde toediening bij verschillende diersoorten.
Bij ratten vertoonde de dosis van 40 mg / 5 ml / kg mortaliteit in de verhouding 4/10 / geslacht, stijfheid van de ledematen, remming van de ademhaling, vermindering van hemoglobine, hematocriet en protrombinetijd. Bij konijnen had een behandeling van 6 maanden met doses van 10, 20, 40, 80 en 160 mg / kg / dag intraveneus toegediend geen effect, behalve een lichte lokale irritatie op de inentingsplaatsen. Bij honden resulteerde een behandeling met 40 mg/kg/dag gedurende 14 dagen in een significante vermindering van de partiële tromboplastinetijd, een verhoogd levergewicht met milde waterzuchtdegeneratie. De dosis van 640 mg/kg/dag veroorzaakte ook een afname van hematocriet en bloedplaatjes en een toename van alkalische fosfatase en alanineaminotransferase.
Uit foetale toxiciteitsgegevens bleek dat de niet-toxische doses bij moeders en het product van conceptie respectievelijk 50 mg/kg, 20 mg/kg en 10 mg/kg waren bij muizen, ratten en konijnen. Het product heeft geen effecten op de vruchtbaarheid en het voortplantingsvermogen bij maximale doses tussen 12 en 36 mg/kg.
Bovendien heeft de verbinding geen mutagene effecten, zoals blijkt uit onderzoeken die zijn uitgevoerd op verschillende genetische systemen.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Ampul met oplosmiddel: water voor injecties
06.2 Incompatibiliteit
In geval van gelijktijdige therapie met andere parenterale geneesmiddelen, is het noodzakelijk gabesaatmesylaat afzonderlijk toe te dienen.
06.3 Geldigheidsduur
3 jaar.
De gereconstitueerde oplossing, bereid door toevoeging van de inhoud van de overeenkomstige injectieflacon met oplosmiddel aan een injectieflacon, is 24 uur houdbaar bij kamertemperatuur en 5 dagen in de koelkast (3 ° C).
06.4 Speciale voorzorgsmaatregelen bij bewaren
Geen
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Injectieflacon met poeder
Type I, kleurloze, neutrale glazen injectieflacon met butylrubberen stop en "Flip-off" type aluminium/plastic dop.
flacon met oplosmiddel
Type I neutrale glazen injectieflacon, kleurloos.
"100 mg poeder en oplosmiddel voor oplossing voor infusie" 1 injectieflacon + 1 ampul met oplosmiddel 5 ml
06.6 Instructies voor gebruik en verwerking
Zie paragraaf 4.2.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Sanofi S.p.A. - Viale L. Bodio, 37 / B - Milaan
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
A.I.C. N. 026829010 - "100 mg poeder en oplosmiddel voor oplossing voor infusie" 1 injectieflacon + 1 ampul oplosmiddel 5 ml
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste vergunning: 28.04.1993
Datum van de meest recente verlenging: 19.05.2008