Actieve ingrediënten: Irbesartan, Hydrochloorthiazide
Karvezide 300 mg / 12,5 mg tabletten
Karvezide bijsluiters zijn beschikbaar voor verpakkingsgrootten:- Karvezide 300 mg / 12,5 mg tabletten
- Karvezide 150 mg/12,5 mg filmomhulde tabletten
- Karvezide 300 mg / 25 mg filmomhulde tabletten
Waarom wordt Karvezide gebruikt? Waar is het voor?
Karvezide is een "combinatie van twee werkzame stoffen: irbesartan en hydrochloorthiazide.
Irbesartan behoort tot een groep geneesmiddelen die bekend staat als angiotensine-II-receptorantagonisten. Angiotensine-II is een stof die in het lichaam wordt aangemaakt en zich bindt aan zijn receptoren, die zich in de bloedvaten bevinden, waardoor ze vernauwen.Dit leidt tot een verhoging van de bloeddruk
. Irbesartan verhindert de binding van angiotensine-II aan deze receptoren, waardoor de bloedvaten ontspannen en de bloeddruk daalt Hydrochloorthiazide behoort tot een groep geneesmiddelen (zogenaamde thiazidediuretica) die een verhoogde urineproductie en bijgevolg een lagere bloeddruk veroorzaken. De twee actieve ingrediënten van Karvezide werken samen en veroorzaken een verlaging van de bloeddrukwaarden die groter is dan die veroorzaakt door de afzonderlijke geneesmiddelen die afzonderlijk worden toegediend.
Karvezide wordt gebruikt om hoge bloeddruk te behandelen wanneer behandeling met irbesartan of hydrochloorthiazide alleen uw bloeddruk niet voldoende onder controle heeft gebracht.
Contra-indicaties Wanneer Karvezide niet mag worden gebruikt
Neem Karvezide niet in
- als u allergisch bent voor irbesartan of voor één van de andere bestanddelen van dit geneesmiddel
- als u allergisch bent voor hydrochloorthiazide of voor een van de geneesmiddelen die zijn afgeleid van sulfonamide
- als u meer dan 3 maanden zwanger bent (het is ook beter om Karvezide in het begin van de zwangerschap te vermijden - zie rubriek Zwangerschap)
- als u ernstige lever- of nierproblemen heeft
- als u moeite heeft met urineren
- als uw arts vaststelt dat u een aanhoudend hoog calcium- of een laag kaliumgehalte in uw bloed heeft
- als u diabetes of een verminderde nierfunctie heeft en u wordt behandeld met een bloeddrukverlagend geneesmiddel dat aliskiren bevat
Voorzorgen bij gebruik Wat u moet weten voordat u Karvezide inneemt
Neem contact op met uw arts voordat u Karvezide inneemt en als u last heeft van een van de volgende aandoeningen:
- overmatig braken of diarree
- als u nierproblemen heeft of een niertransplantatie heeft ondergaan
- als u hartproblemen heeft
- als u lijdt aan leverproblemen
- als u suikerziekte heeft
- als u lijdt aan lupus erythematodes (ook bekend als lupus of SLE)
- als u lijdt aan primair aldosteronisme (een aandoening die verband houdt met een hoge productie van het hormoon aldosteron, dat natriumretentie veroorzaakt en vervolgens een verhoging van de bloeddruk)
- als u een van de volgende geneesmiddelen gebruikt om hoge bloeddruk te behandelen:
- een "ACE-remmer" (bijv. enalapril, lisinopril, ramipril), vooral als u diabetesgerelateerde nierproblemen heeft.
- aliskiren
Uw arts kan uw nierfunctie, bloeddruk en de hoeveelheid elektrolyten (zoals kalium) in uw bloed met regelmatige tussenpozen controleren.
Zie ook de informatie onder het kopje "Neem Karvezide niet in"
Vertel het uw arts als u denkt zwanger te zijn (of als er een kans bestaat om zwanger te worden). Karvezide wordt niet aanbevolen in het begin van de zwangerschap en mag niet worden ingenomen als u langer dan 3 maanden zwanger bent, omdat het ernstige schade toebrengen aan uw baby als het tijdens deze periode wordt ingenomen (zie rubriek over zwangerschap).
Vertel uw arts ook:
- als u een zoutarm dieet volgt
- als u symptomen heeft zoals overmatige dorst, droge mond, algemene zwakte, slaperigheid, spierpijn of spierkrampen, misselijkheid, braken of een te snelle hartslag die kan wijzen op een overmatig effect van hydrochloorthiazide (in Karvezide)
- als u sneller dan normaal een toename van de gevoeligheid van uw huid voor de zon heeft opgemerkt met symptomen van zonnebrand (zoals roodheid, jeuk, zwelling, huiduitslag)
- als u een operatie moet ondergaan of verdovingsmiddelen moet gebruiken als u veranderingen in het gezichtsvermogen of pijn in één of beide ogen ervaart terwijl u Karvezide gebruikt. Dit kan een teken zijn dat glaucoom optreedt, verhoogde druk in het oog U moet stoppen met Karvezide en uw arts raadplegen.
De hydrochloorthiazide in dit geneesmiddel kan positieve resultaten geven in de antidopingtest
Kinderen en adolescenten
Karvezide mag niet worden gegeven aan kinderen en adolescenten (jonger dan 18 jaar).
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Karvezide veranderen?
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Diuretica zoals de hydrochloorthiazide in Karvezide kunnen een effect hebben op andere geneesmiddelen Preparaten die lithium bevatten, mogen niet samen met Karvezide worden ingenomen, tenzij onder strikt medisch toezicht.
. Het kan zijn dat uw arts uw dosis moet wijzigen en/of andere voorzorgsmaatregelen moet nemen:
Als u een ACE-remmer of aliskiren gebruikt (zie ook de informatie onder de kopjes: "Wanneer mag u dit middel niet gebruiken" en "Wanneer moet u extra voorzichtig zijn met dit middel?")
Mogelijk hebt u bloedonderzoek nodig als u:
- kaliumsupplementen
- zoutvervangers die kalium bevatten
- kaliumsparende of andere diuretica
- sommige laxeermiddelen
- medicijnen voor de behandeling van jicht
- vitamine D-supplementen
- medicijnen om uw hartslag onder controle te houden
- geneesmiddelen voor diabetes (orale geneesmiddelen of insuline)
- carbamazepine (een geneesmiddel om epilepsie te behandelen).
Het is ook belangrijk om uw arts te vertellen of u andere medicijnen gebruikt om de bloeddruk te verlagen, steroïden, medicijnen om kanker te behandelen, pijnstillers, medicijnen tegen artritis, of colestyramine en colestipol om het cholesterolgehalte in het bloed te verlagen.
Waarop moet u letten met eten en drinken
Karvezide kan met of zonder voedsel worden ingenomen.
Vanwege de hydrochloorthiazide in Karvezide kunt u, als u alcohol drinkt terwijl u dit geneesmiddel gebruikt, zich duizeliger voelen bij het opstaan, vooral als u op en neer gaat.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Zwangerschap
Vertel het uw arts als u denkt zwanger te zijn (of als er een mogelijkheid bestaat om zwanger te worden); uw arts zal u gewoonlijk adviseren om te stoppen met het gebruik van Karvezide voordat u zwanger wordt of zodra u weet dat u zwanger bent en zal u adviseren om een ander geneesmiddel te gebruiken in plaats van Karvezide.Karvezide wordt niet aanbevolen tijdens de zwangerschap en mag niet worden ingenomen als u meer dan 3 maanden zwanger omdat het ernstige schade kan toebrengen aan uw baby als het na de derde maand van de zwangerschap wordt ingenomen.
Voedertijd
Vertel het uw arts als u borstvoeding geeft of gaat beginnen met borstvoeding.Karvezide wordt niet aanbevolen voor vrouwen die borstvoeding geven en uw arts kan een andere behandeling voor u kiezen als u borstvoeding wilt geven, vooral als de baby pasgeboren is of te vroeg is geboren.
Rijvaardigheid en het gebruik van machines
Er is geen onderzoek gedaan naar de rijvaardigheid en het vermogen om machines te bedienen Het is onwaarschijnlijk dat Karvezide de rijvaardigheid of het vermogen om machines te bedienen beïnvloedt. Soms kan echter duizeligheid of vermoeidheid optreden tijdens de behandeling van hoge bloeddruk. arts voordat u gaat rijden of machines gaat gebruiken.
Karvezide bevat lactose. Als uw arts u heeft verteld dat u bepaalde suikers (bijvoorbeeld lactose) niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt.
Dosis, wijze en tijdstip van toediening Hoe wordt Karvezide gebruikt: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
Dosering
De aanbevolen dosis Karvezide is één tablet per dag. Karvezide zal door uw arts aan u worden voorgeschreven als uw vorige behandeling uw bloeddruk niet voldoende heeft verlaagd. Uw arts zal u adviseren over hoe u kunt overstappen van de vorige behandeling op Karvezide.
Wijze van toediening
Karvezide is voor oraal gebruik. Slik de tabletten door met voldoende vloeistof (bijvoorbeeld een glas water). U kunt Karvezide met of zonder voedsel innemen. U moet proberen het geneesmiddel elke dag op hetzelfde tijdstip in te nemen. Het is belangrijk om de behandeling voort te zetten, tenzij uw arts vertelt je anders. .
Het maximale bloeddrukverlagende effect dient 6-8 weken na aanvang van de behandeling te worden bereikt.
Overdosering Wat moet u doen als u te veel Karvezide heeft ingenomen?
Wat u moet doen als u meer van Karvezide heeft ingenomen dan u zou mogen
Als u per ongeluk te veel tabletten heeft ingenomen, neem dan onmiddellijk contact op met uw arts.
Kinderen mogen Karvezide niet gebruiken
Karvezide mag niet worden gegeven aan kinderen jonger dan 18 jaar. Als een kind tabletten heeft ingeslikt, neem dan onmiddellijk contact op met uw arts.
Wat u moet doen wanneer u bent vergeten Karvezide in te nemen
Als u bent vergeten een dosis van het geneesmiddel in te nemen, ga dan verder met uw behandeling zoals gewoonlijk. Neem geen dubbele dosis om een vergeten dosis in te halen.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Karvezide
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Sommige van deze effecten kunnen ernstig zijn en medische aandacht vereisen.
Zeldzame gevallen van allergische huidreacties (uitslag, urticaria) en plaatselijke zwelling van het gezicht, de lippen en/of de tong zijn gemeld bij patiënten die irbesartan kregen. Als u een van de bovenstaande symptomen heeft of als u moeite heeft met ademhalen, stop dan met het gebruik van Karvezide en neem onmiddellijk contact op met uw arts.
De frequentie van de onderstaande bijwerkingen is gedefinieerd aan de hand van de volgende conventie:
Vaak: kan voorkomen bij maximaal 1 op de 10 patiënten
Soms: kan voorkomen bij maximaal 1 op de 100 patiënten
Bijwerkingen die zijn gemeld in klinische onderzoeken bij patiënten die met Karvezide werden behandeld, waren:
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 patiënten)
- misselijkheid / braken
- urinewegaandoeningen
- vermoeidheid
- duizeligheid (ook bij het gaan van zittende of liggende positie naar staan)
- bloedonderzoeken kunnen verhoogde niveaus van een enzym dat de spier- en hartfunctie meet (creatinekinase) of verhoogde niveaus van stoffen die de nierfunctie meten (BUN, creatinine) aantonen.
Vertel het uw arts als een van deze bijwerkingen u problemen geeft.
Soms voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 100 mensen)
- diarree
- hypotensie
- zwakheid
- hoge hartslag
- opvliegers
- zwelling
- seksuele disfunctie (problemen met seksuele activiteit)
- bloedonderzoek kan een verlaging van het kalium- en natriumgehalte in het bloed aantonen.
Vertel het uw arts als een van deze bijwerkingen u problemen geeft
Bijwerkingen gemeld na het op de markt brengen van Karvezide
Sommige bijwerkingen zijn gemeld sinds het op de markt brengen van Karvezide. Bijwerkingen waarvan de frequentie niet bekend is, zijn: hoofdpijn, oorsuizen, hoesten, smaakstoornissen, indigestie, gewrichts- en spierpijn, abnormale leverfunctie en nierfunctiestoornissen, hoge kaliumspiegels in het bloed en allergische reacties (huiduitslag, netelroos, plaatselijke zwelling van het gezicht, lippen, mond, tong of keel). Soms zijn ook gevallen van geelzucht (gele verkleuring van de huid en/of het wit van de ogen) gemeld.
Zoals bij elke combinatie van twee werkzame stoffen, kunnen de bijwerkingen van elk van de componenten niet worden uitgesloten.
Bijwerkingen geassocieerd met alleen irbesartan
Naast de hierboven genoemde bijwerkingen is er ook melding gemaakt van pijn op de borst
Bijwerkingen geassocieerd met alleen hydrochloorthiazide
Verlies van eetlust; maagirritatie; maagkrampen; constipatie; geelzucht (gele verkleuring van de huid en/of het wit van de ogen); ontsteking van de alvleesklier gekenmerkt door hevige pijn in de bovenbuik, vaak met misselijkheid en braken; slaapongemak; depressie ; wazig zien; gebrek aan witte bloedcellen, wat kan leiden tot frequente infecties, koorts; afname van het aantal bloedplaatjes (essentieel bestanddeel voor de bloedstolling), afname van het aantal rode bloedcellen (anemie) gekenmerkt door vermoeidheid, hoofdpijn, kortademigheid tijdens inspanning, duizeligheid en bleek uiterlijk; nieraandoeningen; longproblemen waaronder longontsteking of toegenomen vocht in de longen; verhoogde gevoeligheid van de huid voor de zon; ontsteking van bloedvaten; een huidaandoening die wordt gekenmerkt door vervelling van de huid over het hele lichaam; lupus erythematosus, te herkennen aan uitslag die op het gezicht, de nek en de hoofdhuid kan verschijnen; allergische reacties; spierzwakte en spasmen; veranderde hartslag; verlaging van de bloeddruk als gevolg van een verandering in lichaamshouding; zwelling van de speekselklieren; hoge bloedsuikerspiegels; suiker in de urine; verhogingen van sommige soorten vet in het bloed; hoge niveaus van urinezuur in het bloed die jicht kunnen veroorzaken.
Het is bekend dat de bijwerkingen die gepaard gaan met hydrochloorthiazide toenemen bij hogere doses hydrochloorthiazide.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan.
U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V.
Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de vervaldatum die staat vermeld op de doos en blister na EXP.De vervaldatum verwijst naar de laatste dag van die maand.
Niet bewaren boven 30°C.
Bewaar in de originele verpakking om het uit de buurt van vocht te houden.
Gooi geneesmiddelen niet weg via het afvalwater of met het huisvuil.Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt.Dit helpt het milieu te beschermen.
Wat bevat Karvezide
- De werkzame stoffen zijn irbesartan en hydrochloorthiazide. Elke tablet Karvezide 300 mg/12,5 mg bevat 300 mg irbesartan en 12,5 mg hydrochloorthiazide.
- De andere stoffen in dit middel zijn: microkristallijne cellulose, verknoopt natriumcarmellose, lactosemonohydraat, magnesiumstearaat, colloïdaal gehydrateerd siliciumdioxide, gepregelatineerd maïszetmeel, rode en gele ijzeroxiden (E172).
Hoe ziet Karvezide er uit en wat is de inhoud van de verpakking
Karvezide 300 mg / 12,5 mg tabletten zijn perzikkleurig, biconvex, ovaal, met een hart ingeslagen aan de ene kant en het nummer 2776 aan de andere kant.
Karvezide 300 mg/12,5 mg tabletten worden geleverd in blisterverpakkingen met 14, 28, 56 of 98 tabletten. Er zijn ook verpakkingen met geperforeerde eenheidsdosisblisterverpakkingen van 56 x 1 tablet voor ziekenhuisgebruik verkrijgbaar.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
KARVEZIDE 300 MG / 12,5 MG TABLETTEN
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet bevat 300 mg irbesartan en 12,5 mg hydrochloorthiazide.
Hulpstof met bekende effecten:
Elke tablet bevat 65,8 mg lactose (als lactosemonohydraat).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Tablet.
Perzikkleurig, biconvex, ovaal van vorm, met een hart in reliëf aan de ene kant en het nummer 2776 aan de andere.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Behandeling van essentiële arteriële hypertensie.
Combinatietherapie met een vaste dosis is geïndiceerd bij volwassen patiënten bij wie de bloeddruk niet voldoende onder controle kan worden gebracht met alleen irbesartan of hydrochloorthiazide (zie rubriek 5.1).
04.2 Dosering en wijze van toediening
Dosering
Karvezide kan eenmaal daags worden ingenomen, ongeacht de voedselinname.
Progressieve dosisaanpassing met de afzonderlijke componenten (bijv. irbesartan en hydrochloorthiazide) kan worden aanbevolen.
Indien klinisch aangewezen, kan een directe overstap van monotherapie naar vaste combinatie worden overwogen:
§ Karvezide 150 mg / 12,5 mg kan worden toegediend aan patiënten bij wie de bloeddruk niet voldoende onder controle kan worden gebracht met alleen hydrochloorthiazide of irbesartan 150 mg;
§ Karvezide 300 mg / 12,5 mg kan worden toegediend aan patiënten die onvoldoende onder controle zijn met irbesartan 300 mg of Karvezide 150 mg / 12,5 mg;
§ Karvezide 300 mg / 25 mg kan worden toegediend aan patiënten die onvoldoende onder controle zijn met Karvezide 300 mg / 12,5 mg.
Doses hoger dan 300 mg irbesartan/25 mg hydrochloorthiazide eenmaal daags worden niet aanbevolen.
Indien nodig kan Karvezide worden toegediend met andere antihypertensiva (zie rubrieken 4.3, 4.4, 4.5 en 5.1).
Speciale populaties
Nierfalen: vanwege de aanwezigheid van hydrochloorthiazide Karvezide wordt niet aanbevolen bij patiënten met ernstige nierinsufficiëntie (thiazidecreatinineklaring. Er zijn geen dosisaanpassingen nodig bij patiënten met nierdisfunctie bij wie de creatinineklaring ≥ 30 ml/min is (zie rubrieken 4.3 en 4.4).
Leverfalen: Karvezide is niet geïndiceerd bij personen met ernstige leverinsufficiëntie. Thiaziden dienen met voorzichtigheid te worden gebruikt bij patiënten met een leverfunctiestoornis. Er is geen dosisaanpassing van Karvezide nodig bij patiënten met een lichte of matige leverfunctiestoornis (zie rubriek 4.3).
Oudere bevolking: Bij ouderen is geen dosisaanpassing van Karvezide vereist.
Pediatrische populatie: Karvezide wordt niet aanbevolen voor gebruik bij kinderen en adolescenten omdat de veiligheid en werkzaamheid niet zijn vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Voor oraal gebruik.
04.3 Contra-indicaties
§ Overgevoeligheid voor de werkzame stoffen of voor één van de in rubriek 6.1 vermelde hulpstoffen of voor andere stoffen die zijn afgeleid van sulfonamide (hydrochloorthiazide is een derivaat van sulfonamide)
§ Tweede en derde trimester van de zwangerschap (zie rubrieken 4.4 en 4.6)
§ Ernstige nierinsufficiëntie (creatinineklaring)
§ Refractaire hypokaliëmie, hypercalciëmie
§ Ernstig leverfalen, biliaire cirrose en cholestase
§ Gelijktijdig gebruik van Karvezide met geneesmiddelen die aliskiren bevatten, is gecontra-indiceerd bij patiënten met diabetes mellitus of nierinsufficiëntie (glomerulaire filtratiesnelheid (GRF)
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Hypotensie - Hypovolemische patiënten: Karvezide is zelden in verband gebracht met symptomatische hypotensie bij hypertensieve patiënten zonder andere risicofactoren voor hypotensie. Dit kan voorkomen bij patiënten met hypovolemie of hyponatriëmie als gevolg van intensieve diuretica, een natriumarm dieet, diarree of braken. In dergelijke gevallen moet de aandoening worden gecorrigeerd voordat u met de behandeling met Karvezide begint.
Nierarteriestenose - Renovasculaire hypertensie: er is een verhoogd risico op ernstige hypotensie en nierfalen bij patiënten met bilaterale nierarteriestenose, of nierarteriestenose met functionerende mononier, en die behandeld worden met angiotensineconverterende enzymremmers of antagonisten van angiotensine-II-receptoren, hoewel dit niet is gedocumenteerd in Karvezide-therapie is een vergelijkbaar effect te verwachten.
Nierfalen en niertransplantatie: periodieke controle van de serumspiegels van kalium, creatinine en urinezuur wordt aanbevolen wanneer Karvezide wordt gebruikt bij patiënten met nierfunctiestoornissen. Er zijn geen klinische gegevens over de toediening van Karvezide aan patiënten met een recente niertransplantatie. Karvezide mag niet worden gebruikt bij patiënten met ernstige nierinsufficiëntie (creatinineklaring azotemie geïnduceerd door thiaziden. Er zijn geen dosisaanpassingen nodig bij patiënten met nierdisfunctie bij wie de creatinineklaring ≥ 30 ml/min is. Maar bij patiënten met lichte nierinsufficiëntie. - matig ( creatinineklaring ≥ 30 ml/min, maar
Dubbele blokkade van het renine-angiotensine-aldosteronsysteem (RAAS): Er zijn aanwijzingen dat gelijktijdig gebruik van ACE-remmers, angiotensine II-receptorblokkers of aliskiren het risico op hypotensie, hyperkaliëmie en verminderde nierfunctie (inclusief acuut nierfalen) verhoogt. Dubbele blokkade van het RAAS door het gecombineerde gebruik van ACE-remmers, angiotensine II-receptorblokkers of aliskiren wordt daarom niet aanbevolen (zie rubrieken 4.5 en 5.1). Als dual block-therapie absoluut noodzakelijk wordt geacht, mag dit alleen worden gedaan onder toezicht van een specialist en met nauwgezette en frequente controle van de nierfunctie, elektrolyten en bloeddruk. ACE-remmers en angiotensine II-receptorantagonisten mogen niet gelijktijdig worden gebruikt bij patiënten met diabetische nefropathie.
Leverfalen: speciale aandacht is vereist wanneer thiaziden worden toegediend aan patiënten met leverinsufficiëntie of progressieve leverziekte, aangezien kleine veranderingen in de water- en elektrolytenhuishouding tot levercoma kunnen leiden. Er is geen klinische ervaring met Karvezide bij patiënten met leverinsufficiëntie.
Aorta- en mitralisklepstenose, obstructieve hypertrofische cardiomyopathie: net als bij andere vaatverwijders is speciale aandacht vereist bij patiënten die lijden aan aorta- of mitralisstenose of obstructieve hypertrofische cardiomyopathie.
Primair aldosteronisme: patiënten met primair aldosteronisme reageren over het algemeen niet op antihypertensiva die werken door remming van het renine-angiotensinesysteem.Daarom wordt het gebruik van Karvezide niet aanbevolen.
Metabole en endocriene effecten: het gebruik van thiaziden kan interfereren met de glucosetolerantie Bij diabetespatiënten kan het nodig zijn om de dosis insuline of orale bloedglucoseverlagende middelen aan te passen Tijdens de behandeling met thiaziden kan latente diabetes mellitus optreden.
Verhoogde cholesterol- en triglyceridenspiegels zijn in verband gebracht met het gebruik van thiazidediuretica; bij de dosis van 12,5 mg die in Karvezide zit, zijn echter geen of minimale effecten gemeld.
Hyperurikemie of jichtcrisis kan optreden bij sommige patiënten die thiaziden gebruiken.
Verstoring van de elektrolytenbalans: zoals bij alle patiënten die diuretica ondergaan, wordt periodieke controle van de serumelektrolyten met geschikte tussenpozen aanbevolen.
Thiaziden, waaronder hydrochloorthiazide, kunnen een verstoring van de water-elektrolytenbalans veroorzaken (hypokaliëmie, hyponatriëmie en hypochloremische alkalose) Alarmsymptomen voor een verstoring van de water-elektrolytenbalans zijn: droge mond, dorst, zwakte, lethargie, slaperigheid, opwinding, spierpijn of spierkrampen, vermoeidheid, hypotensie, oligurie, tachycardie en gastro-intestinale stoornissen zoals misselijkheid of braken.
Hoewel hypokaliëmie kan optreden bij patiënten die thiazidediuretica krijgen, kan dit worden verminderd door gelijktijdige behandeling met irbesartan. Het risico op hypokaliëmie is het grootst bij patiënten met levercirrose, bij patiënten die intense diurese ondergaan, bij patiënten die onvoldoende orale inname van elektrolyten krijgen en bij patiënten die gelijktijdig worden behandeld met corticosteroïden of ACTH. Omgekeerd kan door de aanwezigheid van irbesartan in Karvezide hyperkaliëmie optreden, vooral bij nierfunctiestoornissen en/of hartfalen en diabetes mellitus. Adequate controle van het serumkalium wordt aanbevolen bij risicopatiënten. Kaliumsparende diuretica, kaliumsupplementen of kaliumbevattende zoutvervangers moeten met voorzichtigheid gelijktijdig met Karvezide worden toegediend (zie rubriek 4.5).
Er zijn geen aanwijzingen dat irbesartan door diuretica veroorzaakte hyponatriëmie vermindert of voorkomt.De hypochloremie die kan optreden is gewoonlijk mild en vereist geen behandeling.
Thiaziden kunnen de eliminatie van calcium via de urine verminderen en kunnen een intermitterende en lichte verhoging van de serumcalciumspiegels veroorzaken bij afwezigheid van bekende stoornissen van het calciummetabolisme. Duidelijke hypercalciëmie kan ongemanifesteerde hyperparathyreoïdie aan het licht brengen. Therapie met thiaziden moet worden gestopt voordat bijschildklierfunctietests worden uitgevoerd.
Van thiaziden is aangetoond dat ze de urinaire excretie van magnesium verhogen, wat hypomagnesiëmie veroorzaakt.
Lithium: de combinatie van lithium en Karvezide wordt niet aanbevolen (zie rubriek 4.5).
Dopingtest: De hydrochloorthiazide in dit geneesmiddel kan positieve resultaten geven in de antidopingtest.
Algemene waarschuwingen: bij patiënten bij wie de vasculaire tonus en nierfunctie voornamelijk afhankelijk zijn van de activiteit van het renine-angiotensine-aldosteronsysteem (bijv. patiënten met ernstig congestief hartfalen of met nierziekte, inclusief nierarteriestenose), behandeling met remmers Angiotensine converting enzyme of angiotensine- II-receptorantagonisten die dit systeem beïnvloeden, zijn in verband gebracht met acute hypotensie, azotemie, oligurie of, in zeldzame gevallen, acuut nierfalen (zie rubriek 4.5) Zoals met elk antihypertensivum (zie rubriek 4.5) kan een overmatige bloeddrukdaling bij patiënten met ischemisch hart optreden ziekte of ischemische hart- en vaatziekten, kan leiden tot een hartinfarct of beroerte.
Overgevoeligheidsreacties op hydrochloorthiazide kunnen optreden bij patiënten met of zonder een voorgeschiedenis van allergieën of bronchiale astma; in het eerste geval zijn dergelijke reacties echter waarschijnlijker.
Het optreden en/of verergering van systemische lupus erythematodes is gemeld bij het gebruik van thiazidediuretica.
Er zijn gevallen van fotosensitiviteitsreacties gemeld bij het gebruik van thiazidediuretica (zie rubriek 4.8). Als tijdens de behandeling een fotosensibilisatiereactie optreedt, wordt aanbevolen de behandeling te staken. Als het hervatten van de behandeling noodzakelijk wordt geacht, wordt aanbevolen de behandeling te hervatten. bescherm gebieden die zijn blootgesteld aan zonlicht of kunstmatige UVA-stralen.
Zwangerschap: therapie met angiotensine II-receptorantagonisten (AIIRA's) mag niet worden gestart tijdens de zwangerschap. Een alternatieve antihypertensieve behandeling met een bewezen veiligheidsprofiel voor gebruik tijdens de zwangerschap moet worden gebruikt voor patiënten die van plan zijn zwanger te worden, tenzij voortzetting van de behandeling met een AIIRA essentieel wordt geacht. Wanneer zwangerschap wordt vastgesteld, moet de behandeling met AIIRA's onmiddellijk worden stopgezet en, indien van toepassing, moet een alternatieve therapie worden gestart (zie rubrieken 4.3 en 4.6).
Lactose: dit geneesmiddel bevat lactose. Patiënten met zeldzame erfelijke aandoeningen als galactose-intolerantie, Lapp-lactasedeficiëntie of glucose-galactosemalabsorptie dienen dit geneesmiddel niet te gebruiken.
Acute bijziendheid of secundair acuut gesloten hoekglaucoom: Op sulfonamide gebaseerde geneesmiddelen of van sulfonamide afgeleide geneesmiddelen kunnen een idiosyncratische reactie veroorzaken, wat resulteert in voorbijgaande bijziendheid en acuut geslotenhoekglaucoom. Hoewel hydrochloorthiazide een sulfonamide is, zijn tot nu toe alleen geïsoleerde gevallen van acuut nauwekamerhoekglaucoom gemeld met hydrochloorthiazide Symptomen zijn onder meer een acuut begin van verminderde gezichtsscherpte of oculaire pijn en treden meestal op binnen enkele uren tot weken na aanvang van de behandeling. Onbehandeld acuut geslotenhoekglaucoom kan leiden tot permanent verlies van het gezichtsvermogen. De belangrijkste behandeling is om de toediening van het geneesmiddel zo snel mogelijk te stoppen. Als de intraoculaire druk ongecontroleerd blijft, moet mogelijk een snelle medische of chirurgische behandeling worden overwogen. Een voorgeschiedenis van allergie voor sulfonamiden of penicillines kan worden beschouwd als risicofactoren voor de ontwikkeling van acuut nauwekamerhoekglaucoom (zie rubriek 4.8).
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Andere antihypertensiva: het antihypertensieve effect van Karvezide kan toenemen bij gelijktijdig gebruik van andere antihypertensiva. Irbesartan en hydrochloorthiazide (in doses tot 300 mg irbesartan/25 mg hydrochloorthiazide) zijn veilig toegediend met andere antihypertensiva, waaronder calciumkanaalblokkers en bèta-adrenerge blokkers. Voorafgaande behandeling met hoge doses diuretica kan leiden tot hypovolemie en, indien niet eerder gecorrigeerd, kan leiden tot een risico op hypotensie bij het starten van een behandeling met irbesartan met of zonder thiazidediuretica (zie rubriek 4.4).
Geneesmiddelen die aliskiren of ACE-remmers bevatten: Gegevens uit klinische onderzoeken hebben aangetoond dat dubbele blokkade van het renine-angiotensine-aldosteronsysteem (RAAS) door het gecombineerde gebruik van ACE-remmers, angiotensine II-receptorblokkers of aliskiren gepaard gaat met een hogere frequentie van bijwerkingen. hyperkaliëmie en verminderde nierfunctie (inclusief acuut nierfalen) in vergelijking met het gebruik van een enkelvoudig middel dat actief is op het RAAS-systeem (zie rubrieken 4.3, 4.4 en 5.1).
Lithium : Er is een omkeerbare stijging van de serumconcentraties en toxiciteit van lithium gevonden wanneer het gelijktijdig wordt toegediend met angiotensineconverterende enzymremmers. Vergelijkbare effecten zijn tot dusver zeer zelden gemeld met irbesartan. Bovendien wordt de renale klaring van lithium verminderd door thiaziden met een verhoogd risico op lithiumtoxiciteit met Karvezide. Daarom wordt de combinatie van lithium en Karvezide niet aanbevolen (zie rubriek 4.4). Als de combinatie echt nodig is, wordt een zorgvuldige controle van de serumlithiumspiegels aanbevolen.
Geneesmiddelen die de kaliumspiegel beïnvloeden: de kaliumdepletie veroorzaakt door hydrochloorthiazide wordt afgezwakt door het kaliumsparende effect geïnduceerd door irbesartan.Dit effect van hydrochloorthiazide op het serumkalium zou echter versterkt worden door andere geneesmiddelen die kaliumverlies en hypokaliëmie veroorzaken (andere kaliumsparende, laxeermiddelen, amfotericine, carbenoxolon, penicilline G natrium). Omgekeerd, op basis van ervaring met andere geneesmiddelen die de activiteit van het renine-angiotensinesysteem verminderen, kan het gelijktijdige gebruik van kaliumsparende diuretica, kaliumsupplementen, kaliumbevattende zoutvervangers of andere geneesmiddelen die de serumkaliumspiegels kunnen verhogen (bijv. ) kan een verhoging van het kalium veroorzaken.Adequate controle van het serumkalium wordt aanbevolen bij risicopatiënten (zie rubriek 4.4).
Geneesmiddelen beïnvloed door veranderingen in kalium: wanneer Karvezide wordt toegediend in combinatie met andere potentieel gevaarlijke geneesmiddelen in geval van veranderingen in het serumkalium (bijv. digitalisglycosiden, antiaritmica), wordt periodieke controle van het kalium aanbevolen.
Steroïdeloze ontstekingsremmers: wanneer angiotensine-II-antagonisten gelijktijdig worden toegediend met niet-steroïde anti-inflammatoire geneesmiddelen (dwz selectieve COX-2-remmers, acetylsalicylzuur (> 3 g/dag) en niet-selectieve niet-steroïdale anti-inflammatoire geneesmiddelen), verzwakking van het antihypertensivum effect kan optreden.
Net als bij ACE-remmers kan het gelijktijdige gebruik van angiotensine-II-antagonisten en niet-steroïde anti-inflammatoire geneesmiddelen leiden tot een verhoogd risico op verslechtering van de nierfunctie, waaronder mogelijk acuut nierfalen, en tot een verhoging van het serumkalium, met name bij patiënten. met een reeds bestaande matige nierfunctie. De combinatie moet met voorzichtigheid worden toegediend, vooral bij ouderen. Patiënten dienen voldoende gehydrateerd te zijn en controle van de nierfunctie dient te worden overwogen na het starten van de combinatietherapie en periodiek daarna.
Nadere informatie over interacties met irbesartan: in klinische onderzoeken werd de farmacokinetiek van irbesartan niet beïnvloed door hydrochloorthiazide Irbesartan wordt voornamelijk gemetaboliseerd door CYP2C9 en in mindere mate via glucuronidering. Er werden geen significante farmacokinetische of farmacodynamische interacties waargenomen na gelijktijdige toediening van irbesartan met warfarine, een geneesmiddel dat wordt gemetaboliseerd door CYP2C9. De effecten van CYP2C9-inductoren, zoals rifampicine, op de farmacokinetiek van irbesartan zijn niet onderzocht.De farmacokinetiek van digoxine veranderde niet door gelijktijdige toediening van irbesartan.
Nadere informatie over interacties met hydrochloorthiazide: bij gelijktijdige toediening kunnen de volgende geneesmiddelen een wisselwerking hebben met thiazidediuretica:
Alcohol: potentiëring van orthostatische hypotensie kan optreden;
Antidiabetica (orale antidiabetica en insuline): dosisaanpassing van het antidiabeticum kan nodig zijn (zie rubriek 4.4);
Colestyramine en colestipol: de absorptie van hydrochloorthiazide wordt verminderd in aanwezigheid van de anionenuitwisselingsharsen Karvezide moet ten minste 1 uur vóór of 4 uur na deze geneesmiddelen worden ingenomen;
Corticosteroïden, ACTH: elektrolytdepletie, vooral kalium, kan toenemen;
Digitalisglycosiden: hypokaliëmie en hypomagnesiëmie veroorzaakt door thiaziden bevorderen het ontstaan van digitalis-hartritmestoornissen (zie rubriek 4.4);
Steroïdeloze ontstekingsremmers: bij sommige patiënten kan de toediening van een niet-steroïde anti-inflammatoir geneesmiddel de diuretische, natriumuretische en antihypertensieve effecten van thiazidediuretica verminderen;
Pressoramines (bijv. noradrenaline): het effect van de pressoraminen kan worden verminderd, maar niet zozeer dat het gebruik ervan wordt uitgesloten;
Niet-depolariserende spierverslappers (bijv. tubocurarine): het effect van niet-depolariserende musculoskeletale relaxantia kan worden versterkt door hydrochloorthiazide;
Geneesmiddelen tegen jicht: Aanpassing van de dosering van anti-outgeneesmiddelen kan nodig zijn, aangezien hydrochloorthiazide de serumurinezuurspiegels kan verhogen. Een verhoging van de dosering van probenecide of sulfinpyrazon kan nodig zijn. Gelijktijdige toediening van thiazidediuretica kan de incidentie van overgevoeligheidsreacties verhogen, alle "allopurinol;
Calciumzouten: thiazidediuretica kunnen de serumcalciumspiegels verhogen door een verminderde excretie. Als het nodig is om calciumsupplementen of calciumsparende geneesmiddelen toe te dienen (bijv. vitamine D-therapie), moet de calciumspiegel onder controle worden gehouden en de calciumdosering dienovereenkomstig worden aangepast;
Carbamazepine: Gelijktijdig gebruik van carbamazepine en hydrochloorthiazide is in verband gebracht met het risico op symptomatische hyponatriëmie Tijdens gelijktijdig gebruik dienen elektrolyten gecontroleerd te worden. Indien mogelijk moet een andere klasse diuretica worden gebruikt.
Andere interacties: thiaziden kunnen het hyperglykemische effect van bètablokkers en diazoxide versterken Anticholinergica (bijv. atropine, beperiden) kunnen de biologische beschikbaarheid van diuretica van het thiazidetype verhogen door een afname van de gastro-intestinale motiliteit en maagledigingssnelheid Thiaziden kunnen het risico op bijwerkingen van amantidine verhogen Thiaziden kunnen de renale excretie van cytotoxische geneesmiddelen (bijv. cyclofosfamide, methotrexaat) verminderen en hun myelosuppressieve effect versterken.
04.6 Zwangerschap en borstvoeding
Zwangerschap:
Angiotensine II-receptorantagonisten (AIIRA's):
Het gebruik van angiotensine II-receptorantagonisten (AIIRA's) wordt niet aanbevolen tijdens het eerste trimester van de zwangerschap (zie rubriek 4.4). Het gebruik van AIIRA's is gecontra-indiceerd tijdens het tweede en derde trimester van de zwangerschap (zie rubrieken 4.3 en 4.4).
Epidemiologisch bewijs over het risico op teratogeniteit na blootstelling aan ACE-remmers tijdens het eerste trimester van de zwangerschap was niet overtuigend; een kleine verhoging van het risico kan echter niet worden uitgesloten. Hoewel er geen gecontroleerde epidemiologische gegevens over het risico met angiotensine II-receptorantagonisten (AIIRA's) beschikbaar zijn, kan een vergelijkbaar risico ook bestaan voor deze klasse geneesmiddelen Voor patiënten die zwanger willen worden, moet een alternatieve antihypertensieve behandeling worden gebruikt met een bewezen veiligheidsprofiel voor gebruik tijdens de zwangerschap, tenzij voortzetting van de behandeling met een AIIRA als essentieel wordt beschouwd. Wanneer zwangerschap wordt vastgesteld, moet de behandeling met AIIRA's onmiddellijk worden stopgezet en, indien van toepassing, moet een alternatieve therapie worden gestart.
Het is bekend dat blootstelling aan AIIRA's tijdens het tweede en derde trimester foetale toxiciteit (verminderde nierfunctie, oligohydramnie, achterstand in schedelverharding) en neonatale toxiciteit (nierfalen, hypotensie, hyperkaliëmie) bij vrouwen induceert (zie rubriek 5.3. ).
Indien blootstelling aan AIIRA's heeft plaatsgevonden vanaf het tweede trimester van de zwangerschap, wordt echografische controle van de nierfunctie en schedel aanbevolen.
Pasgeborenen van wie de moeder AIIRA's heeft gebruikt, moeten nauwlettend worden gecontroleerd op hypotensie (zie rubrieken 4.3 en 4.4).
Hydrochloorthiazide:
Ervaring met hydrochloorthiazide tijdens de zwangerschap is beperkt, vooral tijdens het eerste trimester Dierstudies zijn onvoldoende Hydrochloorthiazide passeert de placentabarrière. Op basis van het farmacologische werkingsmechanisme van hydrochloorthiazide kan het gebruik ervan tijdens het tweede en derde trimester de doorbloeding van de foetus en de placenta verminderen en foetale en neonatale effecten veroorzaken, zoals geelzucht, verstoring van de elektrolytenbalans en trombocytopenie.
Hydrochloorthiazide mag niet worden gebruikt bij zwangerschapsoedeem, zwangerschapshypertensie of pre-eclampsie vanwege het risico op een verminderd plasmavolume en placentaire hypoperfusie, zonder gunstige effecten op het verloop van de ziekte.
Hydrochloorthiazide mag niet worden gebruikt voor essentiële hypertensie bij zwangere vrouwen, behalve in zeldzame uitzonderingen wanneer andere behandelingen niet kunnen worden gebruikt.
Aangezien Karvezide hydrochloorthiazide bevat, wordt het gebruik ervan tijdens het eerste trimester van de zwangerschap niet aanbevolen.Overschakelen naar een geschikte alternatieve behandeling moet worden overwogen voordat een zwangerschap wordt gepland.
Voedertijd:
Angiotensine II-receptorantagonisten (AIIRA's):
Aangezien er geen gegevens beschikbaar zijn over het gebruik van Karvezide tijdens het geven van borstvoeding, wordt Karvezide niet aanbevolen en hebben alternatieve behandelingen met een bewezen veiligheidsprofiel voor gebruik tijdens het geven van borstvoeding de voorkeur, vooral bij pasgeborenen en prematuren die borstvoeding geven.
Het is niet bekend of irbesartan of zijn metabolieten in de moedermelk worden uitgescheiden.
Uit beschikbare farmacodynamische/toxicologische gegevens bij ratten blijkt dat irbesartan of zijn metabolieten in melk worden uitgescheiden (zie rubriek 5.3 voor details).
Hydrochloorthiazide:
Hydrochloorthiazide wordt in kleine hoeveelheden uitgescheiden in de moedermelk. Thiaziden in hoge doses kunnen de melkproductie remmen en intense diurese veroorzaken. Het gebruik van Karvezide tijdens het geven van borstvoeding wordt niet aanbevolen. Als Karvezide tijdens het geven van borstvoeding wordt gebruikt, moeten de doses zo laag mogelijk worden gehouden.
Vruchtbaarheid:
Irbesartan had geen effect op de vruchtbaarheid van behandelde ratten en hun nakomelingen tot dosisniveaus die de eerste tekenen van toxiciteit bij de ouders induceerden (zie rubriek 5.3).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er zijn geen onderzoeken uitgevoerd naar de rijvaardigheid en het vermogen om machines te bedienen. Vanwege de farmacodynamische eigenschappen is het onwaarschijnlijk dat Karvezide deze vermogens beïnvloedt. Bij het besturen van voertuigen of het bedienen van machines moet worden opgemerkt dat af en toe duizeligheid of vermoeidheid kan optreden tijdens de behandeling van hypertensie .
04.8 Bijwerkingen
Irbesartan/hydrochloorthiazide combinatie
29,5% van de 898 hypertensieve patiënten die tijdens de placebogecontroleerde onderzoeken verschillende doseringen irbesartan/hydrochloorthiazide kregen (bereik: 37,5 mg/6,25 mg tot 300 mg/25 mg) had bijwerkingen. De meest gemelde bijwerkingen waren duizeligheid (5,6%), vermoeidheid (4,9%), misselijkheid/braken (1,8%) en abnormaal urineren (1,4%). Bovendien werden tijdens klinische onderzoeken vaak azotemie (BUN) (2,3%), creatinekinase (1,7%) en creatinine (1,1%) verhoging waargenomen.
Tabel 1 vermeldt bijwerkingen van spontane en waargenomen bijwerkingen in placebogecontroleerde klinische onderzoeken.
De frequentie van de hieronder beschreven bijwerkingen wordt gedefinieerd aan de hand van de volgende conventie: zeer vaak (≥ 1/10); vaak (≥ 1/100 tot
Aanvullende informatie over de afzonderlijke componenten: naast de hierboven beschreven bijwerkingen voor de combinatie, kunnen andere eerder gemelde bijwerkingen met een van de componenten mogelijke bijwerkingen van Karvezide zijn. In de onderstaande tabellen 2 en 3 worden bijwerkingen vermeld die zijn gemeld met de afzonderlijke componenten van Karvezide.
Dosisafhankelijke bijwerkingen van hydrochloorthiazide (vooral elektrolytenstoornissen) kunnen toenemen bij een geleidelijke verhoging van de dosering.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om vermoedelijke bijwerkingen te melden die optreden na toelating van het geneesmiddel. Het maakt continue monitoring van de baten/risicoverhouding van het geneesmiddel mogelijk. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem.
04.9 Overdosering
Er is geen specifieke informatie beschikbaar over de behandeling van overdosering met Karvezide. De patiënt moet nauwlettend worden gecontroleerd, de behandeling moet symptomatisch en ondersteunend zijn en zal afhangen van de tijd sinds de inname en de ernst van de symptomen De voorgestelde maatregelen zijn onder meer het opwekken van braken en/of maagspoeling Actieve kool Serumelektrolyten en creatinine moeten regelmatig worden gecontroleerd. hypotensie optreedt, moet de patiënt in rugligging worden gelegd en onmiddellijk worden aangevuld met zouten en vloeistoffen.
De belangrijkste verschijnselen van een overdosis irbesartan zijn hypotensie en tachycardie; Bradycardie kan ook optreden.
Een overdosis hydrochloorthiazide wordt in verband gebracht met elektrolytdepletie (hypokaliëmie, hypochloremie, hyponatriëmie) en dehydratie na overmatige diurese. De belangrijkste tekenen en symptomen van overdosering zijn misselijkheid en slaperigheid. Hypokaliëmie kan spierspasmen veroorzaken en/of hartritmestoornissen verergeren die gepaard gaan met het gelijktijdig gebruik van digitalisglycosiden of bepaalde antiaritmica.
Irbesartan is niet dialyseerbaar. De hoeveelheid hydrochloorthiazide die door hemodialyse wordt verwijderd, is niet bekend.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: angiotensine-II-antagonisten, combinaties
ATC-code: C09DA04.
Karvezide is een combinatie van een angiotensine-II-receptorantagonist irbesartan en een thiazidediureticum, hydrochloorthiazide. De combinatie van deze actieve ingrediënten zorgt voor een additief antihypertensief effect, waardoor de bloeddruk sterker wordt verlaagd dan de afzonderlijke componenten.
Irbesartan is een krachtige en selectieve angiotensine-II-receptorantagonist (AT1-subtype), actief voor orale toediening. Aangenomen wordt dat het geneesmiddel alle AT1-gemedieerde effecten van angiotensine-II blokkeert, ongeacht de oorsprong of route van angiotensine-II-synthese.Selectief antagonisme voor angiotensine-II (AT1) veroorzaakt een verhoging van de plasmarenine- en angiotensine-II-spiegels en een afname van de plasma-aldosteronconcentratie. Bij patiënten die geen risico lopen op een verstoorde elektrolytenbalans (zie rubrieken 4.4 en 4.5), wordt het kalium niet wezenlijk veranderd door irbesartan alleen in de aanbevolen doseringen. Irbesartan remt niet ACE (kininase-II), een enzym dat angiotensine-II genereert en bradykinine afbreekt om inactieve metabolieten te produceren. Irbesartan vereist geen metabolische activering om zijn farmacologische activiteit uit te oefenen.
Hydrochloorthiazide is een thiazidediureticum Het mechanisme waarmee thiazidediuretica hun antihypertensieve effecten uitoefenen is niet volledig begrepen Thiaziden werken in op de renale tubulaire mechanismen van elektrolytreabsorptie, waardoor de uitscheiding van natrium en chloride in vrijwel gelijke hoeveelheden direct wordt verhoogd. De diuretische werking van hydrochloorthiazide vermindert het plasmavolume, verhoogt de plasmarenine-activiteit en verhoogt de aldosteronsecretie, wat resulteert in een verhoogd verlies van kalium en bicarbonaat in de urine en een verlaagd serumkalium. Vermoedelijk door blokkering van het renine-angiotensine-aldosteronsysteem heeft gelijktijdige toediening van irbesartan de neiging om het kaliumverlies geassocieerd met deze diuretica te corrigeren. Met hydrochloorthiazide begint de diurese binnen 2 uur, de piek treedt op rond het vierde uur en het effect houdt ongeveer 6-12 uur aan.
Binnen het therapeutische bereik resulteert de combinatie van hydrochloorthiazide en irbesartan in een dosisafhankelijke additieve verlaging van de bloeddruk. De toevoeging van 12,5 mg hydrochloorthiazide aan irbesartan 300 mg eenmaal daags bij patiënten die onvoldoende onder controle waren met irbesartan 300 mg monotherapie resulteerde in een verdere verlaging van de diastolische bloeddruk met 6,1 mmHg in vergelijking met placebo (24 uur later).De combinatie van irbesartan 300 mg en hydrochloorthiazide 12,5 mg resulteert in een algehele verlaging van de systolische/diastolische bloeddruk, vergeleken met placebo, tot 13,6 / 11,5 mmHg.
Beperkte klinische gegevens (7 van 22 patiënten) suggereren dat patiënten die niet onder controle zijn met de combinatie van 300 mg/12,5 mg, kunnen reageren wanneer ze worden behandeld met de combinatie van 300 mg/25 mg. Een superieur hypotensief effect op zowel de systolische bloeddruk (PAS) als de diastolische bloeddruk (PAD) werd waargenomen bij deze patiënten (respectievelijk 13,3 en 8,3 mmHg).
Bij patiënten met lichte tot matige hypertensie leidde eenmaal daagse toediening van 150 mg irbesartan en 12,5 mg hydrochloorthiazide tot een gemiddelde verlaging van 12,9 / 6,9 mmHg van de systolische/diastolische bloeddruk in vergelijking met placebo (24 uur na toediening). De antihypertensieve piek wordt bereikt na 3-6 uur. Continue 24-uurs monitoring van de bloeddruk toont aan dat de combinatie van 150 mg irbesartan en 12,5 mg hydrochloorthiazide eenmaal daags een vergelijkbare verlaging van de bloeddruk geeft over 24 uur, met een gemiddelde verlaging van de systolische/diastolische bloeddruk vergeleken met placebo, gedurende 24 uur van 15,8 / 10,0 mmHg Gemeten met continue monitoring gedurende 24 uur, was het dal-/piekeffect van Karvezide 150 mg / 12,5 mg 100%. Gemeten door manchet tijdens een polikliniekbezoek, was het dal-/piekeffect respectievelijk 68% en 76% voor Karvezide 150 mg / 12,5 mg en Karvezide 300 mg / 12,5 mg. Deze effecten werden waargenomen gedurende 24 uur zonder overmatige verlaging van het bloed druk tot piek en zijn consistent met de veilige en effectieve verlaging die wordt verkregen met eenmaal daagse dosering Bij patiënten die onvoldoende onder controle waren met alleen 25 mg hydrochloorthiazide, veroorzaakte de toevoeging van irbesartan een verdere gemiddelde verlaging van de waarden systolisch/diastolisch, in vergelijking met placebo, van 11,1 / 7,2 mmHg.
Het antihypertensieve effect van irbesartan in combinatie met hydrochloorthiazide treedt op na de eerste dosis en is duidelijk binnen 1-2 weken, met een maximaal effect binnen 6-8 weken. In langetermijnstudies was het effect van irbesartan en hydrochloorthiazide constant gedurende meer dan een jaar Hoewel niet specifiek onderzocht met Karvezide, werd rebound-hypertensie niet waargenomen met irbesartan of hydrochloorthiazide.
Het effect van de combinatie van irbesartan en hydrochloorthiazide op morbiditeit en mortaliteit is niet onderzocht.Epidemiologische studies hebben aangetoond dat langdurige behandeling met hydrochloorthiazide het risico op cardiovasculaire mortaliteit en morbiditeit vermindert.
De werkzaamheid van Karvezide wordt niet beïnvloed door leeftijd of geslacht. Net als bij andere geneesmiddelen die het renine-angiotensinesysteem beïnvloeden, reageren negroïde hypertensieve patiënten significant minder op irbesartan alleen. Wanneer irbesartan gelijktijdig wordt toegediend met een lage dosis hydrochloorthiazide (bijv. 12,5 mg/dag), benadert de antihypertensieve respons bij negroïde patiënten die bij niet-negroïde patiënten.
De werkzaamheid en veiligheid van Karvezide als initiële therapie voor ernstige hypertensie (gedefinieerd als SeDBP ≥ 110 mmHg) werd geëvalueerd in een 8 weken durende, multicenter, gerandomiseerde, dubbelblinde, actief-gecontroleerde studie met parallelle armen. In totaal werden 697 patiënten gerandomiseerd in een 2-op-1-verhouding om ofwel irbesartan/hydrochloorthiazide 150 mg/12,5 mg ofwel irbesartan 150 mg te krijgen, dat systematisch werd getitreerd (voordat respons op de minimale dosis werd gevonden) en na één week irbesartan / hydrochloorthiazide 300 mg / 25 mg of irbesartan 300 mg respectievelijk.
De studie rekruteerde 58% mannelijke patiënten. De gemiddelde leeftijd van de patiënten was 52,5 jaar, 13% was ≥ 65 jaar en slechts 2% was ≥ 75 jaar. Twaalf procent (12%) van de patiënten had diabetes, 34% was dyslipidemisch en de meest voorkomende cardiovasculaire pathologie was stabiele angina pectoris aanwezig bij 3,5% van de onderzochte proefpersonen.
Het primaire doel van deze studie was om het percentage patiënten te vergelijken bij wie SeDBP controle bereikte (SeDBP
De kwaliteit en incidentie van bijwerkingen die werden geregistreerd voor patiënten die werden behandeld met combinatietherapie waren vergelijkbaar met het bijwerkingenprofiel voor patiënten die monotherapie kregen. Gedurende 8 weken behandeling werden geen gevallen van syncope gemeld in beide behandelingsgroepen. Er waren 0,6% en 0% gevallen van hypotensie en 2,8% en 3,1% gevallen van duizeligheid als bijwerkingen gemeld in respectievelijk de patiëntengroepen met combinatietherapie en monotherapie.
Dubbele blokkade van het renine-angiotensine-aldosteronsysteem (RAAS)
Twee grote gerandomiseerde gecontroleerde onderzoeken (ONTARGET (ONgoing Telmisartan Alone and in combinatie met Ramipril Global Endpoint Trial) en VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) hebben het gebruik van de combinatie van een ACE-remmer met een antagonist van de angiotensine II-receptor. ONTARGET was een onderzoek dat werd uitgevoerd bij patiënten met een voorgeschiedenis van cardiovasculaire of cerebrovasculaire aandoeningen, of type 2-diabetes mellitus in verband met aanwijzingen voor orgaanschade. VA NEPHRON-D was een onderzoek dat werd uitgevoerd bij patiënten met diabetes mellitus type 2 en diabetische nefropathie.
Deze onderzoeken hebben geen significant gunstig effect op de nier- en/of cardiovasculaire uitkomsten en mortaliteit aangetoond, terwijl een verhoogd risico op hyperkaliëmie, acuut nierletsel en/of hypotensie werd waargenomen in vergelijking met monotherapie. Deze resultaten zijn ook relevant voor andere ACE-remmers en angiotensine II-receptorantagonisten, gezien hun vergelijkbare farmacodynamische eigenschappen.
ACE-remmers en angiotensine II-receptorantagonisten mogen daarom niet gelijktijdig worden gebruikt bij patiënten met diabetische nefropathie.
ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) was een onderzoek gericht op het verifiëren van het voordeel van het toevoegen van aliskiren aan de standaardtherapie van een ACE-remmer of angiotensine II-receptorantagonist bij patiënten met diabetes mellitus type 2 en chronische nierziekte , hart- en vaatziekten, of beide. De studie werd vroegtijdig beëindigd vanwege een verhoogd risico op bijwerkingen. Cardiovasculaire sterfte en beroerte kwamen beide numeriek vaker voor in de aliskiren-groep dan in de placebogroep, en bijwerkingen en ernstige bijwerkingen die van belang waren ( hyperkaliëmie, hypotensie en nierdisfunctie) werden vaker gemeld in de aliskiren-groep dan in de placebogroep.
05.2 "Farmacokinetische eigenschappen
Gelijktijdige toediening van hydrochloorthiazide en irbesartan heeft geen invloed op de farmacokinetiek van beide.
Irbesartan en hydrochloorthiazide zijn als zodanig oraal actief en vereisen geen biotransformatie om actief te zijn. Na orale toediening van Karvezide is de absolute orale biologische beschikbaarheid 60-80% voor irbesartan en 50-80% voor hydrochloorthiazide. Voedsel heeft geen invloed op de biologische beschikbaarheid van Karvezide. De maximale plasmaconcentratie wordt 1,5-2 uur na orale toediening voor irbesartan en 1-2,5 uur voor hydrochloorthiazide bereikt.
Eiwitbinding is ongeveer 96% met een verwaarloosbare hoeveelheid binding aan bloedcellen. Het distributievolume van irbesartan is 53-93 liter De eiwitbinding voor hydrochloorthiazide is 68%, met een schijnbaar distributievolume van 0,83-1,14 l/kg.
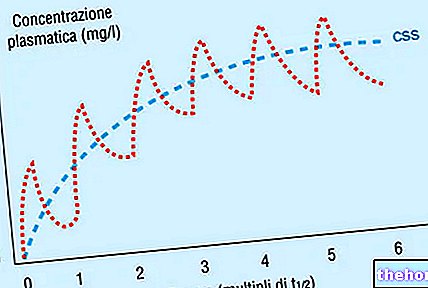
Irbesartan vertoont een lineaire en dosisproportionele farmacokinetiek over het dosisbereik van 10-600 mg Een minder dan evenredige toename van de orale absorptie werd waargenomen bij doses boven 600 mg; het mechanisme waarmee dit wordt bepaald is onbekend. De totale lichaams- en renale klaring zijn respectievelijk 157-176 en 3,0-3,5 ml/min. De terminale eliminatiehalfwaardetijd van irbesartan is 11-15 uur Steady-state plasmaconcentraties worden bereikt binnen 3 dagen na aanvang van eenmaal daagse dosering. Verminderde accumulatie van irbesartan (plasma na herhaalde eenmaal daagse dosering. In één onderzoek werden iets hogere plasmaconcentraties waargenomen bij hypertensieve patiënten. Er was echter geen verschil in de halfwaardetijd of accumulatie van irbesartan. dosering bij patiënten AUC en Cmax
Na orale of intraveneuze toediening van 14C-gelabeld irbesartan, is 80-85% van de gedetecteerde radioactiviteit in het plasma toe te schrijven aan onveranderd irbesartan. Irbesartan wordt door de lever gemetaboliseerd door oxidatie en glucuronideconjugatie. De belangrijkste circulerende metaboliet (ongeveer 6%) is irbesartanglucuronide. in vitro geven aan dat irbesartan voornamelijk wordt geoxideerd via het cytochroom P450-enzym CYP2C9; het CYP3A4-iso-enzym heeft een verwaarloosbaar effect Irbesartan en zijn metabolieten worden zowel via de gal als via de nieren geëlimineerd. Na orale of intraveneuze toediening van 14C-irbesartan kan ongeveer 20% van de radioactiviteit in de urine worden teruggevonden, terwijl de rest aantoonbaar is in de feces. Minder dan 2% van de ingenomen dosis wordt als onveranderd irbesartan in de urine uitgescheiden. Hydrochloorthiazide wordt niet gemetaboliseerd maar wordt snel uitgescheiden door de nieren Ten minste 61% van de orale dosis wordt binnen 24 uur onveranderd uitgescheiden Hydrochloorthiazide passeert de placenta, maar kan de bloed-hersenbarrière niet passeren en wordt uitgescheiden in de moedermelk.
Nierfalen : bij patiënten met nierinsufficiëntie of bij hemodialysepatiënten zijn de farmacokinetische parameters van irbesartan niet significant gewijzigd. Irbesartan wordt niet verwijderd tijdens het hemodialyseproces. Er is gemeld dat bij patiënten met een creatinineklaring
Leverinsufficiëntie : bij personen met lichte tot matige cirrose zijn de farmacokinetische parameters van irbesartan niet significant veranderd. Er zijn geen onderzoeken uitgevoerd bij patiënten met een ernstige leverfunctiestoornis.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Irbesartan / hydrochloorthiazide: de potentiële toxiciteit van de combinatie irbesartan/hydrochloorthiazide na orale toediening werd geëvalueerd bij ratten en makaken in onderzoeken tot 6 maanden Er waren geen toxicologische waarnemingen die relevant zijn voor therapeutisch gebruik bij mensen.
De volgende veranderingen, waargenomen bij ratten en makaken die werden behandeld met de combinatie irbesartan/hydrochloorthiazide in een dosering van 10/10 en 90/90 mg/kg/dag, werden ook waargenomen met ofwel alleen het geneesmiddel en/of waren secundair aan bloeddrukverlagingen arteriële (geen significante toxicologische interacties werden waargenomen):
§ veranderingen in de nieren, gekenmerkt door een lichte toename van urikemie en creatininemie, en door hyperplasie/hypertrofie van het juxtaglomerulaire apparaat, die een direct gevolg zijn van de interactie van irbesartan met het renine-angiotensinesysteem;
§ lichte dalingen in erytrocytenparameters (erytrocyten, hemoglobine, hematocriet);
§ Maagverkleuring, zweren en focale necrose van het maagslijmvlies werden waargenomen bij enkele ratten in een toxiciteitsonderzoek van 6 maanden met irbesartan toegediend in een dosis van 90 mg/kg/dag, hydrochloorthiazide 90 mg/kg/dag en irbesartan/hydrochloorthiazide 10/10 mg/kg/dag. Deze laesies werden niet waargenomen bij makaken;
§ verlaging van het serumkalium als gevolg van hydrochloorthiazide en wordt gedeeltelijk voorkomen bij gelijktijdige toediening met irbesartan.
De meeste van de bovengenoemde effecten lijken het gevolg te zijn van de farmacologische activiteit van irbesartan (blokkade van door angiotensine II geïnduceerde remming van de afgifte van renine, met stimulatie van renineproducerende cellen) en treden ook op bij enzymremmers omzetting van angiotensine. niet relevant zijn voor de therapeutische doseringen van irbesartan/hydrochloorthiazide die bij mensen worden gebruikt.
max
irbesartan waren ook iets hoger bij oudere patiënten (≥ 65 jaar) dan bij jongere proefpersonen (18-40 jaar), maar de uiteindelijke halfwaardetijd was niet significant veranderd. Bij ouderen zijn geen dosisaanpassingen nodig. De gemiddelde plasmahalfwaardetijd van hydrochloorthiazide varieert tussen 5-15 uur.
Er zijn geen teratogene effecten waargenomen bij ratten die werden behandeld met de combinatie van irbesartan en hydrochloorthiazide in doses die maternale toxiciteit veroorzaken. De effecten van de combinatie ibersartan/hydrochloorthiazide op de vruchtbaarheid zijn nog niet geëvalueerd in dierstudies, aangezien ze niet zijn gemeld. effecten op de vruchtbaarheid bij dieren of mensen met zowel irbesartan als hydrochloorthiazide wanneer het alleen wordt gegeven.In dierstudies had echter een andere angiotensine-II-antagonist invloed op de vruchtbaarheidsparameters wanneer het alleen werd gegeven. Deze bevindingen zijn ook waargenomen bij lage doses van deze angiotensine-II-antagonist bij gelijktijdige toediening met hydrochloorthiazide.
Er zijn geen aanwijzingen voor mutageniteit of clastogeniteit met de combinatie irbesartan/hydrochloorthiazide. Het carcinogene potentieel van irbesartan en hydrochloorthiazide in combinatie is niet onderzocht in dierstudies.
Irbesartan: er zijn geen tekenen van systemische of doelorgaantoxiciteit gevonden bij de doseringen die in de kliniek worden gebruikt In niet-klinische veiligheidsstudies hoge doses irbesartan (≥ 250 mg/kg/dag bij ratten en ≥ 100 mg/kg/dag bij makaken) veroorzaakte een vermindering van sommige erytrocytenparameters (erytrocyten, hemoglobine, hematocriet) Bij zeer hoge doses (≥ 500 mg/kg/dag), degeneratieve veranderingen in de nieren (zoals interstitiële nefritis, tubulaire dilatatie, basofiele tubuli, verhoogde plasmaconcentraties van ureum en creatinine) Deze effecten worden als secundair beschouwd aan het hypotensieve effect van het geneesmiddel, wat leidt tot verminderde nierperfusie. Bovendien veroorzaakte irbesartan hyperplasie/hypertrofie van juxtaglomerulaire cellen (≥ 90 mg/kg/dag bij ratten en ≥ 10 mg/kg/dag bij makaken). Al deze veranderingen worden geacht te worden veroorzaakt door de farmacologische werking van irbesartan. . Hyperplasie/hypertrofie van juxtaglomerulaire niercellen lijkt niet relevant te zijn voor therapeutische doses irbesartan die bij mensen worden gebruikt.
Er werden geen mutageniciteits-, clastogeniteits- of carcinogeniteitseffecten vastgesteld.
Vruchtbaarheid en reproductievermogen werden niet beïnvloed in onderzoeken bij mannelijke en vrouwelijke ratten, zelfs niet bij doses irbesartan, wat enige toxiciteit bij de ouders veroorzaakte (50 tot 650 mg/kg/dag), inclusief sterfte bij de hoogste dosis. Er werden geen significante effecten waargenomen op het aantal corpora lutei, implantaten of levende foetussen. Irbesartan had geen invloed op de overleving, ontwikkeling of reproductie van het nageslacht. Uit dieronderzoek blijkt dat radioactief gelabeld irbesartan wordt aangetroffen bij foetussen van ratten en konijnen.
Irbesartan wordt uitgescheiden in de melk van zogende ratten.
Dierstudies met irbesartan laten voorbijgaande toxische effecten zien (dilatatie van het nierbekken, hydro-ureter en subcutaan oedeem) bij rattenfoetussen, die na de geboorte afnemen. Abortus of vroege embryo-resorptie werd gemeld bij konijnen in doseringen die maternale toxiciteit kunnen veroorzaken, waaronder de dood.Er werden geen teratogene effecten waargenomen bij ratten of konijnen.
Hydrochloorthiazide: hoewel in sommige experimentele modellen onzeker bewijs van genotoxiciteit en carcinogeniteit is waargenomen, heeft de uitgebreide ervaring met het gebruik bij mensen met hydrochloorthiazide geen correlatie aangetoond tussen het gebruik ervan en een toename van neoplasmata.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Microkristallijne cellulose
Verknoopt natriumcarmellose
Lactosemonohydraat
Magnesium stearaat
Colloïdale silicahydraten
Voorgegelatineerd maïszetmeel
Rode en gele ijzeroxiden (E172)
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren bij temperaturen boven 30°C.
Bewaar in de originele verpakking om het uit de buurt van vocht te houden.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Dozen met 14 tabletten; PVC/PVDC/aluminium blisterverpakkingen.
Dozen met 28 tabletten; PVC/PVDC/aluminium blisterverpakkingen.
Dozen met 56 tabletten; PVC/PVDC/aluminium blisterverpakkingen.
Dozen met 98 tabletten; PVC/PVDC/aluminium blisterverpakkingen.
Dozen met 56 x 1 tablet; PVC / PVDC / aluminium blisters deelbaar per eenheidsdosis
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Ongebruikte medicijnen en afval afkomstig van dit medicijn moeten worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
sanofi-aventis groupe 54 rue La Boétie F-75008 Parijs - Frankrijk
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU / 1/98/085 / 004-006
034190049
034190052
034190064
EU / 1/98/085/008
034190088
EU / 1/98/085/010
034190102
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum van eerste vergunning: 16 oktober 1998 Datum van laatste verlenging: 16 oktober 2008
10.0 DATUM VAN HERZIENING VAN DE TEKST
D.CCE september 2014