Actieve ingrediënten: Tobramycine
TOBRAL 0,3% oogdruppels, oplossing
Bijsluiters van Tobral zijn beschikbaar voor verpakkingsgrootten:- TOBRAL 0,3% oogdruppels, oplossing
- TOBRAL 3 mg/ml oogdruppels met verlengde afgifte
- TOBRAL 0,3% oogzalf
Waarom wordt Tobral gebruikt? Waar is het voor?
FARMACOTHERAPEUTISCHE CATEGORIE
Antibioticum van de aminoglycosidefamilie.
INDICATIES
TOBRAL 0,3% oogdruppels, oplossing is geïndiceerd bij volwassenen en kinderen vanaf één jaar voor de behandeling van infecties van het oog en de adnexa, veroorzaakt door bacteriën die gevoelig zijn voor tobramycine: acute, subacute en catarrale conjunctivitis chronische blefaritis; bacteriële keratitis, dacryocystitis, pre- en postoperatieve profylaxe bij chirurgie van het voorste segment.
Contra-indicaties Wanneer Tobral niet mag worden gebruikt
Gebruik TOBRAL 0,3% oogdruppels niet als u allergisch (overgevoelig) bent voor tobramycine of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in de rubriek "Samenstelling").
Voorzorgen bij gebruik Wat u moet weten voordat u Tobral inneemt
- Bij sommige patiënten kan overgevoeligheid voor topisch toegediende aminoglycoside-antibiotica optreden. Als zich tijdens het gebruik van dit geneesmiddel overgevoeligheid ontwikkelt, dient de behandeling te worden gestaakt.
- Er kan kruisovergevoeligheid voor andere aminoglycosiden optreden, daarom moet de mogelijkheid worden overwogen dat patiënten die gesensibiliseerd zijn voor topisch toegediende tobramycine ook gevoelig kunnen zijn voor andere topisch en/of systemisch toegediende aminoglycosiden.
- Ernstige bijwerkingen zoals neurotoxiciteit, ototoxiciteit en nefrotoxiciteit zijn opgetreden bij patiënten die werden behandeld met systemische tobramycine. Voorzichtigheid is geboden wanneer TOBRAL gelijktijdig wordt toegediend met systemische therapie met tobramycine.
- Net als bij andere antibiotica kan langdurig gebruik van TOBRAL oogdruppels een abnormale groei van niet-gevoelige organismen veroorzaken, waaronder schimmels.Als superinfectie optreedt, moet een geschikte therapie worden ingesteld.
- Het wordt aanbevolen om geen contactlenzen te dragen bij de behandeling van een "ooginfectie".
- TOBRAL oogdruppels bevatten benzalkoniumchloride, dat oogirritatie kan veroorzaken en waarvan bekend is dat het zachte contactlenzen verkleurt. Vermijd contact met zachte contactlenzen. Als patiënten contactlenzen mogen dragen, ja, dan moet u hen opdragen hun contactlenzen te verwijderen voordat TOBRAL wordt aangebracht oogdruppels en wacht ten minste 15 minuten na indruppeling van de dosis voordat u ze opnieuw inbrengt.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Tobral . veranderen
Vertel uw arts of apotheker als u andere geneesmiddelen gebruikt of kort geleden heeft gebruikt. Dit geldt ook voor geneesmiddelen die u zonder voorschrift kunt krijgen. Als u meer dan één actueel geneesmiddel voor het oog gebruikt, wacht dan ten minste 5 minuten tussen het indruppelen van elk geneesmiddel. Oftalmische zalf moet als laatste worden gebruikt.
Onverenigbaarheid
Het tyloxapol-bestanddeel in de oogdruppels is onverenigbaar met tetracycline.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
Vraag uw arts om advies voordat u een geneesmiddel inneemt. Als u zwanger bent of in verwachting bent, of als u borstvoeding geeft, vraag dan uw arts om advies voordat u dit medicijn gebruikt.
Zwangerschap
Gegevens over lokaal oculair gebruik van tobramycine bij zwangere vrouwen bestaan niet of zijn beperkt in aantal Dierproeven hebben reproductietoxiciteit aangetoond Tobramycine wordt niet aanbevolen tijdens de zwangerschap.
Zwangerschap
Het is niet bekend of tobramycine wordt uitgescheiden in de moedermelk na plaatselijke oculaire toediening. Tobramycine wordt uitgescheiden in de moedermelk na systemische toediening. Een risico voor zuigelingen kan niet worden uitgesloten. Er moet worden besloten of de borstvoeding moet worden gestaakt of dat de behandeling met tobramycine moet worden gestaakt, waarbij het voordeel van borstvoeding voor het kind en het voordeel van behandeling voor de vrouw in overweging moeten worden genomen.
Rijvaardigheid en het gebruik van machines
TOBRAL heeft geen of tijdelijk effect op de rijvaardigheid en op het vermogen om machines te bedienen. Voorbijgaand wazig zien of andere visuele stoornissen kunnen de rijvaardigheid en het vermogen om machines te bedienen beïnvloeden.Als wazig zien optreedt na instillatie, moet de patiënt wachten tot het zicht helder is voordat hij gaat rijden en machines gaat bedienen.
Belangrijke informatie met betrekking tot een hulpstof in TOBRAL 0,3% oogdruppels, oplossing
TOBRAL 0,3% oogdruppels bevatten een conserveermiddel (benzalkoniumchloride) dat oogirritatie kan veroorzaken en waarvan bekend is dat het zachte contactlenzen verkleurt. Het gebruik van contactlenzen wordt niet aanbevolen tijdens de behandeling van een " ooginfectie Als u contactlenzen mag dragen , verwijder ze voordat u TOBRAL 0,3% oogdruppels gebruikt en wacht 15 minuten voordat u ze weer aanbrengt.
Dosering en wijze van gebruik Hoe Tobral te gebruiken: Dosering
Gebruik TOBRAL oogdruppels alleen voor instillatie in het oog.
Gebruik dit geneesmiddel altijd zoals voorgeschreven door uw arts of apotheker.
Druppel in de conjunctivale zak vier keer per dag twee druppels in de acute vormen en drie keer per dag in de chronische vormen, volgens medisch voorschrift.
Pediatrische populatie
TOBRAL 0,3% oogdruppels kunnen bij kinderen vanaf één jaar worden gebruikt in dezelfde doseringen als bij volwassenen. De veiligheid en werkzaamheid bij kinderen jonger dan één jaar zijn niet vastgesteld en er zijn geen gegevens beschikbaar.
Als een druppel uw oog mist, probeer het dan opnieuw.
Overdosering Wat te doen als u te veel Tobral heeft ingenomen
OVERDOSERING
Als u meer van het geneesmiddel heeft gebruikt dan u zou mogen, was uw oog dan onmiddellijk met warm water.
Er worden echter geen toxische effecten verwacht. Gebruik het geneesmiddel pas weer als het tijd is voor de volgende toediening.
WAT MOET U DOEN ALS U EEN OF MEER DOSES BENT VERGETEN?
Als u bent vergeten TOBRAL 0,3% oogdruppels te gebruiken, ga dan verder met de behandeling met de volgende dosis zoals gepland. Als het echter bijna tijd is voor de volgende dosis, sla dan de gemiste dosis over en ga terug naar het normale doseringsschema. Gebruik geen dubbele dosis om een vergeten dosis in te halen.
ALS U TWIJFEL BENT OVER HET GEBRUIK VAN DIT GENEESMIDDEL, NEEM DAN CONTACT OP MET UW ARTS OF APOTHEKER
Bijwerkingen Wat zijn de bijwerkingen van Tobral
Zoals alle geneesmiddelen kan TOBRAL 0,3% oogdruppels bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
De volgende bijwerkingen in onderstaande tabel zijn gemeld tijdens klinische onderzoeken met tobramycine oogdruppels en/of oogzalf en zijn geclassificeerd volgens de volgende conventie: zeer vaak (≥1/10), vaak (≥1/100,
De onderstaande tabel geeft een overzicht van aanvullende bijwerkingen die zijn vastgesteld tijdens postmarketingervaring.De frequentie kan met de beschikbare gegevens niet worden bepaald.
Beschrijving van de gemarkeerde bijwerkingen
Ernstige bijwerkingen zoals neurotoxiciteit, ototoxiciteit en nefrotoxiciteit zijn opgetreden bij patiënten die werden behandeld met systemische tobramycine. Bij sommige patiënten kan overgevoeligheid voor topisch toegediende aminoglycosiden optreden.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via de website van het Italiaanse Geneesmiddelenbureau: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel
Vervaldatum en retentie
Niet gebruiken na de vervaldatum die staat vermeld op de buitenverpakking en de fles. De vervaldatum verwijst naar de laatste dag van de maand.
Niet bewaren boven 25°C.
De vervaldatum verwijst naar het product in intacte verpakking, correct bewaard.
Het product mag niet meer dan 30 dagen na eerste opening van de container worden gebruikt.
Buiten het zicht en bereik van kinderen houden.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
SAMENSTELLING
100 ml bevatten: Werkzaam bestanddeel: tobramycine 0,3 g. Hulpstoffen: tyloxapol, benzalkoniumchloride, boorzuur, watervrij natriumsulfaat, natriumchloride, gezuiverd water.
FARMACEUTISCHE VORM EN INHOUD
Steriele oftalmische oplossing. Druppelflesje van 5 ml.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
TOBRAL 0,3%
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Oogdruppels, oplossing
100ml bevatten:
Actief principe: tobramycine 0,3 g.
Hulpstoffen met bekend effect: benzalkoniumchloride.
oogzalf
100 gram bevat:
Actief principe: tobramycine 0,3 g.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Oogdruppels, oplossing. Oogheelkundige zalf.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
TOBRAL is geïndiceerd bij volwassenen en kinderen vanaf één jaar voor de behandeling van oog- en adnexale infecties veroorzaakt door bacteriën die gevoelig zijn voor tobramycine: acute, subacute en chronische catarrale conjunctivitis, blefaritis, bacteriële keratitis; dacryocystitis; pre- en postoperatieve profylaxe bij chirurgie van het voorste segment.
04.2 Dosering en wijze van toediening
Oogdruppels, oplossing
Druppel in de conjunctivale zak vier keer per dag twee druppels in de acute vormen en drie keer per dag in de chronische vormen, volgens medisch voorschrift.
oogzalf
Breng volgens medisch voorschrift twee tot vier keer per dag aan in de conjunctivale zak.
Pediatrische populatie
TOBRAL oogdruppels, oplossing en TOBRAL oogzalf kunnen bij kinderen vanaf één jaar worden gebruikt in dezelfde dosering als bij volwassenen. De momenteel beschikbare gegevens worden beschreven in rubriek 5.1.
De veiligheid en werkzaamheid bij kinderen jonger dan één jaar zijn niet vastgesteld en er zijn geen gegevens beschikbaar.
Wijze van toediening
Alleen voor oogheelkundig gebruik
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
- Bij sommige patiënten kan overgevoeligheid voor topisch toegediende aminoglycoside-antibiotica optreden. Als zich tijdens het gebruik van dit geneesmiddel overgevoeligheid ontwikkelt, dient de behandeling te worden gestaakt.
- Er kan kruisovergevoeligheid voor andere aminoglycosiden optreden. Daarom moet rekening worden gehouden met de mogelijkheid dat patiënten die gesensibiliseerd zijn voor topisch toegediende tobramycine ook gevoelig zijn voor andere topisch en/of systemisch toegediende aminoglycosiden.
- Ernstige bijwerkingen zoals neurotoxiciteit, ototoxiciteit en nefrotoxiciteit zijn opgetreden bij patiënten die werden behandeld met systemische tobramycine. Voorzichtigheid is geboden wanneer TOBRAL gelijktijdig wordt toegediend met systemische therapie met tobramycine.
- Net als bij andere antibiotica kan langdurig gebruik van TOBRAL oogdruppels of oogzalf abnormale groei van niet-gevoelige organismen veroorzaken, inclusief schimmels.Als superinfectie optreedt, moet een geschikte therapie worden ingesteld.
- Het wordt aanbevolen om geen contactlenzen te dragen bij de behandeling van een ooginfectie.
- TOBRAL oogdruppels bevatten benzalkoniumchloride, dat oogirritatie kan veroorzaken en waarvan bekend is dat het zachte contactlenzen verkleurt. Vermijd contact met zachte contactlenzen. Als patiënten contactlenzen mogen dragen, moeten ze worden geïnstrueerd deze te verwijderen voordat TOBRAL wordt toegediend oogdruppels en wacht ten minste 15 minuten na indruppeling van de dosis voordat u ze opnieuw inbrengt.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Er zijn geen klinisch relevante interacties met topisch oculair gebruik beschreven.
Als u meer dan één actueel geneesmiddel voor het oog gebruikt, wacht dan ten minste 5 minuten tussen het indruppelen van elk geneesmiddel. Oftalmische zalf moet als laatste worden gebruikt.
04.6 Zwangerschap en borstvoeding
Vruchtbaarheid
Er zijn geen onderzoeken uitgevoerd om het effect op de menselijke vruchtbaarheid van lokale oculaire toediening van TOBRAL oogdruppels en TOBRAL oogzalf te evalueren.
Zwangerschap
Gegevens over lokaal oculair gebruik van tobramycine bij zwangere vrouwen bestaan niet of zijn beperkt in aantal Dierproeven hebben reproductietoxiciteit aangetoond Tobramycine wordt niet aanbevolen tijdens de zwangerschap.
Voedertijd
Het is niet bekend of tobramycine wordt uitgescheiden in de moedermelk na plaatselijke oculaire toediening. Tobramycine wordt uitgescheiden in de moedermelk na systemische toediening. Een risico voor zuigelingen kan niet worden uitgesloten. Er moet worden besloten of de borstvoeding moet worden gestaakt of dat de behandeling met tobramycine moet worden gestaakt, waarbij het voordeel van borstvoeding voor het kind en het voordeel van behandeling voor de vrouw in overweging moeten worden genomen.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
TOBRAL heeft geen of tijdelijk effect op de rijvaardigheid en op het vermogen om machines te bedienen. Voorbijgaand wazig zien of andere visuele stoornissen kunnen de rijvaardigheid en het vermogen om machines te bedienen beïnvloeden.Als wazig zien optreedt na instillatie, moet de patiënt wachten tot het zicht helder is voordat hij gaat rijden en machines gaat bedienen.
04.8 Bijwerkingen
De volgende bijwerkingen in onderstaande tabel zijn gemeld tijdens klinische onderzoeken met tobramycine oogdruppels en/of oogzalf en zijn geclassificeerd volgens de volgende conventie: zeer vaak (≥1/10), vaak (≥1/100,
De onderstaande tabel geeft een overzicht van aanvullende bijwerkingen die zijn vastgesteld tijdens postmarketingervaring.De frequentie kan met de beschikbare gegevens niet worden bepaald.
Beschrijving van de gemarkeerde bijwerkingen
Ernstige bijwerkingen zoals neurotoxiciteit, ototoxiciteit en nefrotoxiciteit zijn opgetreden bij patiënten die werden behandeld met systemische tobramycine (zie rubriek 4.4).
Bij sommige patiënten kan overgevoeligheid voor topisch toegediende aminoglycosiden optreden (zie rubriek 4.4).
Melding van vermoedelijke bijwerkingen.
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk, omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt.Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Italiaanse Geneesmiddelenbureau. , Website: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Vanwege de eigenschappen van dit geneesmiddel worden er geen toxische effecten verwacht in geval van oogheelkundige overdosering of accidentele inname van een hele fles oogdruppels of een tube zalf.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Therapeutische geneesmiddelencategorie: oogheelkundig - anti-infectiva - antibiotica.
ATC-code: S01AA12 tobramycine.
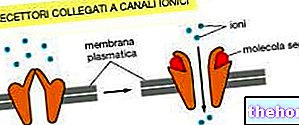
Werkingsmechanisme
TOBRAL oogdruppels en oogzalf bevatten tobramycine, een snelwerkend bactericide aminoglycoside antibioticum. Het oefent zijn primaire effect uit op bacteriële cellen door de synthese en assemblage van peptiden in het ribosoom te remmen.
Weerstandsmechanisme:
Resistentie tegen tobramycine ontwikkelt zich via verschillende mechanismen, waaronder: 1) veranderingen van de ribosomale subeenheid in de bacteriële cel; 2) interferentie met het transport van tobramycine in de cel 3) inactivering van tobramycine door een reeks adenyl-, fosforyl- en acetyl-enzymen De genetische informatie voor de productie van inactiverende enzymen kan worden getransporteerd op bacteriële chromosomen of op plasmiden. Kruisresistentie met andere aminoglycosiden kan optreden.
Breekpunten
De breekpunten en het spectrum in vitro Het volgende is gebaseerd op systemisch gebruik. Deze breekpunten zijn mogelijk niet van toepassing op lokaal oculair gebruik van het geneesmiddel omdat lokaal hogere concentraties worden verkregen en de fysische/chemische eigenschappen de activiteit van het geneesmiddel op de toedieningsplaats kunnen beïnvloeden. opgesteld door de European Committee on Antimicrobial Susceptibility Tests, zijn de volgende breekpunten gedefinieerd voor tobramycine:
• Enterobacteriën S ≤ 2 mg/l, R> 4 mg/l
• Pseudomonas S ≤ 4 mg/l, R> 4 mg/l
• Acinetobacter S ≤ 4 mg/l, R> 4 mg/l
• Stafylokokken S ≤ 1 mg/l, R> 1 mg/l
• Niet soortgebonden S ≤ 2 mg/l, R> 4 mg/l
De onderstaande informatie geeft slechts een ruwe indicatie van de waarschijnlijkheid dat micro-organismen vatbaar zijn voor de tobramycine die aanwezig is in TOBRAL. Bacteriesoorten die zijn gevonden bij uitwendige ooginfecties zoals conjunctivitis worden hier vermeld.
De prevalentie van verworven resistentie voor de geïdentificeerde soorten kan geografisch en in de tijd variëren; Lokale informatie over resistentie is daarom wenselijk, vooral bij de behandeling van ernstige infecties. Indien nodig moet deskundig advies worden ingewonnen als de prevalentie van lokale resistentie zodanig is dat het nut van tobramycine bij ten minste een soort infectie twijfelachtig is.
* weerstand groter dan 50%
Pediatrische populatie
Meer dan 600 pediatrische patiënten namen deel aan 10 klinische onderzoeken met tobramycine oogdruppels of oogzalf voor de behandeling van bacteriële conjunctivitis, blefaritis of blepharoconjunctivitis. Deze patiënten varieerden in leeftijd van 1 tot 18 jaar. Het veiligheidsprofiel bij pediatrische patiënten bleek vergelijkbaar te zijn met dat van volwassen patiënten. Vanwege een gebrek aan gegevens kan geen doseringsadvies worden gegeven voor kinderen jonger dan 1 jaar.
05.2 Farmacokinetische eigenschappen
Onderzoek naar de penetratie van tobramycine op oculair niveau, na topische toediening bij konijnen, heeft aangetoond dat de maximale concentratie van tobramycine in het hoornvlies 0,5 uur na toediening en 1,5 - 2,5 uur in het kamerwater wordt gedetecteerd.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
De LD50 van intraveneus toegediende tobramycine bij muizen is 118 mg/kg. Acute toxiciteitsstudies, door lokale oculaire toediening bij konijnen, hebben aangetoond dat TOBRAL geen lokale irriterende effecten heeft. De toediening van TOBRAL, via topische oculaire route herhaald in het konijn gedurende drie weken, vertoonde geen irriterende effecten op lokaal niveau, evenals farmacotoxische effecten op systemisch niveau.
Embryo-foetale toxiciteit, carcinogenese en mutagenese
Studies uitgevoerd bij ratten en konijnen met doses die 33 keer hoger zijn dan de normale systemische dosis voor de mens, hebben aangetoond dat dit antibioticum niet mutageen of carcinogeen is en geen toxische effecten heeft op embryo-foetaal niveau.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Oogdruppels, oplossing
tyloxapol, boorzuur, watervrij natriumsulfaat, natriumchloride, benzalkoniumchloride, gezuiverd water.
oogzalf
chloorbutanol, vaseline-olie, vaseline.
06.2 Incompatibiliteit
Oogdruppels, oplossing: de tyloxapol-component is onverenigbaar met tetracycline.
06.3 Geldigheidsduur
3 jaar, zowel voor oogdruppels als oogzalf.
Oogdruppels, oplossing: het product mag niet meer dan 30 dagen na eerste opening van de container worden gebruikt
oogzalf: het product mag niet meer dan 28 dagen na eerste opening van de container worden gebruikt
06.4 Speciale voorzorgsmaatregelen bij bewaren
Oogdruppels, oplossing: niet bewaren boven 25°C.
Oogzalf: niet bewaren boven 25°C. Niet in de koelkast bewaren.
Voor bewaarcondities na eerste opening, zie rubriek 6.3.
Niet gebruiken na de vervaldatum.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Druppelflesje van 5 ml in polyethyleen met lage dichtheid.
3,5 g aluminium buis met HDPE (Ostalene) en LPDE (Lupolene) oogheelkundige tip en HDPE-sluiting.
06.6 Instructies voor gebruik en verwerking
Ongebruikte medicijnen en afval afkomstig van dit medicijn moeten worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
ALCON Italia S.p.A., Viale Giulio Richard 1 / B, 20143 Milaan.
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Oogdruppels, oplossing: AIC n. 025860026
Oogzalf: AIC n. 025860077
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Eerste autorisatie:
oogdruppels, oplossing: 20 augustus 1985
oogzalf: 27 juli 1987
Laatste verlenging: mei 2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
09/2014