Actieve ingrediënten: Ribosomale fracties bestaande uit bacteriële ribosomen en Membraanfracties van de soort Klebsiella pneumoniae, Streptococcus pneumoniae, Streptococcus pyogenes, Haemophilus influenzae
BIOMUNIL-tabletten
BIOMUNIL Granulaat voor suspensies
Indicaties Waarom wordt Biomunil gebruikt? Waar is het voor?
FARMACOTHERAPEUTISCHE CATEGORIE
Bacteriële vaccins.
THERAPEUTISCHE INDICATIES
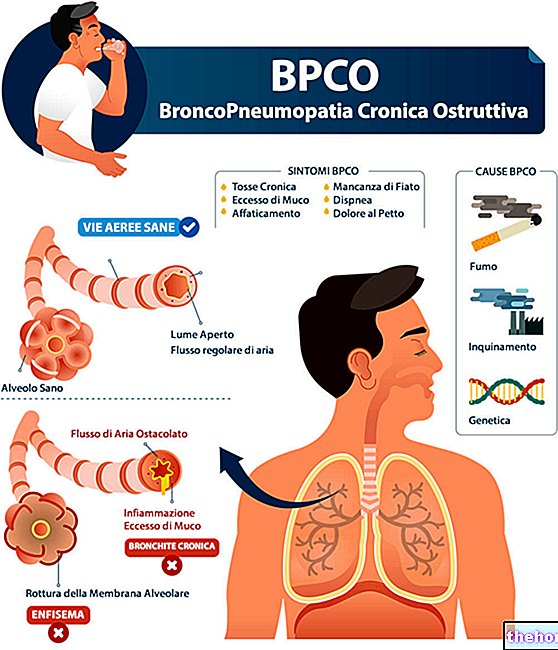
Profylaxe van terugkerende bacteriële infecties van de bovenste luchtwegen bij kinderen met een aantal episoden dat hoger is dan verwacht voor de leeftijd. BIOMUNIL kan helpen het aantal en de intensiteit van infectieuze episodes te verminderen.
Contra-indicaties Wanneer Biomunil niet mag worden gebruikt
Overgevoeligheid voor de werkzame stof of voor één van de hulpstoffen.
Het gebruik van het preparaat bij patiënten met auto-immuunziekten is gecontra-indiceerd.
Voorzorgsmaatregelen bij gebruik Wat u moet weten voordat u Biomunil® inneemt
Aangezien er geen gegevens beschikbaar zijn uit onderzoeken bij zwangere vrouwen, verdient het de voorkeur om het gebruik van BIOMUNIL bij zwangere vrouwen en vrouwen die borstvoeding geven te vermijden (zie Zwangerschap en borstvoeding).
Bij personen bij wie hyperreactiviteit kan worden vermoed, is het raadzaam om een type behandeling te volgen met progressief toenemende doses.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Biomunil . veranderen
Vertel het uw arts of apotheker als u onlangs andere geneesmiddelen heeft gebruikt, ook zonder voorschrift.
Er zijn geen interactiestudies uitgevoerd.
Waarschuwingen Het is belangrijk om te weten dat:
Wees extra voorzichtig met BIOMUNIL:
- als u koorts (≥ 39 ° C) van onverklaarbare oorsprong krijgt na gebruik van dit geneesmiddel, stop dan met de behandeling en raadpleeg zo snel mogelijk uw arts;
- als u allergisch bent voor dit geneesmiddel, stop dan met de behandeling;
- als u aan astma lijdt. Astma-aanvallen veroorzaakt door de toediening van geneesmiddelen met bacterieextracten die het immuunsysteem stimuleren, zijn beschreven bij astmapatiënten. Als u astma-aanvallen krijgt, stop dan met de behandeling en herhaal deze niet;
- u mag dit medicijn niet gebruiken als u een acute darminfectie heeft;
Zwangerschap en borstvoeding
Vraag uw arts of apotheker om advies voordat u een geneesmiddel inneemt.
Aangezien er geen studies zijn met betrekking tot het gebruik van BIOMUNIL tijdens zwangerschap en borstvoeding, moet u het gebruik van dit geneesmiddel tijdens deze periodes vermijden.
Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
BIOMUNIL heeft geen invloed op de rijvaardigheid of het vermogen om machines te bedienen.
Belangrijke informatie over enkele ingrediënten:
BIOMUNIL-tabletten bevatten sorbitol. Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt. BIOMUNIL granulaat voor suspensie bevat mannitol. Het kan een licht laxerend effect hebben.
Dosering en wijze van gebruik Hoe gebruikt u Biomunil: Dosering
Dosering
BIOMUNIL granulaat voor orale suspensie kan worden toegediend aan kinderen vanaf 2 jaar.
BIOMUNIL-tabletten zijn gereserveerd voor kinderen ouder dan 6 jaar.
Dosering:
1e maand:
1 tablet of sachet 's morgens op een lege maag gedurende 4 opeenvolgende dagen per week gedurende 3 opeenvolgende weken.
Vanaf de 2e maand:
1 tablet of sachet 's morgens op een lege maag gedurende 4 opeenvolgende dagen per maand gedurende de volgende 5 maanden.
Wijze van toediening
De inhoud van het sachet oplossen in een half glas water De orale suspensie moet onmiddellijk worden gedronken.
Overdosering Wat moet u doen als u te veel Biomunil heeft ingenomen?
Er zijn geen gevallen van overdosering gemeld
In geval van accidentele inname/inname van een overmatige dosis BIOMUNIL, waarschuw dan onmiddellijk uw arts of neem contact op met het dichtstbijzijnde ziekenhuis.
Als u vragen heeft over het gebruik van BIOMUNIL, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Biomunil
Zoals alle geneesmiddelen kan BIOMUNIL bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
De onderstaande tabel toont de bijwerkingen die zijn waargenomen in negen klinische onderzoeken, waaronder in totaal 1.231 patiënten die werden behandeld met oraal BIOMUNIL, waarvoor de causaliteitsbeoordeling "niet was uitgesloten" en in spontane meldingen.
Bijwerkingen zijn gerangschikt volgens de systeem/orgaanklassen van MedDRA en worden hieronder gedefinieerd als: zeer vaak (≥ 1/10), vaak (≥ 1/100 tot <1/10), soms (≥ 1 / 1.000, <1/100) , zelden (≥ 1 / 10.000, < 1 / 1.000), zeer zelden (< 1 / 10.000) of niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Er werden geen bijwerkingen gevonden met de frequentie "zeer zelden", "zelden" of "zeer vaak" en daarom zijn deze frequenties niet weergegeven in de tabel.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. Bijwerkingen kunnen ook rechtstreeks worden gemeld via het nationale meldsysteem op "www.agenziafarmaco.gov.it/it/responsabili". Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Vervaldatum: zie de vervaldatum die op de verpakking staat vermeld.
De vervaldatum verwijst naar het product in intacte verpakking, correct bewaard.
Waarschuwing: gebruik het geneesmiddel niet meer na de vervaldatum die staat vermeld op de verpakking.
Tabletten: Bewaren bij een temperatuur van maximaal 30 ° C.
Bewaar in de originele verpakking.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Buiten het zicht en bereik van kinderen houden.
Samenstelling en farmaceutische vorm
SAMENSTELLING
Elke tablet of elk sachet granulaat voor orale suspensie bevat:
Actieve ingrediënten: Ribosomale fracties van:
Klebsiella pneumoniae 3,5 delen
Streptococcus pneumoniae 3.0 onderdelen
Streptococcus pyogenes (groep A) 3,0 delen
Haemophilus influenzae 0,5 delen
Membraanfracties van
Klebsiella pneumoniae 15 delen
voor een lyofilisaat gelijk aan 0,525 mg ribosomaal RNA
Lijst van hulpstoffen
Tabletten:
Colloïdaal silica 1,5 mg
Magnesiumstearaat 6 mg
Sorbitol naar smaak tot 294 mg
Sachets met granulaat voor orale suspensie:
polyvinylpyrrolidon 10 mg
mannitol 488,12 mg
FARMACEUTISCHE VORM EN INHOUD
12 of 20 tabletten voor oraal gebruik in een gelithografeerde kartonnen doos
12 of 20 sachets granulaat voor orale suspensie in een gelithografeerde kartonnen doos
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
BIOMUNIL
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
BIOMUNIL-tabletten
Actieve principes:
ribosomale fracties bestaande uit bacteriële ribosomen in de volgende verhoudingen:
Klebsiella pneumoniae 3,5 delen
Streptococcus pneumoniae 3.0 onderdelen
Streptococcus pyogenes (groep A) 3,0 delen
Haemophilus influenzae 0,5 delen
Membraanfracties van Klebsiella pneumoniae 15 delen
voor een lyofilisaat gelijk aan 0,525 mg ribosomaal RNA
Hulpstoffen met bekende effecten: sorbitol.
BIOMUNIL granulaat voor orale suspensie
Actieve principes:
ribosomale fracties bestaande uit bacteriële ribosomen in de volgende verhoudingen:
Klebsiella pneumoniae 3,5 delen
Streptococcus pneumoniae 3.0 onderdelen
Streptococcus pyogenes (groep A) 3,0 delen
Haemophilus influenzae 0,5 delen
Membraanfracties van Klebsiella pneumoniae 15 delen
voor een lyofilisaat gelijk aan 0,525 mg ribosomaal RNA
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
03.0 FARMACEUTISCHE VORM
Tabletten, voor oraal gebruik.
Korrels voor orale suspensie.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Profylaxe van terugkerende bacteriële infecties van de bovenste luchtwegen bij kinderen met een aantal episoden dat hoger is dan verwacht voor de leeftijd.
BIOMUNIL kan helpen het aantal en de intensiteit van infectieuze episodes te verminderen.
04.2 Dosering en wijze van toediening
BIOMUNIL granulaat voor orale suspensie kan worden toegediend aan kinderen vanaf 2 jaar.
BIOMUNIL-tabletten zijn gereserveerd voor kinderen ouder dan 6 jaar.
Dosering:
1e maand:
1 tablet of sachet 's morgens op een lege maag gedurende 4 opeenvolgende dagen per week gedurende 3 opeenvolgende weken.
Vanaf de 2e maand:
1 tablet of sachet 's morgens op een lege maag gedurende 4 opeenvolgende dagen per maand gedurende de volgende 5 maanden.
Los de inhoud van het sachet op in een half glas water.
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen van het vaccin.
Auto-immuunziekten.
Acute darminfecties.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Bij personen bij wie hyperreactiviteit kan worden vermoed, is het raadzaam om een type behandeling te volgen met progressief toenemende doses.
De behandeling moet worden stopgezet in geval van koorts, vooral aan het begin van de behandeling.
De patiënt moet worden geïnformeerd over de mogelijkheid als een zeldzame ongewenste gebeurtenis van verhoogde koorts boven 39 ° C, geïsoleerd en zonder bekende oorzaak, en het type koorts moet worden onderscheiden van de koorts die ontstaat als gevolg van de oorspronkelijke pathologie, op basis van van de larynx, neusaandoeningen of otologische; in dat geval moet de behandeling worden gestaakt en niet worden hervat.
Gelijktijdige inname van een ander immunostimulant moet worden vermeden.
In sommige gevallen is het ontstaan van astma-aanvallen waargenomen bij gepredisponeerde patiënten na inname van geneesmiddelen die bacterieextracten bevatten.In dit geval mag BIOMUNIL niet verder worden gebruikt.
In geval van overgevoeligheidsreacties moet de behandeling onmiddellijk worden stopgezet en niet opnieuw worden gestart.
BIOMUNIL wordt niet aanbevolen tijdens de zwangerschap. Het geneesmiddel mag alleen worden toegediend in geval van werkelijke noodzaak onder direct toezicht van de arts (zie rubriek 4.6).
Belangrijke informatie over enkele ingrediënten
Het geneesmiddel bevat sorbitol. Patiënten met zeldzame erfelijke aandoeningen als fructose-intolerantie mogen dit geneesmiddel niet gebruiken.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Er zijn geen interactiestudies uitgevoerd. Er wordt een interval van 4 weken aanbevolen tussen het einde van de behandeling met BIOMUNIL en het begin van de toediening van een vaccin.De immuunrespons kan worden geremd bij personen met een aangeboren of verworven immunodeficiëntie, bij immunosuppressieve therapie of bij gebruik van corticosteroïden.
04.6 Zwangerschap en borstvoeding
Er zijn geen gegevens over het gebruik van BIOMUNIL bij zwangere vrouwen.
Dierstudies wijzen niet op directe of indirecte schadelijke effecten met betrekking tot reproductietoxiciteit.
Als voorzorgsmaatregel moet het gebruik van BIOMUNIL tijdens zwangerschap en borstvoeding echter worden vermeden.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
BIOMUNIL heeft geen invloed op de rijvaardigheid of het vermogen om machines te bedienen.
04.8 Bijwerkingen
De onderstaande tabel toont de bijwerkingen die zijn waargenomen in negen klinische onderzoeken, waaronder in totaal 1.231 patiënten die werden behandeld met oraal BIOMUNIL, waarvoor de causaliteitsbeoordeling "niet was uitgesloten" en in spontane meldingen.
Bijwerkingen zijn vermeld volgens de MedDRA-systeem/orgaanklasse en worden hieronder gedefinieerd als:
zeer vaak (≥ 1/10), vaak (≥ 1/100,
Er werden geen bijwerkingen gevonden met de frequentie "zeer zelden", "zelden" of "zeer vaak" en daarom zijn deze frequenties niet weergegeven in de tabel.
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres http: //www.agenziafarmaco.gov.it/it/responsabili
04.9 Overdosering
Er zijn geen gevallen van overdosering gemeld.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: bacteriële vaccins
ATC-code: J07AX
BIOMUNIL draagt bij tot de ontwikkeling van niet-specifieke en specifieke immuunresponsen, door een verbetering van de bacteriële klaring en een stimulering van antivirale reacties.
De immunogene en immunomodulerende eigenschappen van BIOMUNIL zijn vastgesteld in dier- en mensstudies, wat aangeeft dat BIOMUNIL het darmslijmvlies kan passeren.Dit werd bevestigd met behulp van een model. in vitro die het darmepitheel reproduceerde.
Van de membraanfractie en ribosomale fracties van K pneumoniae, een Gram-negatieve bacterie, is in in-vitro-onderzoeken aangetoond dat ze een interactie aangaan met aangeboren immuniteitscelreceptoren (TLR's), waardoor activering van NK-cellen wordt geïnduceerd, met productie van defensines, een verhoogde functie van neutrofielen (adhesie en migratie), activering van het monocyt-macrofaagsysteem, chemotactische activiteit op T-lymfocyten.
De studie van ribosomen door biochemische karakterisering toonde de aanwezigheid op ribosomen van antigene epitopen van het bacteriële membraan van Klebsiella pneumoniae. Zo werken ribosomen als antigene vectoren en induceren ze specifieke antilichaam-afscheidende cellen in het bloed en de slijmvliezen die plaatselijk specifieke antilichamen produceren.
05.2 Farmacokinetische eigenschappen
BIOMUNIL is biologisch beschikbaar en bereikt de plaques van Peyer voor de stimulatie van immunocompetente cellen.
Kinetische studies bij ratten en honden hebben slechts een bescheiden absorptie aangetoond van de macromoleculen waaruit BIOMUNIL intragastrisch wordt toegediend.
Na 6 uur werden plasmaspiegels in de orde van grootte van 1-2% van de toegediende dosis, leverspiegels van 0,25% en darmspiegels van 0,08% gedetecteerd.
Urine-excretie was 33% na 72 uur.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Effecten in niet-klinische onderzoeken werden alleen waargenomen bij blootstellingsniveaus die als voldoende boven de maximale menselijke blootstelling werden beschouwd, wat wijst op weinig relevantie voor klinisch gebruik.
Acute toxiciteit is extreem laag; er werden geen sterfgevallen of tekenen van toxiciteit waargenomen met de tabletformulering, hoewel enkelvoudige doses van meer dan 3000 maal de dosis voor de mens werden toegediend; met de granulaatformulering werd bij muizen en ratten een LD50 bepaald, gelijk aan ongeveer 2500 maal de humane dosis. Chronische toxiciteit werd beoordeeld na herhaalde toediening bij zowel ratten als honden: bij geen enkel dier werden tekenen van toxiciteit of veranderingen in ontwikkeling, normaal gedrag en gewichtstoename gevonden; bij de behandelde dieren waren de hematologische, biochemische parameters en de histologische bevindingen consistent binnen de normale waarden. Er werd gezocht naar mogelijke embryotoxische en/of teratogene effecten bij verschillende diersoorten: muizen, ratten en konijnen. Er werden geen negatieve effecten op de vruchtbaarheid, op het percentage placentaire reabsorptie naar voren gebracht, noch afwijkingen bij foetussen of pasgeborenen bij microscopisch onderzoek van de ingewanden en skelet.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Tabletten:
Colloïdaal silica 1,5 mg
Magnesiumstearaat 6 mg
Sorbitol naar smaak tot 294 mg
Sachets met granulaat voor orale suspensie:
Polyvinylpyrrolidon 10 mg
Mannitol 488,12 mg
06.2 Incompatibiliteit
Niet relevant
06.3 Geldigheidsduur
Tabletten: 3 jaar
Korrels voor orale suspensie: 3 jaar
06.4 Speciale voorzorgsmaatregelen bij bewaren
Tabletten: Bewaren bij een temperatuur van maximaal 30 ° C
Granulaat voor orale suspensie: voor dit geneesmiddel zijn er geen speciale bewaarcondities.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
- 12 tabletten in Al / PVC blisterverpakkingen
- 20 tabletten in Al / PVC blisterverpakkingen
- 12 sachets granulaat voor orale suspensie in papier / Al / PVC
- 20 sachets granulaat voor orale suspensie in papier / Al / PVC
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies voor verwijdering.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
LUSOFARMACO
Luso Farmaco Instituut van Italië S.p.A.
Milanofiori - Straat 6 - Gebouw L - Rozzano (MI)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
12 tabletten: 026730022
12 sachets granulaat voor orale suspensie: 026730034
20 tabletten: 026730046
20 sachets granulaat voor orale suspensie: 026730059
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
12 tabletten: 31.10.94 / 1.06.10
12 sachets granulaat voor orale suspensie: 28.10.94 / 1.06.10
20 tabletten: 27.07.00 / 1.06.10
20 sachets granulaat voor orale suspensie: 27.07.00 / 1.06.10
10.0 DATUM VAN HERZIENING VAN DE TEKST
januari 2015